Как распознать железодефицитную анемию у пациентов с ХСН. Какие методы диагностики наиболее информативны. Какие препараты железа эффективны при ХСН. Каковы особенности лечения ЖДА у пожилых пациентов с сердечной недостаточностью.
Анемия и хроническая сердечная недостаточность: патогенетическая связь
Хроническая сердечная недостаточность (ХСН) и анемия часто сосуществуют у пациентов, особенно пожилого возраста. Анемия выявляется примерно у 30% амбулаторных пациентов с ХСН и у 50% госпитализированных. Причины развития анемии при ХСН многообразны:
- Нарушение функции почек и снижение продукции эритропоэтина
- Повышение уровня провоспалительных цитокинов, угнетающих эритропоэз
- Дефицит железа вследствие мальабсорбции и нарушения всасывания
- Гемодилюция из-за задержки жидкости
- Прием некоторых лекарственных препаратов (ингибиторы АПФ, антикоагулянты)
Анемия ухудшает течение ХСН, снижает толерантность к физическим нагрузкам и качество жизни пациентов. Поэтому своевременная диагностика и коррекция анемии крайне важны для оптимального ведения пациентов с ХСН.

Диагностика железодефицитной анемии при ХСН
Для диагностики железодефицитной анемии (ЖДА) у пациентов с ХСН рекомендуется определять следующие лабораторные показатели:
- Гемоглобин
- Ферритин сыворотки
- Сатурация трансферрина
Согласно современным рекомендациям, диагноз ЖДА у пациентов с ХСН устанавливается при следующих значениях:
- Уровень ферритина <100 мкг/л
- Или уровень ферритина 100-299 мкг/л при сатурации трансферрина <20%
Важно отметить, что ферритин является белком острой фазы и может повышаться при воспалении, поэтому его изолированное определение недостаточно информативно. Более значимым показателем считается сатурация трансферрина.
Особенности лечения ЖДА у пациентов с ХСН
Основные принципы лечения ЖДА у пациентов с ХСН включают:
- Выявление и устранение причины кровопотери
- Назначение препаратов железа (пероральных или парентеральных)
- Длительную терапию до нормализации запасов железа
- Использование гемотрансфузий только по жизненным показаниям
Целью лечения является достижение уровня гемоглобина ≥120 г/л. Выбор между пероральными и парентеральными препаратами железа зависит от тяжести анемии, переносимости и сопутствующих заболеваний.

Пероральные препараты железа
Пероральные препараты железа могут быть препаратами первой линии при легкой и среднетяжелой ЖДА у пациентов с ХСН. Их преимуществами являются:
- Доступность
- Низкая стоимость
- Удобство применения
Наиболее часто используются препараты двухвалентного (Fe2+) и трехвалентного (Fe3+) железа. Препараты Fe2+ (сульфат, фумарат) обеспечивают более быстрое повышение уровня гемоглобина, но чаще вызывают побочные эффекты со стороны ЖКТ. Препараты Fe3+ (гидроксид полимальтозат) лучше переносятся и могут использоваться длительно.
Парентеральные препараты железа
Парентеральное введение препаратов железа показано в следующих случаях:
- Тяжелая анемия
- Непереносимость пероральных препаратов
- Нарушение всасывания железа
- Необходимость быстрой коррекции анемии
Наиболее изученным парентеральным препаратом при ХСН является карбоксимальтозат железа. Его эффективность и безопасность подтверждены в ряде клинических исследований (FAIR-HF, CONFIRM-HF, EFFECT-HF).
Особенности ведения пожилых пациентов с ХСН и анемией
Лечение ЖДА у пожилых пациентов с ХСН имеет ряд особенностей:

- Необходим тщательный поиск причины анемии (исключение онкопатологии, кровотечений)
- Предпочтительно использование пероральных препаратов железа с хорошей переносимостью
- Парентеральные препараты железа следует применять с осторожностью из-за риска перегрузки железом
- Важен контроль сопутствующих заболеваний (ХБП, сахарный диабет)
- Необходимо учитывать лекарственные взаимодействия при полипрагмазии
Целевой уровень гемоглобина у пожилых пациентов с ХСН не должен превышать 120 г/л, так как более высокие значения могут ассоциироваться с повышенным риском тромбоэмболических осложнений.
Заключение
Своевременная диагностика и коррекция железодефицитной анемии у пациентов с хронической сердечной недостаточностью позволяет улучшить их функциональный статус, качество жизни и прогноз. Выбор метода лечения должен быть индивидуальным с учетом тяжести анемии, сопутствующих заболеваний и возраста пациента. Необходимы дальнейшие исследования для уточнения оптимальных подходов к терапии ЖДА при ХСН, особенно у пациентов пожилого возраста.
Анемия и хроническая сердечная недостаточность ,
Большинство проблем, связанных с диагностикой, лечением и реабилитацией пожилых больных хронической сердечной недостаточностью (ХСН), по-прежнему приходится решать врачу-терапевту и врачу общей практики. ХСН на сегодняшний день вполне возможно рассматривать как заболевание пожилого возраста, поскольку в течение последних двух десятилетий существенно изменился «фенотип» больных ХСН: увеличилось число больных старшего возраста, число больных с сохраненной и промежуточной фракцией выброса левого желудочка (ФВЛЖ), количество сопутствующих заболеваний и принимаемых лекарственных препаратов.
Сопутствующие заболевания могут взаимно провоцировать прогрессирование друг друга, включая декомпенсацию сердечной деятельности, приводя к госпитализациям или летальному исходу. Среди сопутствующих заболеваний особый интерес представляют анемия и железодефицитное состояние (дефицит железа).
Анемия — это патологическое состояние, которое характеризуется абсолютным снижением концентрации гемоглобина и количества эритроцитов в единице объема крови за счет их уменьшения в организме.
Дефицит железа (сидеропения, гипосидероз) — это состояние здоровья, при котором доступное количество железа в организме недостаточно для удовлетворения его потребностей, и может наблюдаться как на фоне анемии, так и без нее [3].
Железодефицитная анемия (ЖДА) представляет собой клинико-гематологический синдром, возникающий при развитии дефицита железа вследствие патологических (или физиологических) процессов, и характеризуется снижением концентрации гемоглобина в сочетании с клиническими признаками сидеропении:
Анемия выявляется приблизительно у 30% амбулаторных пациентов со стабильным течением ХСН и у 50% пациентов, получающих лечение в госпитальных условиях, независимо от характера ФВЛЖ.
Результаты крупного исследования RED-HF trial (Reduction of Events With Darbepoetin Alfa in Heart Failure) показали, что сама по себе анемия, возможно, не является предиктором летального исхода у больных ХСН, но выступает маркером тяжелого течения сердечной недостаточности [6]. Анемия даже легкого течения при ХСН ассоциируется с ухудшением клинического состояния, снижением функциональной активности, адаптивными гемодинамическими изменениями, усугубляющими процессы ремоделирования левого желудочка (ЛЖ), почечной дисфункцией и госпитализациями [7, 8].
При выявлении у пациента пожилого возраста с ХСН анемии перед врачом, особенно в первичном звене, встает ряд вопросов:
Какова причина анемии?
Каков минимум диагностических мероприятий, требуемых для выявления характера анемии?
Как правильно назначить лечение?
Согласно общепринятой точке зрения анемия у пожилых больных не связана с возрастными изменениями кроветворной системы, а является в большинстве случаев проявлением сопутствующих заболеваний, которые чаще встречаются в более старшем возрасте (ХБП, неопластические процессы, нарушение питания, в основном за счет снижения употребления продуктов, содержащих железо), а другие могут быть не связаны с инволютивными изменениями (эрозивно-язвенные поражения желудочно-кишечного тракта (ЖКТ), прием аспирина, антикоагулянтов, хронические воспалительные заболевания, сердечная кахексия, обусловленная компенсаторной гиподинамией и неполноценным питанием, уменьшение всасывания железа в ЖКТ из-за застоя слизистой и др.
Патогенетические основы коморбидности
Практически у каждого 3-го пациента пожилого возраста анемия развивается без очевидной причины (гипопролиферативная анемия на фоне низкой активности эритропоэтина) [4].
Регуляция эритропоэза является сложным и комплексным процессом c участием разных представителей цитокинов. Для окончательной дифференцировки эритроидных клеток необходим эритропоэтин — гликопротеид, первичный медиатор нормальной физиологической реакции на гипоксию, стимулирующий митоз и являющийся гормоном дифференцировки, который способствует образованию эритроцитов из стволовых клеток. Эритропоэтин вырабатывается преимущественно в почках (в основном в перитубулярных интерстициальных фибробластах коры и внешней области мозгового слоя) и в меньшей степени (до 15%) — в печени (гепатоцитами и фибробластоподобными клетками печени — Ito-клетками).
ХСН способствует гипоперфузии почек, перераспределению кровотока в них, вазоконстрикции, что приводит к нарушению функции почек практически у каждого 2-го пациента пожилого возраста [10]. Анемия, развивающаяся у больных с ХСН и патологией почек, определяется дефицитом эндогенной продукции эритропоэтина вследствие необратимого уменьшения количества клубочков почек или их относительной ишемии из-за снижения сердечного выброса. По мере снижения функциональной активности почек структуры, продуцирующие эритропоэтин, замещаются фиброзной тканью и утрачивают гормонпродуцирующие свойства. В результате гипоперфузии почек нарастает ишемия эндотелиоцитов перитубулярных капилляров и фибробластов, локализующихся в тубулоинтерстиции, и уменьшается продукция эритропоэтина. Помимо этого, протеинурия при ХСН усиливает потерю эритропоэтина, трансферрина, ионизированного железа с мочой и может приводить к развитию железодефицитного состояния.
Анемия, развивающаяся у больных с ХСН и патологией почек, определяется дефицитом эндогенной продукции эритропоэтина вследствие необратимого уменьшения количества клубочков почек или их относительной ишемии из-за снижения сердечного выброса. По мере снижения функциональной активности почек структуры, продуцирующие эритропоэтин, замещаются фиброзной тканью и утрачивают гормонпродуцирующие свойства. В результате гипоперфузии почек нарастает ишемия эндотелиоцитов перитубулярных капилляров и фибробластов, локализующихся в тубулоинтерстиции, и уменьшается продукция эритропоэтина. Помимо этого, протеинурия при ХСН усиливает потерю эритропоэтина, трансферрина, ионизированного железа с мочой и может приводить к развитию железодефицитного состояния.
Подавление костномозговой функции с формированием анемии при ХСН может реализоваться и через воспалительные реакции, т. к. при данном заболевании увеличивается уровень и активность провоспалительных цитокинов, в частности ФНО-α и ИЛ-6. Повышение цитокинов ассоциируется с угнетением пролиферации и дифференцировки эритроидных клеток-предшественников, с неадекватной гипоксией, выработкой эндогенного эритропоэтина и повышением синтеза гепсидина. Последний высвобождается в печени в ответ на воспаление и подавляет абсорбцию железа в тонком кишечнике и выход железа из ретикулоэндотелиальной макрофагальной системы вследствие снижения активности ферропортина, что приводит к неэффективному эритропоэзу.
Последний высвобождается в печени в ответ на воспаление и подавляет абсорбцию железа в тонком кишечнике и выход железа из ретикулоэндотелиальной макрофагальной системы вследствие снижения активности ферропортина, что приводит к неэффективному эритропоэзу.
Показано, что низкий уровень гепсидина, наряду с нормальными значениями показателей воспалительного ответа и отсутствием связи между ними, а также отсутствием корреляции между уровнем гепсидина и концентрацией гемоглобина, свидетельствует о том, что гепсидин не играет роли в развитии анемии у больных старшего возраста с ХСН и ЖДА. И наоборот, высокие уровни гепсидина, показателей воспаления, положительные корреляции между ними и отрицательная корреляция между уровнем гепсидина и концентрацией гемоглобина указывают на воспаление как причину повышения уровня гепсидина, который обусловливает развитие анемии при ХСН в пожилом и старческом возрасте [11].
Возможной причиной развития анемии при ХСН является применение ингибиторов ренин-ангиотензин-альдостероновой системы, в частности иАПФ и АРА, особенно в высоких дозах, что замедляет выработку эритропоэтина в почках и снижает его активность в костном мозге. К примеру, обсуждается роль ингибитора гематопоэза N-ацетил-серил-аспартил-лизил-пролина (AсSDKP), который разрушается под действием АПФ, роль уменьшения циркулирующего ангиотензина II — митогенного фактора для предшественников эритропоэтина [12, 13].
К примеру, обсуждается роль ингибитора гематопоэза N-ацетил-серил-аспартил-лизил-пролина (AсSDKP), который разрушается под действием АПФ, роль уменьшения циркулирующего ангиотензина II — митогенного фактора для предшественников эритропоэтина [12, 13].
Сахарный диабет также играет немаловажную роль в развитии анемии, т. к. в процессе гликозилирования на ранних этапах повреждаются продуцирующие эритропоэтин клетки в почках [14].
У большинства пациентов с ХСН, помимо истинной анемии, может встречаться и гемодилюционная анемия, при которой снижение гемоглобина и гематокрита становится результатом повышенного объема плазмы[15]. Сниженный кровоток в почках и усиленная канальцевая реабсорбция натрия при ХСН способствуют увеличению объема плазмы, который обычно повышен даже при отсутствии застойных явлений. Еще в 2003 г. А. Androne et al. [16] показали неблагоприятный прогноз у пациентов с ХСН и гемодилюцией в отличие от пациентов с истинной анемией, и возможным объяснением этого факта выдвинули перегрузку объемом, приводящую к дилатации ЛЖ, увеличению длины саркомеров и перерастяжению миофибрилл, что в итоге приводит к эксцентрической гипертрофии миокарда — независимого предиктора неблагоприятного исхода. На сегодняшний день существует мнение, что гемодилюция предшествует клиническим проявлениям накопления жидкости и играет немаловажную роль в развитии анемии при ХСН. Помимо этого у пациентов со стабильной ХСН и низкой ФВЛЖ при оптимальной медикаментозной терапии объем плазмы в целом нормальный, но неоднородно распределенный, а встречаемость анемии при ХСН гораздо выше, чем когда ее оценивают только по уровню гемоглобина (поскольку методы измерения внеклеточного объема жидкости не всегда доступны, особенно в рутинной клинической практике) [17].
На сегодняшний день существует мнение, что гемодилюция предшествует клиническим проявлениям накопления жидкости и играет немаловажную роль в развитии анемии при ХСН. Помимо этого у пациентов со стабильной ХСН и низкой ФВЛЖ при оптимальной медикаментозной терапии объем плазмы в целом нормальный, но неоднородно распределенный, а встречаемость анемии при ХСН гораздо выше, чем когда ее оценивают только по уровню гемоглобина (поскольку методы измерения внеклеточного объема жидкости не всегда доступны, особенно в рутинной клинической практике) [17].
При ХСН дефицит железа рассматривается как сопутствующая патология и встречается у 37–61% пациентов [18]. Данные исследования NHANES III свидетельствуют о наличии дефицита железа у 61,3% из 574 взрослых пациентов с ХСН (уровень ферритина менее 100 или 100–199 при уровне трансферрина <20%) [19]. Согласно E. Jankowska et al. дефицит железа имел место у 37% из 546 пациентов с ХСН (включая 32% пациентов без анемии) [20].
Результаты проспективного обсервационного регистра PReP registry (Prävalenz des Eisenmangels bei Patienten mit Herzinsuffizienz) с участием амбулаторных пациентов с ХСН и ФВЛЖ ≤45% из Германии показали встречаемость дефицита железа у 42,5% пациентов (до включения в регистр никто из пациентов не знал о наличии этого состояния у них), анемии — у 18,9% (4,8% пациентов знали о наличии у них анемии). Средний возраст пациентов составил 69,0±10,6 года, среди них было 25,3% женщин, ФВЛЖ отмечена у 35,3±7,2%. Дефицит железа ассоциировался с женским полом, более низкой массой тела и низким уровнем гемоглобина, более высоким функциональным классом (ФК) ХСН и высоким уровнем натрийуретического пептида (при всех показателях p<0,05) [21].
Средний возраст пациентов составил 69,0±10,6 года, среди них было 25,3% женщин, ФВЛЖ отмечена у 35,3±7,2%. Дефицит железа ассоциировался с женским полом, более низкой массой тела и низким уровнем гемоглобина, более высоким функциональным классом (ФК) ХСН и высоким уровнем натрийуретического пептида (при всех показателях p<0,05) [21].
Железо играет центральную роль в поглощении, транспорте, хранении и метаболизме кислорода, эритропоэзе и клеточном иммунном ответе. Регуляция баланса железа, определяемого комбинацией абсорбции алиментарного железа, использования и его выведения, необходима для поддержания основных клеточных функций, особенно в клетках с высокими энергетическими потребностями — скелетных миоцитах и кардиомиоцитах [22, 23]. Дефицит железа может приводить к дисфункции митохондрий, нарушению активности ферментов, активации апоптоза, нарушению синтеза и функции белков. Последствия дефицита железа выражаются в ремоделировании тканей организма, в снижении работоспособности и изменении когнитивно-эмоциональной cферы.
Дефицит железа как на фоне анемии, так и независимо от нее может ухудшать течение самой ХСН и заболеваний, лежащих в ее основе, значительно снижать качество жизни, физическую активность и увеличивать риск летального исхода [24, 25]. К тому же дефицит железа повышает вероятность госпитализаций пациентов с ХСН [26].
- Moliner et al. полагают, что дефицит железа возможно рассматривать не только в качестве одного из сопутствую-щих состояний, но и как ключевой элемент в патофизиологической последовательности изменений, способствующий развитию и прогрессированию ХСН [28].
Дефицит железа может быть абсолютным, когда общее количество железа в организме снижается, или функциональным, когда общее количество железа в организме нормальное или повышенное, но достаточное количество железа не поступает из депо (происходит неравномерное распределение железа). При абсолютном дефиците железа снижаются и общие запасы железа, и запасы функционального железа, тогда как при функциональном дефиците железа снижается лишь пул функционального железа. Оба состояния могут возникать независимо друг от друга или сосуществовать у отдельного пациента.
Оба состояния могут возникать независимо друг от друга или сосуществовать у отдельного пациента.
Абсолютный дефицит железа при сердечной недостаточности может быть вызван снижением потребления железа из-за анорексии, кахексии, нарушенного всасывания железа в результате отека слизистой кишечника, а также индуцированным гепсидином подавлением активности переносчиков железа (например, ферропортина). Другие причины абсолютного дефицита железа включают желудочно-кишечные кровотечения, связанные с использованием аспирина, антиагрегантов или антикоагулянтов или вызванные сопутствующими заболеваниями, такими как злокачественные новообразования ЖКТ или мочеполовой системы.
Функциональный дефицит железа при ХСН вызван механизмами, аналогичными тем, которые ответственны за анемию хронического заболевания или воспаления, обусловленных повышением уровня воспалительных цитокинов, включая ИЛ-1, ИЛ-6, ИЛ-18 и ФНО-α, которые, в свою очередь (особенно ИЛ-6), повышают уровень гепсидина в печени. Пролиферация эритробластов напрямую ингибируется повышенными уровнями гепсидина, что еще более ухудшает синтез гемоглобина (рис. 2) [9].
Пролиферация эритробластов напрямую ингибируется повышенными уровнями гепсидина, что еще более ухудшает синтез гемоглобина (рис. 2) [9].
Принципы дифференциальной диагностики
Ранними проявлениями ХСН в пожилом возрасте могут быть утомляемость, слабость, тяжесть в ногах, часто проявляющиеся во время повседневной физической нагрузки и не всегда ассоциирующиеся с выраженностью одышки и отечного синдрома. Пациенты могут жаловаться на головокружение, пресинкопальные и синкопальные состояния, раздражительность, нарушение сна. Как правило, эти симптомы малоспецифичны, поскольку могут присутствовать и при других заболеваниях, в частности при анемии. Клиническая картина анемического синдрома включает в себя 3 субъективных симптома: усталость, одышку и сердцебиение. При осмотре пациента с ХСН следует обращать внимание не только на эти симптомы, являющиеся неотъемлемой частью клинической картины сердечной недостаточности, но и помнить об анемическом синдроме и не игнорировать роль гемодилюции, особенно у лиц пожилого возраста.
Затруднения в дифференциальной диагностике ХСН возникают, как правило, вследствие мультиморбидности. У пожилых больных с анемией также нередко приходится исключать или подтверждать наличие ХСН. Диагностическими критериями в этом случае является совокупность анамнестических данных (в частности, ишемическая болезнь сердца, инфаркт миокарда), клинических симптомов и признаков (смещение верхушечного толчка влево, повышенная ЧСС), данных объективных методов исследования. С учетом атипичности клинических проявлений и малосимптомности заболевания в пожилом возрасте большое значение приобретает контроль уровня натрийуретического пептида.
При постановке диагноза ЖДА решающее значение имеют данные комплекса лабораторных исследований — подтверждение факта анемии и дефицита железа. Анализ крови характеризуется наличием признаков гипохромной микроцитарной анемии со снижением концентрации гемоглобина и цветового показателя. Гипохромия — уменьшение средней концентрации Hb в эритроцитах (<24 пг), микроцитоз — уменьшение размеров эритроцитов (<75 нм). В мазках крови преобладают небольшие по размеру гипохромные эритроциты, аннулоциты (эритроциты в виде колец с отсутствием Hb в центре), отмечаются пойкилоцитоз и анизоцитоз. В пользу дефицита железа свидетельствуют уровень сывороточного железа <12,5 мкмоль/л, ферритина сыворотки <30 мкг/л, сатурация трансферрина <17%) [29].
В мазках крови преобладают небольшие по размеру гипохромные эритроциты, аннулоциты (эритроциты в виде колец с отсутствием Hb в центре), отмечаются пойкилоцитоз и анизоцитоз. В пользу дефицита железа свидетельствуют уровень сывороточного железа <12,5 мкмоль/л, ферритина сыворотки <30 мкг/л, сатурация трансферрина <17%) [29].
При анемии, развившейся на фоне кровопотери, непосредственно после кровотечения отмечается повышение количества ретикулоцитов. Количество лейкоцитов имеет тенденцию к снижению, но лейкоцитарная формула не меняется. Количество тромбоцитов обычно нормальное, с тенденцией к увеличению при кровотечении. Наблюдается снижение уровня сывороточного железа и повышение общей железосвязывающей способности плазмы крови. Около 33% всего количества трансферрина сыворотки связано с железом (показатель насыщения трансферрина железом). Остальное количество трансферрина остается свободным и характеризует скрытую железосвязывающую способность сыворотки крови. При дефиците железа снижается уровень трансферрина до 10–20 мг/л, но при этом увеличивается скрытая железосвязывающая способность плазмы.
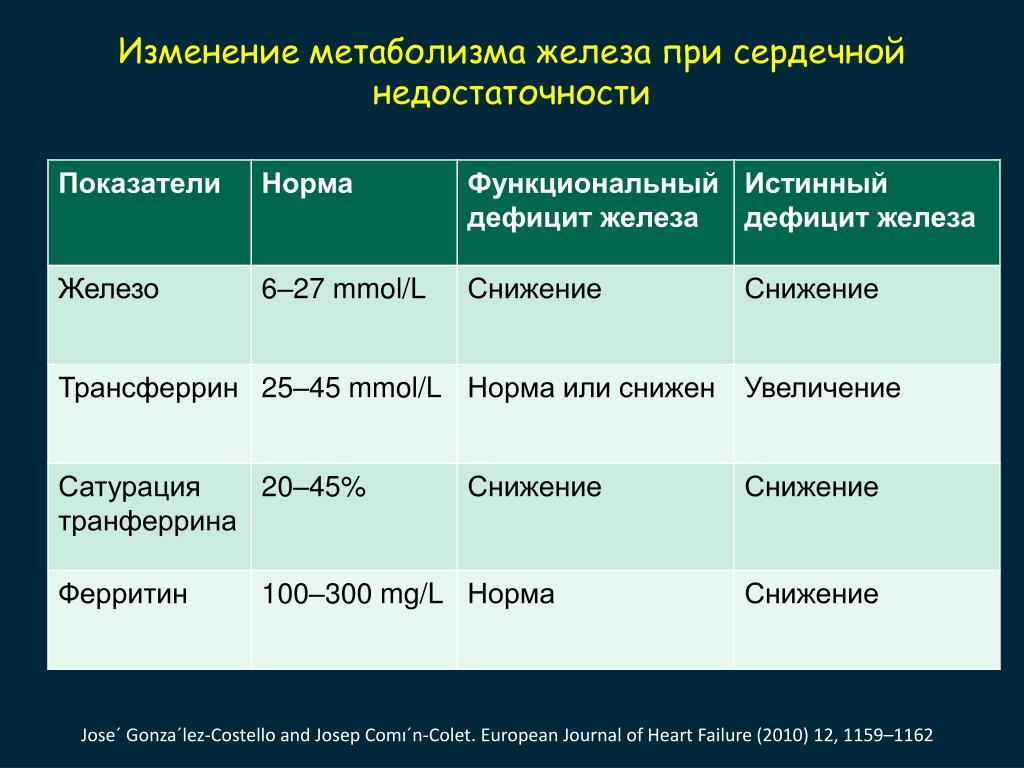
На сегодняшний день эксперты рекомендуют проводить скрининг дефицита железа у всех пациентов, независимо от уровня гемоглобина, с впервые поставленным диагнозом ХСН (класс рекомендаций I, уровень доказанности С), а также при наличии уже существующей ХСН с клиническими проявлениями. Лабораторные параметры обмена железа рекомендовано определять хотя бы однократно в год (табл. 3) [1, 29].
Таким образом, дефицит железа у пациентов с ХСН диагностируется при снижении уровня ферритина <100 мкг/л или при уровне ферритина 100–299 мкг/л при условии, что сатурация трансферрина <20%.
Следует отметить, что ферритин не обладает диагностической ценностью, поскольку достаточно изменчив, является белком острой фазы, а его увеличение, которое наблюдается при ХСН и других воспалительных заболеваниях, не всегда отражает высокие уровни запаса железа, что следует принимать во внимание. К тому же показано, что именно низкий уровень сатурации трансферрина, а не ферритина ассоциируется с высоким риском летальности [30]. Кроме этого, у пациентов с уровнем сатурации трансферрина 20,1% не наблюдалось улучшения выживаемости при приеме железосодержащих препаратов [31].
Кроме этого, у пациентов с уровнем сатурации трансферрина 20,1% не наблюдалось улучшения выживаемости при приеме железосодержащих препаратов [31].
Насыщение трансферрина железом является биологическим маркером доставки железа клеткам. Трансферрин — это специфический транспортный белок плазмы
крови, который обеспечивает доставку железа к клеткам через рецепторы трансферрина. Поскольку концентрация трансферрина зависит от многих факторов, в практике его в изолированном виде не используют для определения дефицита железа в организме. Степень насыщения трансферрина железом (СНТЖ) рассчитывается методом деления сывороточной концентрации железа на сывороточную концентрацию трансферрина и отражает то количество железа, которое доступно для эритробластов и других клеток, нуждающихся в нем. СНТЖ не зависит от степени воспаления в организме, а его уровень менее 20% свидетельствует о недостаточном эритропоэзе [32].
Авторы последних исследований полагают, что лечение ЖДА само по себе может быть благоприятно, но сохраняется ряд пробелов в вопросах понимания, когда, как и насколько длительно необходимо лечить текущую анемию или железодефицитное состояние при ХСН, а также понимания механизмов, лежащих в основе лечебных эффектов.
Основные принципы лечения ЖДА, в т. ч. у лиц пожилого возраста с ХСН
Установить причину кровопотери и провести лечение основного заболевания.
Нельзя только одной диетой вылечить ЖДА!
Возместить дефицит железа без железосодержащих лекарственных средств невозможно!
Терапию препаратами железа необходимо проводить длительно.
Терапия ЖДА не должна прекращаться после нормализации уровня гемоглобина и количества эритроцитов.
Гемотрансфузии при ЖДА должны проводиться строго по жизненным показаниям.
Парентеральное назначение препаратов показано только при определенных обстоятельствах.
Целью лечения ЖДА при ХСН является достижение уровня Hb ≥120 г/л за счет перорального или парентерального введения необходимого количества железа.
Терапевтические возможности в отношении улучшения функциональной способности человека очень ограничены, и целевое выявление нарушений, препятствующих транспортировке кислорода и/или его использованию, может достичь функциональных преимуществ. Эти гипотезы были подтверждены во всех 5 рандомизированных контролируемых исследованиях по изучению парентерального введения железа с участием пациентов с ХСН.
Эти гипотезы были подтверждены во всех 5 рандомизированных контролируемых исследованиях по изучению парентерального введения железа с участием пациентов с ХСН.
К примеру, исследование FAIR-HF (The Ferinject Assessment in Patients with Iron Deficiency and Chronic Heart Failure) продемонстрировало улучшение самочувствия, функциональной и физической работоспособности пациентов с ХСН и дефицитом железа (средний возраст 67 лет, ФВЛЖ <40%) при применении карбоксимальтозата железа [33]. Результаты многоцентрового, двойного слепого плацебо-контролируемого рандомизированного исследования CONFIRM-HF (Ferric CarboxymaltOse evaluatioN on perFormance in patients with IRon deficiency in coMbination with chronic Heart Failure) с участием 304 амбулаторных пациентов с клинически выраженной ХСН, ФВЛЖ ≤45%, повышенным уровнем НУП и дефицитом железа (ферритин <100 нг/мл или 100–300 нг/мл при уровне сатурации трансферрина <20%) также подтвердили положительное действие парентерального введения железа на функциональный статус, выраженность клинических симптомов и качество жизни пациентов [34]. Рандомизированное контролируемое исследование EFFECT-HF (Effect of Ferric Carboxymaltose on Exercise Capacity in Patients With Iron Deficiency and Chronic Heart Failure) с участием 172 пациентов с ХСН и железодефицитом показало увеличение VO2 max у пациентов, которым парентерально вводился препарат железа, по сравнению с группой контроля [35].
Рандомизированное контролируемое исследование EFFECT-HF (Effect of Ferric Carboxymaltose on Exercise Capacity in Patients With Iron Deficiency and Chronic Heart Failure) с участием 172 пациентов с ХСН и железодефицитом показало увеличение VO2 max у пациентов, которым парентерально вводился препарат железа, по сравнению с группой контроля [35].
Результаты исследования FAIR-HF2 (Intravenous Iron in Patients With Systolic Heart Failure and Iron Deficiency to Improve Morbidity & Mortality) с участием пациентов с систолической дисфункцией ЛЖ и дефицитом железа ожидаются в 2020 г. [36].
Благоприятный эффект препаратов железа, оказываемый на пациентов с ХСН, подтвержден и в метаанализе, проведенном в 2018 г. S. Anker et al., согласно которому парентеральное введение железа способствовало снижению частоты повторных госпитализаций в связи с декомпенсацией ХСН (ОШ 0,53; 95% ДИ 0,33–0,86; р=0,011) и повторных госпитализаций по сердечно-сосудистым причинам (ОШ 0,60; 95% ДИ 0,41–0,88; р=0,009) [31].
Вышепредставленные данные позволяют рассматривать терапию железосодержащими препаратами как полезное дополнение к общепринятому медикаментозному лечению пациентов с ХСН.
Имеющаяся на сегодняшний день доказательная база по лечению пациентов пожилого и старческого возраста с ХСН и анемией не позволяет однозначно рассматривать вышепредставленные подходы как целесообразные и безопасные. К тому же нет данных об эффективности и безопасности терапии препаратами железа у пациентов с ХСН с сохраненной и промежуточной ФВЛЖ, большинство из которых и являются лицами старшего возраста.
В связи с этим эксперты Общества специалистов по сердечной недостаточности акцентируют внимание на необходимости выявления и коррекции причин, приводящих к развитию железодефицита у пациентов с ХСН (алиментарные нарушения, желудочно-кишечные кровотечения, прием нежелательных лекарственных препаратов и др.).
Пероральные железосодержащие средства могут быть препаратами выбора при ЖДА в комплексном лечении пациентов c ХСН вследствие их достаточно высокой эффективности и низкой стоимости. Лекарственные препараты железа могут быть в виде ионизированного (Fe2+) в составе органических или неорганических солей (фумарат, лактат, сульфат, хлорид) и неионного — в составе комплексов, содержащих окисное железо (Fe3+), — протеин-сукцинилат, полимальтозат или сахарозный комплекс. Препараты ионизированного железа используются только перорально, препараты комплексов окисного железа — парентерально.
Лекарственные препараты железа могут быть в виде ионизированного (Fe2+) в составе органических или неорганических солей (фумарат, лактат, сульфат, хлорид) и неионного — в составе комплексов, содержащих окисное железо (Fe3+), — протеин-сукцинилат, полимальтозат или сахарозный комплекс. Препараты ионизированного железа используются только перорально, препараты комплексов окисного железа — парентерально.
Эффективность лечения пациентов с ЖДА определяется суточной дозой и формой элементарного железа, входящего в состав лекарственного препарата. При этом темп нарастания уровня гемоглобина зависит от выраженности анемического синдрома. Выбор между препаратами железа — Fe2+ или Fe3+ — определяется в первую очередь клинической целью: быстрое достижение эффекта (предпочтение отдается препарату Fe2+) или хорошая переносимость на фоне длительного приема (предпочтение отдается препарату Fe3+).
Железа (III) гидроксид полимальтозат показан для лечения латентного железодефицита и ЖДА. Этот препарат имеет несколько лекарственных форм, в частности форму жевательных таблеток, содержащих 400 мг железополимальтозного комплекса (100 мг элементарного железа), что позволяет пациенту принимать препарат по 1 таблетке 2 р./день с хорошим клиническим эффектом. Данное действие препарата обусловлено, во‑первых, структурой комплекса, которая имеет железо (III) гидроксидное ядро и углеводную оболочку, что напоминает белок запаса железа — ферритин, и, во‑вторых, контролируемой диссоциацией ионов железа из этого лекарственного комплекса. Помимо вышесказанного, полимальтозная оболочка обеспечивает стабильность и растворимость комплекса в достаточно широком диапазоне pH, что и определяет его терапевтическую эффективность и хорошую переносимость с последующим улучшением клинического состояния и качества жизни, что важно в старшем возрасте, особенно при невозможности устранения основной причины заболевания.
Этот препарат имеет несколько лекарственных форм, в частности форму жевательных таблеток, содержащих 400 мг железополимальтозного комплекса (100 мг элементарного железа), что позволяет пациенту принимать препарат по 1 таблетке 2 р./день с хорошим клиническим эффектом. Данное действие препарата обусловлено, во‑первых, структурой комплекса, которая имеет железо (III) гидроксидное ядро и углеводную оболочку, что напоминает белок запаса железа — ферритин, и, во‑вторых, контролируемой диссоциацией ионов железа из этого лекарственного комплекса. Помимо вышесказанного, полимальтозная оболочка обеспечивает стабильность и растворимость комплекса в достаточно широком диапазоне pH, что и определяет его терапевтическую эффективность и хорошую переносимость с последующим улучшением клинического состояния и качества жизни, что важно в старшем возрасте, особенно при невозможности устранения основной причины заболевания.
Адекватный ответ на терапию железосодержащими препаратами включает [37, 38]:
увеличение количества ретикулоцитов через 7 дней;
увеличение уровня гемоглобина на ≈2 г/дл через 1–2 нед. после начала приема препаратов железа;
после начала приема препаратов железа;
нормализацию содержания гемоглобина через 6–8 нед.
Следует обращать внимание на динамику эритроцитарных индексов, нормализация которых отражает адекватность терапии: средний объем эритроцита, среднее содержание гемоглобина в эритроците, среднюю концентрацию гемоглобина в эритроците. Анализы периферической крови проводят 1 раз в 1–2 нед. в начале лечения, а затем 1 раз в 2–4 нед.
Поскольку не вполне корректно расценивать любое снижение гемоглобина ниже нормы у больных ХСН как анемию, то у большинства больных ХСН, помимо истинной анемии, может быть диагностирована и гемодилюция [39, 40], лечение которой должно фокусироваться на коррекции дозы диуретиков. Очевидно, что стратегия лечения возрастной категории пациентов, помимо патогенетической терапии анемии, предусматривает воздействие на нейрогуморальную активацию — применение ингибиторов АПФ и блокаторов рецепторов к ангиотензину II, антагонистов минералокортикоидных рецепторов, бета-адреноблокаторов, а также петлевых диуретиков. Поскольку в развитии отечного синдрома задействованы сложные нейрогуморальные механизмы, бездумная дегидратация вызывает побочные эффекты и рикошетную задержку жидкости, что может приводить к необоснованной терапии.
Поскольку в развитии отечного синдрома задействованы сложные нейрогуморальные механизмы, бездумная дегидратация вызывает побочные эффекты и рикошетную задержку жидкости, что может приводить к необоснованной терапии.
Блокирование гепсидина может быть эффективной терапевтической стратегией, особенно в отношении функционального железодефицита. Как перспективные меры могут рассматриваться прямая блокада экспрессии гепсидина с помощью анти-гепсидин-1-олигорибонуклеотида (lexaptepid), подавление активности гепсидина с помощью препаратов человеческих антител к гепсидину, блокирование передачи сигнала с гепсидина с помощью низкомолекулярного ингибитора (LDN-193189) или неантикоагулянтные гепарины. Спиронолактон, обычно используемый в качестве основного лекарственного средства у пациентов с сердечной недостаточностью, подавляет экспрессию гепсидина у мышей [41, 42].
Заключение
Таким образом, анемия и дефицит железа являются часто встречающимися сопутствующими ХСН состояниями у лиц пожилого возраста. Дефицит железа как на фоне анемии, так и независимо от анемии может ухудшать течение ХСН и заболеваний, лежащих в основе ее развития, снижать качество жизни, физическую активность пациентов и увеличивать риск неблагоприятных событий. Принципиально важным является скрининг дефицита железа у всех пациентов с ХСН, особенно при впервые возникшей, а при постановке диагноза ЖДА решающее значение имеют данные лабораторных исследований — подтверждение факта анемии и дефицита железа. На сегодняшний день однозначных рекомендаций по лечению пациентов пожилого и старческого возраста с ХСН и анемией не существует. В связи с этим необходимо выявлять и корректировать причины дефицита железа у пациентов с ХСН, воздействовать на нейрогуморальную активацию и разумно подходить к лечению отечного синдрома. Требуется тесное сотрудничество нефрологов, кардиологов, терапевтов для эффективной коррекции терапии ХСН и анемии в соответствии с современными достижениями и требованиями. Только в условиях активного регулярного врачебного наблюдения возможно улучшить качество и увеличить продолжительность жизни больным ХСН.
Дефицит железа как на фоне анемии, так и независимо от анемии может ухудшать течение ХСН и заболеваний, лежащих в основе ее развития, снижать качество жизни, физическую активность пациентов и увеличивать риск неблагоприятных событий. Принципиально важным является скрининг дефицита железа у всех пациентов с ХСН, особенно при впервые возникшей, а при постановке диагноза ЖДА решающее значение имеют данные лабораторных исследований — подтверждение факта анемии и дефицита железа. На сегодняшний день однозначных рекомендаций по лечению пациентов пожилого и старческого возраста с ХСН и анемией не существует. В связи с этим необходимо выявлять и корректировать причины дефицита железа у пациентов с ХСН, воздействовать на нейрогуморальную активацию и разумно подходить к лечению отечного синдрома. Требуется тесное сотрудничество нефрологов, кардиологов, терапевтов для эффективной коррекции терапии ХСН и анемии в соответствии с современными достижениями и требованиями. Только в условиях активного регулярного врачебного наблюдения возможно улучшить качество и увеличить продолжительность жизни больным ХСН.
112Препараты железа.
1.Соединения железа:
-гидроксидполимальтозат
-глюканат железа
-сульфат железа
-фумарат железа
-хлорид железа
2. Монокомпонентные препараты:
— мальтофер
-феррорнал
-гемоферпролангатум
-актиферрин
-тардиферон
-хеферол
-гемофер
3.Комбинированные препараты, содержащие аскорбиновую кислоту:
-сорбифер
-дурулес
-ферроплекс
4.Комбинированные препараты, содержащие фолиевую кислоту:
-мальтофер
-фол
-гино-Тардиферон
-ферретаб
Железо – компонент
гемоглобина, миоглобина и различных
ферментов. Общее содержание железа в
организме составляет около 50 мг/кг у
мужчин и 35 мг/кг у женщин. Примерно 60%
железа участвует в переносе кислорода
Суточная
потребность в железе составляет 12-20
мг/кг/сут у мужчин и 8-15 мг/кг/сут у женщин.
Однако в ЖКТ всасывается не более 10%
железа. Пища препятствует всасыванию
препаратов железа, хотя и улучшает их
переносимость. Для приема внутрь используют различные
соли железа: Для
улучшения клинического эффекта и
всасывания ионов железа некоторые
препараты содержат фолиевую
кислоту ( Актиферрин, Гино-тардиферон ,
Мальтофер-фри, Фефол-вит),
цианкобаламин (Аддитива с
железом, Актиферрин , Фенюльс , Ферро-фольгамма ),
аскорбиновую кислоту (Сорбифер
дурулес, Тардиферон , Ферроплекс ).
Применение аскорбиновой кислоты
позволяет использовать меньшую дозу
железа и уменьшить выраженность побочных
действий. При
невозможности обеспечить поступление
железа через ЖКТ назначаются препараты
железа для парентерального введения.
Парентеральное введение показано также
больным, получающим препараты
эритропоэтина, чтобы обеспечить организм
достаточным количеством железа и тем
самым поддержать пролиферацию клеток
эритроидного ростка. Обычно
используют комплекс декстран-железо
(Спейсферрон) — препарат, содержащий
комплексное соединение декстрана с
гидроксидом железа (III). При в/в введении
комплекса декстран-железо возможны
анафилактоидные реакции.
Для приема внутрь используют различные
соли железа: Для
улучшения клинического эффекта и
всасывания ионов железа некоторые
препараты содержат фолиевую
кислоту ( Актиферрин, Гино-тардиферон ,
Мальтофер-фри, Фефол-вит),
цианкобаламин (Аддитива с
железом, Актиферрин , Фенюльс , Ферро-фольгамма ),
аскорбиновую кислоту (Сорбифер
дурулес, Тардиферон , Ферроплекс ).
Применение аскорбиновой кислоты
позволяет использовать меньшую дозу
железа и уменьшить выраженность побочных
действий. При
невозможности обеспечить поступление
железа через ЖКТ назначаются препараты
железа для парентерального введения.
Парентеральное введение показано также
больным, получающим препараты
эритропоэтина, чтобы обеспечить организм
достаточным количеством железа и тем
самым поддержать пролиферацию клеток
эритроидного ростка. Обычно
используют комплекс декстран-железо
(Спейсферрон) — препарат, содержащий
комплексное соединение декстрана с
гидроксидом железа (III). При в/в введении
комплекса декстран-железо возможны
анафилактоидные реакции. Любая реакция
на комплекс декстран-железо в анамнезе,
как немедленная, так и отсроченная
(слабость, лихорадка, артралгия, сыпь
или увеличение лимфоузлов), служит
противопоказанием к введению этого
препарата. Препараты
железа для приема внутрь
Любая реакция
на комплекс декстран-железо в анамнезе,
как немедленная, так и отсроченная
(слабость, лихорадка, артралгия, сыпь
или увеличение лимфоузлов), служит
противопоказанием к введению этого
препарата. Препараты
железа для приема внутрь
Твердые лекарственные формы, содержащие железа (II) сульфат
Твердые лекарственные формы, содержащие железа (II) фумарат
Твердые лекарственные формы, содержащие железа (II) глюконат
Препараты железа для парентерального введения.
Для внутривенного введения
Венофер (полинуклеарный комплекс гидроксида железа с сахарозой) Спейсферрон (декстран железа) Феррлецит (натрий-железоглюконатный комплекс)
Для внутримышечного введения
Мальтофер (полиизомальтозат железа)
Для внутривенного и внутримышечного введения
Феррум лек : полиизомальтозат железа – для в/в введения; сахарат железа – для в/м введения
Показания.
Железодефицитная анемия. Для восстановления запасов железа в макрофагах, взрослому, не страдающему другими хроническими заболеваниями, следует принимать препараты железа как минимум в течение 6 мес. Уже через 3-4 сут после начала лечения повышается содержание ретикулоцитов. Если ретикулоцитоз отсутствует, причина может заключаться в нерегулярном приеме препарата; нарушении всасывания железа; продолжающейся кровопотере, превосходящей всасывание железа; ошибочном диагнозе или сопутствующих заболеваниях. При парентеральном введении препаратов железа пациентам с железодефицитной анемией вся доза, необходимая для устранения дефицита железа, вводится однократно, в/в, с учетом веса пациента и уровня гемоглобина в крови. Повышенная потребность в железе. Это состояние наблюдается, например, при лечении эритропоэтинами.
Противопоказания.
Гиперчувствительность,
анемия, не связанная с дефицитом железа
(гемолитическая, мегалобластная),
нарушение эритропоэза и гипоплазия
костного мозга, избыток железа в организме
(гемохроматоз, гемосидероз), нарушение
утилизации железа (сидероахрестическая
анемия, талассемия, свинцовая интоксикация,
поздняя порфирия кожи). Не
следует применять препараты железа
пациентам с нормальным балансом железа.
Не
следует применять препараты железа
пациентам с нормальным балансом железа.
Побочные действия.
При приеме внутрь часто наблюдаются: анорексия, тошнота, рвота, запор или диарея, почернение стула. При парентеральном введении отмечаются: артериальная гипотензия, боли в суставах, головная боль, головокружение, лимфоаденопатия, диспепсия, анафилактоидная реакция, боль и реакция в месте инъекции, тромбофлебит. Из-за того, что организм человека не способен экскретировать избыток железа, возможно хроническое перенасыщение железом (например, при гемохроматозе, гемолитической анемии и талассемии) с развитием гемосидероза.
Фумарат железа при железодефицитной анемии – Лекарства для детей
Эта брошюра предназначена для родителей и опекунов о том, как использовать это лекарство у детей. Наша информация может отличаться от информации, предоставленной производителями, поскольку их информация обычно относится к взрослым. Внимательно прочитайте эту брошюру. Сохраните его в безопасном месте, чтобы вы могли прочитать его снова.
Сохраните его в безопасном месте, чтобы вы могли прочитать его снова.
Не давайте ребенку фумарат железа, если это не рекомендовано врачом. Если анемия вашего ребенка не связана с дефицитом железа, у него может быть слишком много железа, что может быть опасно.
- Название лекарства
- Почему важно, чтобы мой ребенок принимал фумарат железа?
- В каком виде доступен фумарат железа?
- Когда следует давать фумарат железа
- Сколько я должен дать?
- Как следует давать фумарат железа?
- Когда лекарство должно начать действовать
- Что делать, если мой ребенок болен (рвота)?
- А если я забуду дать?
- Что, если я даю слишком много?
- Возможны ли побочные эффекты?
- Можно ли давать другие лекарства одновременно с фумаратом железа?
- Есть ли что-то еще, что мне нужно знать об этом лекарстве?
- Общие советы по лекарствам
- Где мне хранить это лекарство?
- К кому обратиться за дополнительной информацией?
Название лекарства
Фумарат железа
Торговые марки : Fersaday®, Fersamal®, Galfer®
В этой брошюре рассказывается об использовании фумарата железа, который представляет собой форму железа, для профилактики или лечения железодефицитной анемии.
Почему моему ребенку важно принимать фумарат железа?
Анемия — это заболевание крови, при котором наблюдается недостаток белка, называемого гемоглобином. Гемоглобин необходим для переноса кислорода в крови и транспортировки его по всему телу. Дети с анемией часто бледны, чувствуют усталость, у них мало энергии, они могут не расти или развиваться должным образом.
Фумарат железа — это форма железа, которую можно принимать внутрь. Это помогает организму вырабатывать больше гемоглобина и лечить анемию. Его также можно использовать для профилактики анемии у детей, подверженных ее риску, или, например, перед операцией.
В каком виде доступен фумарат железа?
Таблетки : 210 мг (68 мг железа), 322 мг (100 мг железа)
Капсулы : 305 мг (100 мг железа)
Жидкое лекарство (суспензия) или сироп : 140 мг (45 мг железа) в 5 мл; содержит глюкозу и сахарозу
Когда следует давать фумарат железа
Это зависит от того, используется ли он для профилактики или лечения анемии. Ваш врач скажет вам, как часто следует давать фумарат железа.
Ваш врач скажет вам, как часто следует давать фумарат железа.
Если фумарат железа используется для предотвращения анемии, его обычно назначают один раз каждый день. Это может быть утром ИЛИ вечером.
Если фумарат железа используется для лечения анемии, его обычно назначают два раза по каждый день. Это должно быть один раз утром и один раз вечером. В идеале эти периоды должны быть разделены на 10–12 часов, например, между 7 и 8 часами утра и между 7 и 8 часами вечера.
Давайте лекарство примерно в одно и то же время каждый день, чтобы это стало частью распорядка дня вашего ребенка, что поможет вам запомнить.
Сколько я должен дать?
Ваш врач подберет количество фумарата железа (дозу), подходящее для вашего ребенка. Доза будет указана на этикетке лекарства.
Важно, чтобы вы следовали указаниям своего врача о том, сколько давать.
Как давать фумарат железа?
Таблетки
- Таблетки следует проглатывать, запивая стаканом воды или сока, но не молока.
 Ваш ребенок не должен жевать таблетку. Не раздавливайте таблетки.
Ваш ребенок не должен жевать таблетку. Не раздавливайте таблетки.
Капсулы
- Капсулы следует проглатывать, запивая стаканом воды или сока, но не молока. Ваш ребенок не должен жевать капсулу.
Жидкое лекарство
- Хорошо встряхните лекарство.
- Отмерьте нужное количество с помощью орального шприца или медицинской ложки. Вы можете получить их у своего фармацевта. Не используйте кухонную чайную ложку, так как она не даст нужного количества.
Фумарат железа лучше всего действует, если принимать его натощак. Старайтесь давать его за 30 минут до или через 2 часа после еды. Однако, если это расстраивает желудок вашего ребенка, давайте ему немного еды.
Когда должно начать действовать лекарство?
Фумарат железа требует времени, чтобы подействовать.
Если ваш ребенок принимает его для профилактики анемии, вы не заметите никакой разницы, но если он принимает его для лечения анемии, вы можете заметить улучшение его симптомов через 3–4 недели приема препарата. Ваш ребенок должен будет регулярно принимать фумарат железа в течение как минимум 3 месяцев, чтобы он работал должным образом.
Ваш ребенок должен будет регулярно принимать фумарат железа в течение как минимум 3 месяцев, чтобы он работал должным образом.
Если ваш ребенок принимает фумарат железа для профилактики анемии, вы не заметите никаких изменений в состоянии вашего ребенка, но лекарство по-прежнему будет работать, повышая уровень железа у вашего ребенка и предотвращая развитие анемии.
Что делать, если мой ребенок болен (рвота)?
Если ваш ребенок заболел менее чем через 30 минут после приема дозы фумарата железа, дайте ему ту же дозу еще раз.
Если ваш ребенок заболел более чем через 30 минут после приема дозы фумарата железа, вам не нужно давать ему еще одну дозу. Подождите до следующей нормальной дозы.
Что, если я забуду дать?
Если вы обычно даете его один раз в день : Дайте пропущенную дозу, когда вспомните, но не менее чем за 12 часов до следующей дозы. Вам не нужно будить спящего ребенка, чтобы дать пропущенную дозу.
Если вы обычно даете его два раза в день : Если вы помните до 4 часов после того, как вы должны были дать дозу, дайте ребенку пропущенную дозу. Например, если вы обычно вводите дозу примерно в 7 часов утра, вы можете дать пропущенную дозу в любое время до 11 часов утра. Если вы помните по истечении этого времени, не давайте пропущенную дозу. Просто дайте следующую дозу, как обычно.
Никогда не давайте двойную дозу фумарата железа. Если вы не уверены, следует ли давать пропущенную дозу, не давайте ее. Предоставление дополнительной дозы фумарата железа по ошибке с большей вероятностью причинит вред, чем пропуск дозы.
Что делать, если я даю слишком много?
Дети, получившие слишком много фумарата железа, могут не проявлять никаких симптомов или иметь только легкие симптомы. Если вы считаете, что ваш ребенок принял слишком много фумарата железа, обратитесь к своему врачу или в NHS Direct (111 в Англии и Шотландии; 111 или 0845 4647 в некоторых частях Уэльса) или отвезите ребенка в больницу.
Если у вашего ребенка есть один или несколько из следующих симптомов, возможно, он получил слишком много фумарата железа:
- боли в животе
- повторное недомогание (рвота)
- диарея
- рвотные массы или стул (фекалии) могут быть окрашены кровью, быть зелеными или серыми.
Давать слишком много фумарата железа может быть опасно. Никогда не давайте ребенку больше, чем посоветовал врач.
Если ваш ребенок очень плохо себя чувствует или чувствует сонливость, немедленно вызовите скорую помощь. Возьмите с собой контейнер или упаковку с лекарством, даже если она пуста. Это будет полезно врачу. Имейте при себе лекарство или упаковку, если звоните за консультацией.
Возможны ли побочные эффекты?
Мы используем лекарства, чтобы сделать наших детей лучше, но иногда они имеют другие эффекты, которые нам не нужны (побочные эффекты).
- Ваш ребенок может заболеть или заболеть.
 Может помочь введение фумарата железа после еды.
Может помочь введение фумарата железа после еды. - У вашего ребенка может быть несварение желудка, запор (трудности с опорожнением) или диарея/жидкий стул (понос).
Если эти побочные эффекты являются проблемой или не проходят, обратитесь к своему врачу или фармацевту, так как они могут порекомендовать другой препарат железа или более низкую дозу. Не уменьшайте дозу без предварительного обсуждения этого с врачом.
Иногда могут возникать другие побочные эффекты, не перечисленные выше. Если вы заметили что-то необычное и обеспокоены, обратитесь к врачу.
Можно ли давать другие лекарства одновременно с фумаратом железа?
- Вы можете давать ребенку лекарства, содержащие парацетамол, если только ваш врач не запретил вам это делать.
- Фумарат железа не следует принимать с некоторыми лекарствами, отпускаемыми по рецепту. Расскажите своему врачу и фармацевту о любых других лекарствах, которые принимает ваш ребенок, прежде чем давать ему фумарат железа.

- Если вашему ребенку необходимо принимать какие-либо лекарства от расстройства желудка, не давайте их с фумаратом железа. Дайте два лекарства в разное время дня.
- Прежде чем давать ребенку какие-либо другие лекарства, другие продукты, содержащие железо, а также любые продукты, содержащие цинк или магний, проконсультируйтесь со своим врачом или фармацевтом. Это включает в себя поливитаминные препараты и травяные или дополнительные лекарства.
Что еще мне нужно знать об этом лекарстве?
Храните фумарат железа в недоступном для детей месте.
- На упаковке фумарата железа может быть предупреждение: «Важное предупреждение: содержит железо. Хранить в недоступном для детей месте, так как передозировка может быть фатальной». Однако железо не вредно, если его давать в количествах, рекомендованных врачом. Вы не должны давать ребенку больше, чем это.
- Стул вашего ребенка (кал) может казаться темнее, чем обычно, при приеме фумарата железа.
 Это очень распространено, и вам не нужно об этом беспокоиться. Однако, если вы обеспокоены, ваш фармацевт или врач сможет дать вам дополнительные советы.
Это очень распространено, и вам не нужно об этом беспокоиться. Однако, если вы обеспокоены, ваш фармацевт или врач сможет дать вам дополнительные советы. - Ваш врач проведет анализы крови, чтобы измерить количество железа в крови вашего ребенка и убедиться, что лекарство работает.
- Отдельные брошюры о других препаратах, содержащих железо, для лечения и профилактики анемии доступны на веб-сайте «Лекарства для детей».
Общие рекомендации по лекарствам
- Старайтесь давать лекарства примерно в одно и то же время каждый день, чтобы лучше помнить.
- Если вы не уверены, что лекарство работает, обратитесь к врачу, но тем временем продолжайте давать лекарство как обычно. Не давайте лишние дозы, так как вы можете навредить.
- Давайте это лекарство только ребенку. Никогда не давайте его никому другому, даже если их состояние кажется таким же, так как это может причинить вред.
- Убедитесь, что у вас всегда достаточно лекарств.
 Закажите новый рецепт как минимум за 2 недели до того, как он закончится.
Закажите новый рецепт как минимум за 2 недели до того, как он закончится.
- Убедитесь, что на упаковке лекарств, которые есть у вас дома, не истек срок годности или срок годности, указанный на упаковке. Отдайте старые лекарства своему фармацевту для утилизации.
Если вы считаете, что кто-то другой мог случайно принять лекарство, немедленно обратитесь к врачу.
Где я должен хранить это лекарство?
- Храните лекарство в шкафу, вдали от источников тепла и прямых солнечных лучей.
- Хранить в холодильнике не нужно.
- Убедитесь, что дети не могут увидеть или достать лекарство.
- Храните лекарство в контейнере, в котором оно было получено.
К кому обратиться за дополнительной информацией?
Ваш врач, фармацевт или медсестра могут предоставить вам дополнительную информацию о фумарате железа и о других лекарствах, используемых для профилактики или лечения железодефицитной анемии.
Отказ от ответственности за авторские права
Версия [1]. © NPPG, RCPCH и WellChild, все права защищены. Проверка до июня 2015 г.
Основным источником информации, содержащейся в данной брошюре, является Британский национальный формуляр для детей. Для получения подробной информации о любых других источниках, использованных для данной брошюры, свяжитесь с нами через наш веб-сайт www.medicinesforchildren.org.uk.
Мы уделяем большое внимание тому, чтобы информация в этой брошюре была правильной и актуальной. Однако лекарства могут использоваться по-разному для разных пациентов. Важно, чтобы вы посоветовались со своим врачом или фармацевтом, если вы в чем-то не уверены. Эта брошюра посвящена использованию этих лекарств в Великобритании и может не применяться в других странах. Королевский колледж педиатрии и детского здоровья (RCPCH), Группа неонатальных и детских фармацевтов (NPPG), WellChild, а также участники и редакторы не несут ответственности за точность информации, упущение информации или любые действия, которые могут быть предприняты как после прочтения этой брошюры.
Прием препаратов железа Информация | Гора Синай
Употребление в пищу продуктов, богатых железом, является ключевой частью лечения анемии, вызванной низким уровнем железа. Вам также может понадобиться принимать добавки железа, чтобы восстановить запасы железа в организме.
Информация
О ДОБАВКАХ ЖЕЛЕЗА
Добавки железа можно принимать в виде капсул, таблеток, жевательных таблеток и жидкостей. Наиболее распространенный размер таблетки составляет 325 мг (сульфат железа). Другими распространенными химическими формами являются глюконат железа и фумарат железа.
Попросите вашего поставщика медицинских услуг сообщить вам, сколько таблеток вы должны принимать каждый день и когда вы должны их принимать. Прием большего количества железа, чем необходимо вашему организму, может вызвать серьезные проблемы со здоровьем.
Прием большего количества железа, чем необходимо вашему организму, может вызвать серьезные проблемы со здоровьем.
У большинства людей показатели крови возвращаются к норме через 2 месяца лечения препаратами железа. Вы должны продолжать принимать добавки еще от 6 до 12 месяцев, чтобы создать запасы железа в организме в костном мозге.
СОВЕТЫ ПО ПРИЕМУ ЖЕЛЕЗА
Железо лучше всего усваивается на пустой желудок. Тем не менее, добавки железа могут вызывать у некоторых людей спазмы желудка, тошноту и диарею. Возможно, вам придется принимать железо с небольшим количеством пищи, чтобы избежать этой проблемы.
Молоко, кальций и антациды не следует принимать одновременно с добавками железа. Вы должны подождать не менее 2 часов после употребления этих продуктов, прежде чем принимать добавки железа.
Продукты, которые вы не должны есть одновременно с приемом железа, включают:
- Продукты с высоким содержанием клетчатки, такие как цельнозерновые, сырые овощи и отруби
- Продукты и напитки, содержащие кофеин
Некоторые врачи рекомендуют принимать добавки с витамином С или пить апельсиновый сок вместе с таблетками железа. Это может помочь железу впитаться в ваше тело. Выпивать 8 унций жидкости с железной таблеткой тоже нормально.
Это может помочь железу впитаться в ваше тело. Выпивать 8 унций жидкости с железной таблеткой тоже нормально.
Сообщите своему врачу обо всех лекарствах, которые вы принимаете.
- Таблетки железа могут привести к тому, что другие лекарства, которые вы принимаете, также не подействуют. Некоторые из них включают тетрациклин, пенициллин, ципрофлоксацин и препараты, применяемые при болезни Паркинсона и судорогах.
- Лекарства, снижающие кислотность желудка, ухудшают всасывание железа и могут вызвать дефицит железа. Ваш провайдер может предложить изменить их.
- Подождите не менее 2 часов между дозами этих препаратов и добавок железа.
ПОБОЧНЫЕ ДЕЙСТВИЯ
Запор и диарея очень распространены. Если запор становится проблемой, примите размягчитель стула, такой как докузат натрия (Colace).
Тошнота и рвота могут возникнуть при приеме более высоких доз, но их обычно можно контролировать, принимая железо в меньших количествах. Спросите своего провайдера о переходе на другую форму железа, а не просто о прекращении.
Черный стул является нормальным при приеме таблеток железа. Немедленно обратитесь к своему поставщику медицинских услуг, если:
- Стул выглядит как смолистый, а также черный
- Если в нем есть красные прожилки
- Возникают спазмы, острые боли или болезненность в желудке
Жидкие формы железа могут окрашивать ваш зубы.
- Попробуйте смешать железо с водой или другими жидкостями (например, фруктовым соком или томатным соком) и выпить лекарство через соломинку.
- Железные пятна можно удалить, почистив зубы пищевой содой или перекисью.
Хранить таблетки следует в прохладном месте. (Аптечки в ванной комнате могут быть слишком теплыми и влажными, что может привести к распаду таблеток.)
Храните добавки железа в недоступном для детей месте. Если ваш ребенок проглотил железную таблетку, немедленно обратитесь в токсикологический центр.
Бриттенхэм GM.
