Очистка воды от железа. Методы удаления железа из воды ➣ Первая вода
Ржавая вода? Вы правы — это железо!
Часто бывает так, что из скважины идет прозрачная и чистая вода, однако, немного отстоявшись, она становится мутной и ржавой. Это показатель того, что в жидкости содержится много растворенного железа (Fe2). Исправить ситуацию можно, используя фильтры очистки воды от железа.
Железо — один из самых распространенных природных элементов. Железо присутствует в большинстве вулканических пород, оно также входит в состав пород, цементирующих песчаники. Железо в значительных количествах содержится в различных глинах, а в осадочных карбонатных породах (например, известняк) встречается только в виде незначительных примесей.
Неудивительно, что проблема присутствия в природной воде железа является одной из самых распространенных. C такой водой возникает целый ряд проблем, как быту, так и при коммерческо-промышленных операциях. Уже при концентрациях железа свыше 0,3 мг/л такая вода при бытовом использовании в коттеджах и квартирах вызывает образование ржавых потеков, способна изменить цвет тканей при их стирке и т. п. При больших концентрациях у воды возникает характерный металлический привкус, что отрицательно сказывается на качестве напитков (чай, кофе и т. п.). В некоторых случаях может пострадать даже качество еды, приготовленной на воде с высоким содержанием железа. Все это делает задачу по удалению железа очень актуальной как для питьевого и хозяйственно-бытового применения, так и для промышленного использования.
Уже при концентрациях железа свыше 0,3 мг/л такая вода при бытовом использовании в коттеджах и квартирах вызывает образование ржавых потеков, способна изменить цвет тканей при их стирке и т. п. При больших концентрациях у воды возникает характерный металлический привкус, что отрицательно сказывается на качестве напитков (чай, кофе и т. п.). В некоторых случаях может пострадать даже качество еды, приготовленной на воде с высоким содержанием железа. Все это делает задачу по удалению железа очень актуальной как для питьевого и хозяйственно-бытового применения, так и для промышленного использования.
Железо существует в природе в различных формах (в зависимости от валентности): Fe°, Fe+2, Fe+3, а также в виде различных сложных химических соединений.
1. Элементарное железо (Fe°). Элементарное, или металлическое железо, безусловно, нерастворимо в воде. В присутствии влаги и кислорода воздуха окисляется до трехвалентного, образуя нерастворимый оксид Fe2O3(процесс, известный в быту как «ржавление»).
2. Двухвалентное железо (Fe+2). Почти всегда находится в воде в растворенном состоянии, хотя возможны случаи (при определенных редко встречающихся в природной воде уровнях рН), когда гидроксид железа Fe(OH)2 способен выпадать в осадок.
3. Трехвалентное железо (Fe+3). Гидроксид железа Fe(OH)3 нерастворим в воде (кроме случая очень низкого рН). Хлорид FeCl3 и сульфат Fe2(SO4)3 трехвалентного железа растворимы и могут образовываться даже в слабощелочных водах.
4. Органическое железо. Органическое железо встречается в воде в разных формах и в составе различных комплексов. Органические соединения железа, как правило, растворимы или имеют коллоидную структуру и очень трудно поддаются удалению.
Различают следующие виды органического железа:
Бактериальное железо. Некоторые виды бактерий способны использовать энергию растворенного железа в процессе своей жизнедеятельности. При этом происходит преобразование двухвалентного железа в трехвалентное, которое сохраняется в желеобразной оболочке вокруг бактерии.
Коллоидное железо. Коллоиды — это нерастворимые частицы очень малого размера (менее 1 микрона), в силу чего они трудно поддаются фильтрации на гранулированных фильтрующих материалах. Крупные органические молекулы (такие, как танины и лигнины) также попадают в эту категорию. Коллоидные частицы из-за своего малого размера и высокого поверхностного заряда (отталкивающего частицы друг от друга, препятствуя их укрупнению) создают в воде суспензии и не осаждаются, находясь во взвешенном состоянии.
Растворимое органическое железо. Так же, как, например, полифосфаты, способны связывать и удерживать в растворе кальций и другие металлы, некоторые органические молекулы способны связывать железо в сложные растворимые комплексы, называемые хелатами. Примером такого связывания может служить удерживающая железопорфириновая группа гемоглобина крови или удерживающий магний хлорофилл растений. Так, прекрасным хелатообразующим агентом является гуминовая кислота, играющая важную роль в почвенном ионообмене. Все вышеперечисленные виды железа «ведут» себя в воде по-разному. Основные отличительные признаки приведены в таблице.
Все вышеперечисленные виды железа «ведут» себя в воде по-разному. Основные отличительные признаки приведены в таблице.
| Тип железа | Вода из-под крана | Вода после отстаивания |
| Двухвалентное | Чистая | Красно-бурый осадок |
| Трехвалентное | Окрашена | Красно-бурый осадок |
| Коллоидное | Желто-бурая | Не образует осадка, не фильтруется |
| Растворенное органическое | Желто-бурая | |
| Бактериальное | Опалесцирующая пленка, желеобразные образования вводопроводной системе |
Необходимо только отметить, что «беда никогда не ходит одна» и на практике почти всегда встречается сочетание нескольких или даже всех видов железа. Учитывая, что нет единых утвержденных методик определения органического, коллоидного и бактериального железа, то в деле подбора эффективного метода (скорее, комплекса методов) обезжелезивания многое зависит от практического опыта специалиста, занимающегося обеспечением систем фильтров для очистки воды.
Учитывая, что нет единых утвержденных методик определения органического, коллоидного и бактериального железа, то в деле подбора эффективного метода (скорее, комплекса методов) обезжелезивания многое зависит от практического опыта специалиста, занимающегося обеспечением систем фильтров для очистки воды.
Очистка воды от железа, удаление его из воды — без преувеличения одна из самых сложных задач в фильтрах для очистки воды. Даже беглый обзор существующих способов обезжелезивания позволяет сделать обоснованный вывод о том, что на данный момент не существует универсального экономически оправданного метода, применимого во всех случаях жизни. Одни методы и фильтры для воды достаточно эффективны в быту в городской среде, однако они могут быть бессильны в процессе очистки воды от железа в коттеджах или производстве — многое зависит от качества фильтруемой воды. Каждый из существующих методов применим только в определенных пределах, и имеет как достоинства, так и существенные недостатки.
Итак, к существующим методам удаления железа можно отнести:
1. Окисление (кислородом воздуха или аэрацией, хлором, перманганатом калия, перекисью водорода, озоном) с последующим осаждением (с коагуляцией или без нее) и фильтрацией.
Окисление (кислородом воздуха или аэрацией, хлором, перманганатом калия, перекисью водорода, озоном) с последующим осаждением (с коагуляцией или без нее) и фильтрацией.
Традиционный метод, применяемый уже много десятилетий. Так как реакция окисления железа требует довольно длительного времени, то использование для окисления только воздуха требует больших резервуаров, в которых можно обеспечить нужное время контакта. Это наиболее старый способ и используется только на крупных муниципальных системах. Добавление же специальных окислителей ускоряет процесс. Наиболее широко применяется хлорирование, так как параллельно позволяет решать проблему с дезинфекцией. Наиболее передовым и сильным окислителем на сегодняшний день является озон. Однако установки для его производства довольно сложны, дороги и требуют значительных затрат электроэнергии, что ограничивает его применение. Необходимо отметить также, что в концентрированном виде (например, на точке ввода в воду) озон является ядом (как, собственно говоря, и многие другие окислители) и требует очень внимательного к себе отношения.
Частицы окисленного железа имеют достаточно малый размер (1-3 мкм) и поэтому осаждаются достаточно долго, поэтому применяют специальные химические вещества-коагулянты, способствующие укрупнению частиц и их ускоренному осаждению. Применение коагулянтов необходимо также потому, что фильтрация на муниципальных очистных сооружениях осуществляется в основном на устаревших песчаных или антрацитовых осветлительных фильтрах (не способных задерживать мелкие частицы). Однако даже применение более современных фильтрующих засыпок (например, алюмосиликатов) не позволяет фильтровать частицы размером менее 20 микрон. Проблему очистки воды от железа могло бы решить применение специальной керамики, но она достаточно дорого стоит (так как не производится в России).
У всех перечисленных способов окисления есть ряд недостатков.
Во-первых, если не применять коагулянты, то процесс осаждения окисленного железа занимает долгое время, в противном же случае фильтрация некоагулированных частиц сильно затрудняется из-за их малого размера.
Во-вторых, эти методы окисления (в меньшей степени это относится к озону) слабо помогают в борьбе с органическим железом.
В-третьих, наличие в воде железа часто (практически всегда) сопровождается наличием марганца. Марганец окисляется гораздо труднее, чем железо, и, кроме того, при значительно более высоких уровнях рН, что естественным образом затрудняет очистку воды от железа
Все вышеперечисленные недостатки сделали невозможным применение этого метода в сравнительно небольших бытовых и коммерческо-промышленных системах, работающих на больших скоростях.
2. Каталитическое окисление с последующей фильтрацией — наиболее распространенный на сегодняшний день метод удаления железа, применяемый в высокопроизводительных компактных системах.
Суть метода заключается в том, что реакция окисления железа происходит на поверхности гранул специальной фильтрующей среды, обладающей свойствами катализатора (ускорителя химической реакции окисления). Наибольшее распространение в современной водоподготовке нашли фильтрующие среды на основе диоксида марганца MnO2: Birm, Filox, Pyrolox, МЖФ, Bremix. и др. Эти фильтрующие «засыпки» отличаются между собой как своими физическими характеристиками, так и содержанием диоксида марганца, и поэтому эффективно работают в разных диапазонах значений параметров, характеризующих воду.
Наибольшее распространение в современной водоподготовке нашли фильтрующие среды на основе диоксида марганца MnO2: Birm, Filox, Pyrolox, МЖФ, Bremix. и др. Эти фильтрующие «засыпки» отличаются между собой как своими физическими характеристиками, так и содержанием диоксида марганца, и поэтому эффективно работают в разных диапазонах значений параметров, характеризующих воду.
Однако принцип их работы одинаков. Железо (и в меньшей степени марганец) в присутствии диоксида марганца быстро окисляется и оседает на поверхности гранул фильтрующей среды. Впоследствии большая часть окисленного железа вымывается в дренаж при обратной промывке. Таким образом, слой гранулированного катализатора является одновременно и фильтрующей средой. Для улучшения процесса окисления в воду могут добавляться дополнительные химические окислители. Наиболее распространенным является перманганат калия KMnO4 («марганцовка»), так как его применение не только активизирует реакцию окисления, но и компенсирует «вымывание» марганца с поверхности гранул фильтрующей среды, то есть регенерирует ее. Используют как периодическую, так и непрерывную регенерацию.
Используют как периодическую, так и непрерывную регенерацию.
Все системы на основе каталитического окисления с помощью диоксида марганца кроме специфических (не все из них работают по марганцу, почти все они имеют большой удельный вес и требуют больших расходов воды при обратной промывке) имеют и ряд общих недостатков.
Во-первых, они неэффективны в отношении органического железа. Более того, при наличии в воде любой из форм органического железа на поверхности гранул фильтрующего материала со временем образуется органическая пленка, изолирующая катализатор — диоксид марганца от воды. Таким образом, вся каталитическая способность фильтрующей засыпки сводится к нулю. Практически «на нет» сводится и способность фильтрующей среды удалять железо, так как в фильтрах этого типа просто не хватает времени для естественного протекания реакции окисления.
Во-вторых, системы этого типа все равно не могут справиться со случаями, когда содержание железа в воде превышает 10-15 мг/л, что совсем не редкость. Присутствие в воде марганца только усугубляет ситуацию.
Присутствие в воде марганца только усугубляет ситуацию.
Для обезжелизивания воды методом окисления Компания «Первая вода» предлагает фильтры с загрузками Birm и МЖФ. Данные фильтрующие среды не требуют применения химических окислителей (марганцовки). Восстановление свойств фильтрующей среды происходит при помощи взрыхления обратным потоком воды. Удаленные соединения железа и марганца смываются в канализацию.
АВТОМАТИЧЕСКИЕ ФИЛЬТРЫ ОБЕЗЖЕЛЕЗИВАНИЯ
3. Ионный обмен как метод обработки воды известен довольно давно и применяется в основном для умягчения воды. Раньше для реализации этого метода использовались природные иониты (сульфоугли, цеолиты). Однако с появлением синтетических ионообменных смол эффективность использования ионного обмена для целей водоочистки резко возросла.
С точки зрения удаления железа из воды важен тот факт, что катиониты способны удалять из воды не только ионы кальция и магния, но и другие двухвалентные металлы, а значит и растворенное двухвалентное железо. Причем теоретически концентрации железа, с которыми могут справиться ионообменные смолы, очень велики. Еще основным достоинством ионного обмена является возможность умягчения воды одновременно с обезжелезивание и удалеением марганца.
Причем теоретически концентрации железа, с которыми могут справиться ионообменные смолы, очень велики. Еще основным достоинством ионного обмена является возможность умягчения воды одновременно с обезжелезивание и удалеением марганца.
Восстановление рабочих свойств фильтрующего материала (регенерация) – автоматизированный процесс при помощи раствора соли и воды. Раствор соли пропускается через фильтрующий материал, а удаленные загрязнения смываются в канализацию.
Достоинством ионного обмена является также и то, что он «не боится» верного спутника железа — марганца, сильно осложняющего работу систем, основанных на использовании методов окисления. Главное же преимущество ионного обмена в том, что из воды могут быть удалены железо и марганец, находящиеся в растворенном состоянии. То есть совсем отпадает необходимость в такой капризной и «грязной» (из-за необходимости вымывать ржавчину) стадии, как окисление.
КОМПЛЕКСНЫЕ АВТОМАТИЧЕСКИЕ ФИЛЬТРЫ ДЛЯ ОБЕЗЖЕЛЕЗИВАНИЯ И УМЯГЧЕНИЯ ВОДЫ
Специалисты компании «Первая вода» выполняют грамотный подбор оборудования по обезжелезиванию воды и удалению марганца.
 Обращайтесь к нам и вы получите качественную исчерпывающую консультацию по вопросам водоочистки.
Обращайтесь к нам и вы получите качественную исчерпывающую консультацию по вопросам водоочистки. Очистка воды от железа. Обзор методов.
Появляются ржавые подтеки на раковине?
На воздухе прозрачная вода из крана стала мутной, и выпал рыжий осадок?
Как бороться с избыточным железом и на что обратить внимание при выборе систем очистки воды от железа?
Ответы на все эти вопросы в нашей статье.
Определение типа железа в воде
Прежде чем приступить к выбору оборудования для очистки воды от железа, следует понять, какой тип железа присутствует в воде.
- Двухвалентное железо (Fe+2) содержится в воде в растворенном состоянии и невидимо невооруженным глазом. Как правило, растворенное железо присутствует в воде из подземных источников (скважин). В присутствии двухвалентного железа вода выглядит прозрачной, но когда некоторое время находится в контакте с воздухом, приобретает рыжий цвет, и выпадает осадок. Это явление происходит вследствие окисления железа кислородом воздуха до трехвалентного состояния.
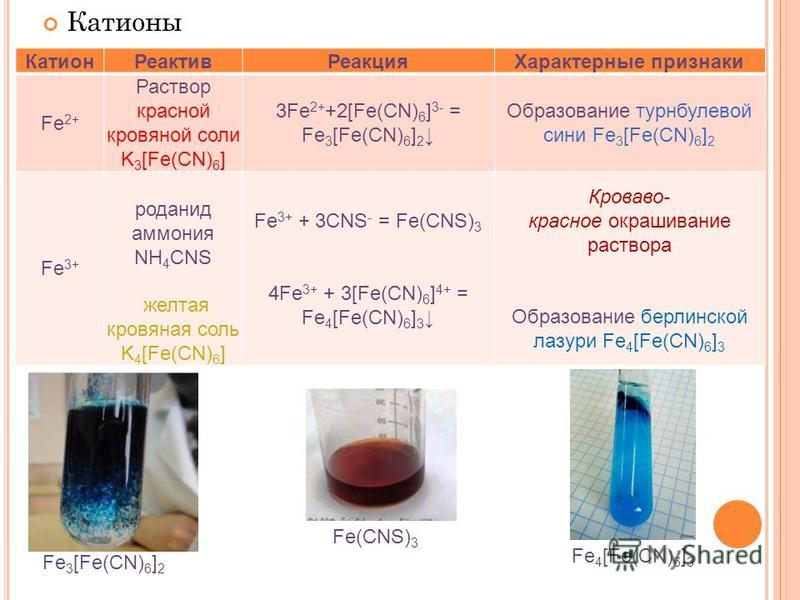
- Трехвалентное железо (Fe+3), окисленное — присутствует в воде в коллоидной форме (образует очень мелкие частицы рыжего цвета). Осаждение коллоидного железа может сопровождаться образованием и ростом железобактерий. Присутствие окисленного железа характерно для воды из поверхностных источников (колодцы, водоемы) и для воды из централизованного водопровода.
- Бактериальное железо (железобактерии) часто сопутствует минеральным отложениям Fe3+ и состоит из живых и мертвых бактерий, их оболочек и продуктов жизнедеятельности. Бактериальное железо достаточно легко отличить от минерального железа — это мягкие вязкие слизистые отложения. В некоторых случаях они безвредны, в других — наносят огромный ущерб. В трубопроводе и водоочистном оборудовании железобактерии часто становятся причиной язвенной коррозии железа и стали и сильно ускоряют образование железистых отложений.
Заполните форму для получения консультации специалиста по водоподготовке
Сообщение
Я подтверждаю согласие на обработку своих персональных данных.
Поставьте галку
Оборудование для очистки воды от железа
- Каталитическое удаление железа (фильтры-обезжелезиватели)
На рынке есть большое многообразие систем обезжелезивания, работающих по принципу каталитического окисления железа, в процессе которого двухвалентное железо (растворенное) переходит в форму трехвалентного железа (нерастворенного), оседающего на фильтрующей загрузке. Такие системы получили название
Принципиально данные фильтры отличаются по принципу окисления железа, которое может производиться безреагентным способом (кислородом воздуха) или же использованием сильных окислителей.
Безреагентные способы являются безопасными для использования в быту, но менее эффективны и стабильны по качеству очистки. Такие фильтры плохо работают в условиях высокой концентрации железа в исходной воде и требовательны к сопутствующим показателям (необходим высокий рН, низкое содержание органических веществ).
Реагентные способы менее чувствительны к составу исходной воды, но сопряжены с работой с сильными окислителями (гипохлорит натрия, перекись водорода, перманганат калия), что небезопасно для использования в домашних условиях, так как в случае аварийной ситуации с оборудованием или изменения состава исходной воды, реагент может попасть в очищенную воду.
После введения окислителя вода попадает на каталитическую загрузку, обеспечивающую последующее окисление и фильтрацию железа.
Если Вы остановили свой выбор на системах каталитического обезжелезивания, то при выборе оборудования необходимо учитывать температуру воды, рН, щелочность, содержание растворенного кислорода и другие параметры, которые могут значительно повлиять на эффективность очистки. При эксплуатации необходимо строго следовать рекомендациям производителя, устанавливая скорость прямого потока воды, скорость потока при обратной промывке, учитывать максимальное содержание входного железа и другие ограничения, которые влияют на рабочие параметры процесса очистки для эффективной работы всего оборудования и фильтрующего материала в частности.
Самые распространенные причины плохой работы фильтра-обезжелезивателя — неполное окисление железа вследствие колебаний в составе исходной воды, низкой скорости потока при обратной промывке, недостаточно частого проведения регенерации фильтрующего материала или подачи на фильтрацию большого потока воды.
Все эти факторы могут стать причиной некачественной работы фильтров-обезжелезивателей. Для обеспечения стабильного результата при обезжелезивании целесообразно предпочесть системы обратного осмоса.
- Обратный осмос
Системы обратного осмоса наиболее эффективны для удаления растворенного железа и по многим параметрам превосходят альтернативные методы обезжелезивания. Поскольку ионы железа намного крупнее пор обратноосмотических мембран, они эффективно задерживаются на мембранах. При этом железо не накапливается в мембране, а сливается в дренаж с концентратом, что предотвращает проблему закупоривания пор. Системы обратного осмоса могут очищать воду с содержанием растворенного железа до 10-20 мг/л.
Обратный осмос может использоваться и для удаления трехвалентного железа в невысоких концентрациях.
Системы обратного осмоса эффективны для очистки воды от распространенного спутника железа — марганца.
- Ионный обмен
Для удаления двухвалентного железа в невысоких концентрациях (незначительно превышающих норму) может использоваться катионообменная смола. Этот метод может быть целесообразен при очистке воды с повышенной жесткостью и невысоких концентрациях растворенного железа. Ионообменная смола замещает ионы железа и солей жесткости на натрий, однако, эффективно работает лишь при низком содержании двухвалентного железа (до 1 мг/л).
Серьезным осложнением работы смолы является возможное окисление железа и переход в форму трехвалентного. При этом на поверхности ионообменного материала появляется непроницаемая окисная пленка, что резко уменьшает обменную емкость катионита за счет снижения реакционной поверхности материала.
Ионообменные системы не очень удобны в эксплуатации, так как требуют постоянного контроля за присутствием соли, необходимой для регенерации смолы (хлорид натрия в таблетированной форме) и ее пополнением.
- Ультрафильтрация
Ультрафильтрационные мембраны с размером пор около 0,02 микрон прекрасно задерживают коллоидное железо. Установки ультрафильтрации с режимами периодического сброса концентрата и обратной промывки мембран обеспечивают эффективное удаление трехвалентного железа. Для эффективности очистки с помощью ультрафильтрации все железо должно быть переведено в окисленное состояние. Рекомендуется предварительное введение коагулянта и обеспечения необходимого времени его контакта с водой.
Удаление бактериального железа
При наличии в исходной воде большого количества железа пользователь может столкнуться еще с одной проблемой — появлением бактериальных загрязнений — активным развитием железобактерий.
Если проблема железобактерий выявлена на ранней стадии, регулярное хлорирование или обработка хелатными агентами (органические вещества, образующие растворимые комплексы с железными отложениями), а также постоянное наблюдение за состоянием оборудования помогут минимизировать её последствия.
На ранней стадии появления железобактерий может помочь ударное хлорирование — необходимо создать избыточную концентрацию хлора 50 мг/л. Перед применением хлорирования нужно выяснить, насколько устойчиво к хлору установленное водоочистное оборудование.
Проблему с бактериальным железом может решить среда redox, однако, в подводящих трубопроводах при этом железобактерии будут продолжать развиваться и образовывать слизистые отложения.
Выводы
Несмотря на большое количество методов удаления железа, наиболее оптимальным методом очистки от двухвалентного железа, обычно присутствующего в подземных источниках, и трехвалентного железа в невысоких концентрациях, является применение систем обратного осмоса.
При содержании в воде большого количества трехвалентного железа рекомендуется применять системы ультрафильтрации.
По всем вопросам очистки воды обращайтесь к нам — опытные специалисты по водоподготовке проконсультируют Вас по любой проблеме, связанной с водой для Вашего дома.
Для консультации с нашими специалистами позвоните нам или отправьте заявку:
Отправить заявку
Скачать опросный лист для частных лиц
С оборудованием для очистки воды для дома Вы можете ознакомиться в разделе Системы очистки воды
Мы предлагаем Вам записаться на демонстрацию работы мембранной системы водоочистки, и наши специалисты подъедут к Вам в любое удобное для Вас время. Вы сможете увидеть, какой будет вода в Вашем доме, если ее очистить с помощью нашего оборудования.
Выезд специалистов и демонстрация работы оборудования бесплатны.
Пейте чистую воду и будьте здоровы!
Рекомендуем прочитать:
Чистая ли вода в скважине? Способы очистки воды из скважины
Соленая вода в скважине – проблема и решения
Нитраты в воде. Опасность и методы очистки воды от нитратов
Опасность и методы очистки воды от нитратов
Очистка воды для коттеджей и квартир или О голубой воде и мембранной технологии
Пир во время цинги или Полезно ли пить обратноосмотическую воду
Глоссарий по очистке воды и водоподготовке
Основы мембранной технологии
Обратный осмос и нанофильтрация в водоочистке
КАТАЛОГ ОБОРУДОВАНИЯ
Разница между железом и железом
24 ноября 2015 г.
от admin
Чтение через 4 мин.
Главное отличие — железо против железа
Оба эти термина, железо и железо, относятся к разным формам существования элемента Железо. Железо — это элемент в «d-блоке» периодической таблицы, что означает, что это переходный металл. Эти металлы имеют особую характеристику проявления нескольких валентностей. Следовательно, переходные металлы могут иметь несколько стабильных степеней окисления. Это возможно благодаря наличию пяти гибридных орбиталей. Основное различие между железом и железом состоит в том, что железо — это +2 степень окисления железа , а железо — это +3 степень окисления железа
что такое железо
Как упоминалось выше, это степень окисления +2 элемента железа и считается стабильным ионом . Его оксид имеет зеленый цвет и является первым шагом в образовании ржавчины. Поскольку железо является металлом, ему необходимо высвобождать или отдавать электроны и образовывать положительные ионы, чтобы получить стабильную электронную конфигурацию. Общая электронная конфигурация элемента железа может быть записана как 1s 9. Когда дело доходит до железа, два электрона высвобождаются с 4s-орбиталей, поскольку это самая внешняя орбиталь. Однако 3d-орбитали имеют более высокую энергию, чем 4s-орбитали. Поэтому сброс электронов происходит с 4s-орбиталей, хотя в конце концов электроны заполняются на 3d-орбитали.
Его оксид имеет зеленый цвет и является первым шагом в образовании ржавчины. Поскольку железо является металлом, ему необходимо высвобождать или отдавать электроны и образовывать положительные ионы, чтобы получить стабильную электронную конфигурацию. Общая электронная конфигурация элемента железа может быть записана как 1s 9. Когда дело доходит до железа, два электрона высвобождаются с 4s-орбиталей, поскольку это самая внешняя орбиталь. Однако 3d-орбитали имеют более высокую энергию, чем 4s-орбитали. Поэтому сброс электронов происходит с 4s-орбиталей, хотя в конце концов электроны заполняются на 3d-орбитали.
Следовательно, электронная конфигурация двухвалентного железа будет 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 . Теперь эта ионная форма способна образовывать соединения и комплексы с другими элементами и отрицательно заряженными ионами. Эти комплексы также могут быть в ионной форме, и в этом случае они обычно известны как «соединения переходных металлов». дается в скобках, например «оксид железа (II)». Некоторыми примерами известных соединений железа являются FeO, FeCl 2 , FeSO 4, и т.д.
дается в скобках, например «оксид железа (II)». Некоторыми примерами известных соединений железа являются FeO, FeCl 2 , FeSO 4, и т.д.
Что такое железо
Железо известно как железо со степенью окисления +3 и является наиболее стабильной формой железа в воздухе . При окислении железа оно превращается в оксид железа, а в присутствии большего количества кислорода ион железа окисляется с образованием ионов железа, в данном случае «оксида железа», который представляет собой ржавчину. Это хлопьевидный материал коричневого цвета. Возвращаясь к определению, чтобы образовался ион трехвалентного железа, элементарная форма железа должна отдать три электрона со своих орбиталей. Результирующая электронная конфигурация иона трехвалентного железа будет: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 . Эта конфигурация более стабильна, чем ион двухвалентного железа, а также элементарная форма. Так как эта конфигурация удовлетворяет частичному электронному заполнению.
Так как эта конфигурация удовлетворяет частичному электронному заполнению.
Чтобы объяснить это подробнее, существует пять d’-орбиталей. Любая конфигурация, в которой орбитали полностью или наполовину заполнены, считается более стабильной, чем другие формы. В случае иона трехвалентного железа каждая d-орбиталь содержит электрон, что делает ее заполненной наполовину, поскольку d-орбитали содержат пять электронов. Ионы трехвалентного железа также образуют другие соединения и комплексы, и при наименовании неорганических комплексов их записывают как «Железо (lll)». Одними из наиболее распространенных соединений трехвалентного железа являются Fe 2 O 3 , FECL 3 , FE 2 (SO 4 ) 3, и т. Д.
Разница между железом и железной дорогой
. степень окисления железа.
Железо — степень окисления железа +3.
Стабильность
Железо +2 относительно менее стабильно.
У иона трехвалентного железа его d-орбитали наполовину заполнены в самой внешней оболочке, что делает его более стабильным, чем другие формы железа.
Окисление/восстановление
Железо может образовываться путем восстановления ионов трехвалентного железа.
Ионы трехвалентного железа образуются в результате окисления элементов железа после стадии ионов двухвалентного железа.
Процесс окисления
Ионы двухвалентного железа образуются в результате потери 4s-электронов элементом Железо.
Ионы трехвалентного железа образуются в результате потери как 4s-, так и 3d-электронов.
Изображение предоставлено:
«Оксид железа (II)» от Calvero (общественное достояние) через Commons
«Образец оксида железа (III)» от Benjah-bmm27 — собственная работа. (общественное достояние) через Commons
Об авторе: admin
Просмотреть все сообщения
Вам также могут понравиться эти
Разница между железом и железом
Ключевое отличие — железо против железа Железо является одним из самых распространенных металлических элементов на земле, а железо (Fe 2+ ) и железо (Fe 2+ ) представляют собой две формы окисления элементарного железа, между которыми существует разница, основанная на их электронной конфигурации. Железо имеет степень окисления +2, а железо имеет степень окисления +3. Другими словами, это два стабильных иона одного родительского элемента. Ключевое различие между этими двумя ионами заключается в их электронной конфигурации. Ион двухвалентного железа образуется путем удаления 2d-электронов из атома железа, тогда как ион трехвалентного железа образуется путем удаления 3d-электронов из атома железа
Железо имеет степень окисления +2, а железо имеет степень окисления +3. Другими словами, это два стабильных иона одного родительского элемента. Ключевое различие между этими двумя ионами заключается в их электронной конфигурации. Ион двухвалентного железа образуется путем удаления 2d-электронов из атома железа, тогда как ион трехвалентного железа образуется путем удаления 3d-электронов из атома железа
Что такое железо?
Двухвалентное железо имеет степень окисления +2; образован удалением двух электронов 3s-оболочки от нейтрального атома железа . При образовании двухвалентного железа 3d-электроны остаются прежними, образующийся ион имеет все шесть d-электронов. Ион двухвалентного железа является парамагнитным, потому что у него есть неспаренные электроны на внешней оболочке. Хотя он имеет четное число d-электронов, когда они заполняют пять d-орбиталей, некоторые электроны остаются в ионе неспаренными. Но когда он связывается с другими лигандами, это свойство может быть изменено. Ионы двухвалентного железа являются относительно более основными, чем ионы трехвалентного железа.
Хотя он имеет четное число d-электронов, когда они заполняют пять d-орбиталей, некоторые электроны остаются в ионе неспаренными. Но когда он связывается с другими лигандами, это свойство может быть изменено. Ионы двухвалентного железа являются относительно более основными, чем ионы трехвалентного железа.
Что такое Феррик?
Трехвалентное железо имеет степень окисления +3; образован удалением двух электронов 3s-оболочки и одного d-электрона из нейтрального атома железа . Трехвалентное железо имеет 5d-электроны на внешней оболочке, и эта электронная конфигурация относительно стабильна из-за дополнительной стабильности за счет наполовину заполненных орбиталей. Ионы трехвалентного железа более кислые по сравнению с ионами двухвалентного железа. Ионы трехвалентного железа могут выступать в качестве окислителя в некоторых реакциях. Например, он может окислять ионы йода до темно-коричневого раствора, если йод.
2Fe 3+ (aq) + 2I – (aq) → 2Fe 2+ (aq) + I 2(aq/s)
What is the разница между Ferrous и Ferric?
Характеристики железа и железа:
Электронная конфигурация:
Электронная конфигурация железа;
1с 2 , 2с 2 , 2п 6 , 3с 2 , 3p 6 , 4s 2 , 3d 6
Двухвалентное железо:
Двухвалентное железо образуется при удалении двух электронов (двух 3s-электронов) из атома железа. Двухвалентное железо имеет шесть электронов в d-оболочке.
Двухвалентное железо имеет шесть электронов в d-оболочке.
Fe → Fe 2+ + 2E
Он имеет конфигурацию электрона 1S 2 , 2S 2 , 2P 6 , 3S 2 , 3P 6 , 3D 6 .
Феррик:
Трехвалентное железо образуется при удалении трех электронов (двух 3s-электронов и одного d-электрона) из железа. Трехвалентное железо имеет пять электронов в d-оболочке. Это полузаполненное состояние на d-орбиталях считается относительно устойчивым. Следовательно, ионы трехвалентного железа относительно стабильны, чем ионы двухвалентного железа.
Fe → Fe 3+ + 3E
Он имеет конфигурацию электрона 1S 2 , 2S 2 , 2P 6 , 3S 2 , 3P 6 , 3S 2 , 3P 6 , 3S 2 , 3P 6 , 3S 20028, 3д 5 .
Растворимость в воде:
Железо:
Когда в воде присутствуют ионы железа, образуется прозрачный бесцветный раствор. Потому что двухвалентное железо полностью растворяется в воде. В природных водотоках небольшое количество Fe 2+ .
Потому что двухвалентное железо полностью растворяется в воде. В природных водотоках небольшое количество Fe 2+ .
Железо:
Его можно четко определить, если в воде присутствуют ионы трехвалентного железа (Fe 3+ ). Потому что он дает красочные отложения с характерным вкусом для воды. Эти отложения образуются из-за того, что ионы трехвалентного железа нерастворимы в воде. Довольно неприятно, когда ионы железа растворяются в воде; люди не могут использовать воду, содержащую ионы железа.
Комплексообразование с водой:Железо:
Ион двухвалентного железа образует комплекс с шестью молекулами воды; его называют ионом гексаакварона (II) [Fe(H 2 O) 6 ] 2+ (водн.) . Он бледно-зеленого цвета.
Железо:
Ион трехвалентного железа образует комплекс с шестью молекулами воды; его называют ионом гексаакварона (III) [Fe(H 2 O) 6 ] 3+ (водн.
