Что такое свободные радикалы и как они влияют на старение клеток. Каков механизм действия свободных радикалов в организме. Какие существуют способы защиты от окислительного стресса. Почему теория свободных радикалов остается одной из ведущих в изучении процессов старения.
Что такое свободные радикалы и их роль в процессах старения
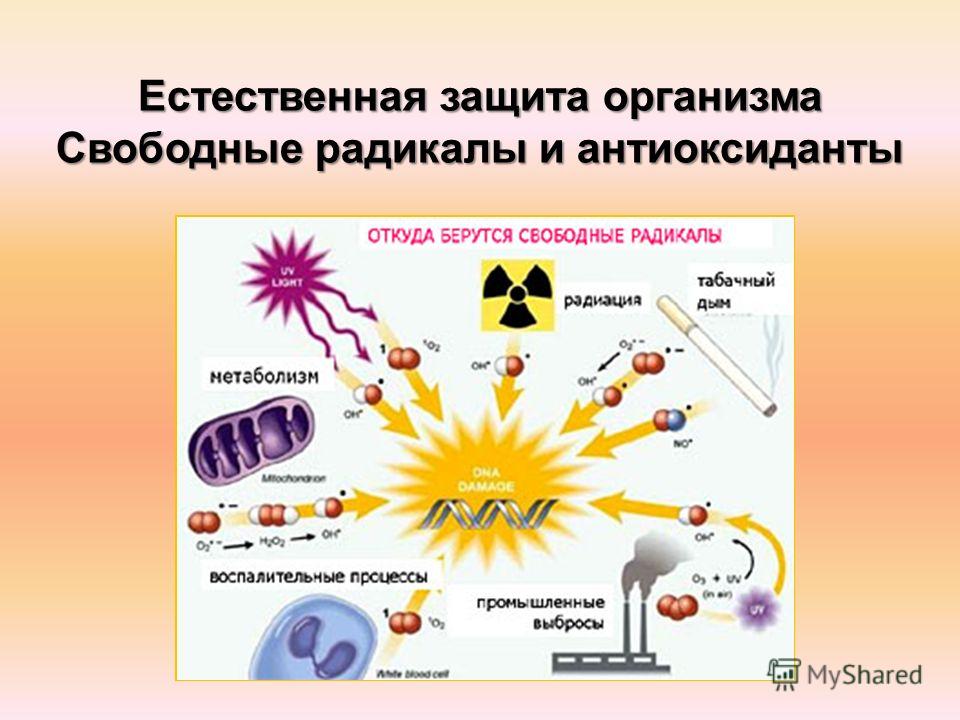
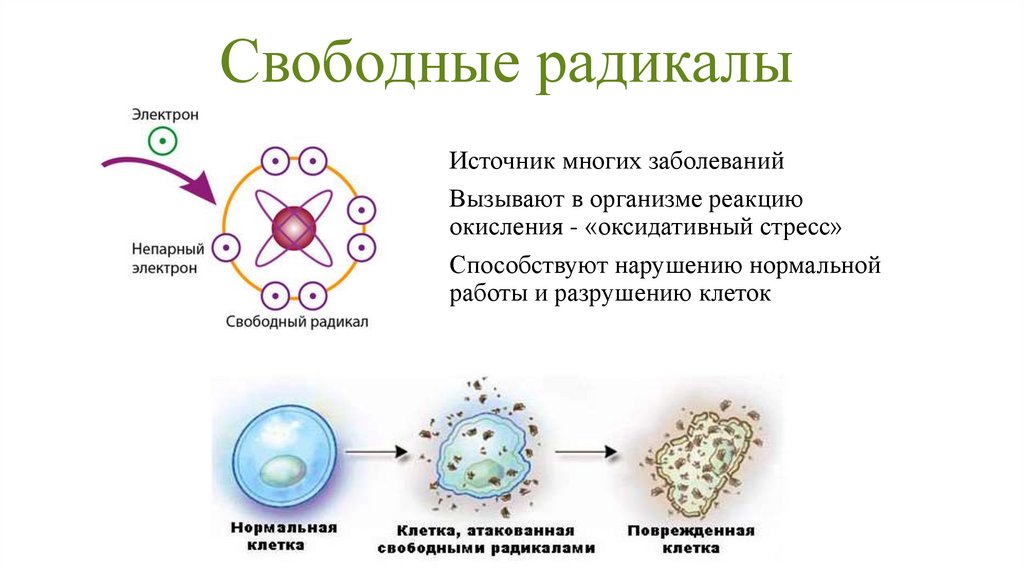
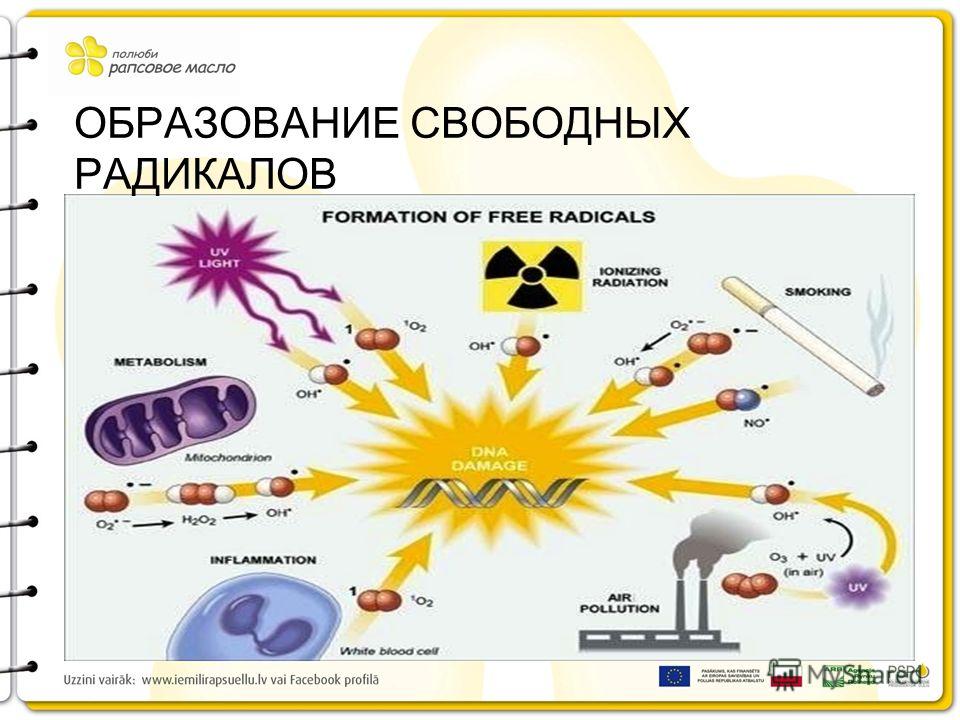
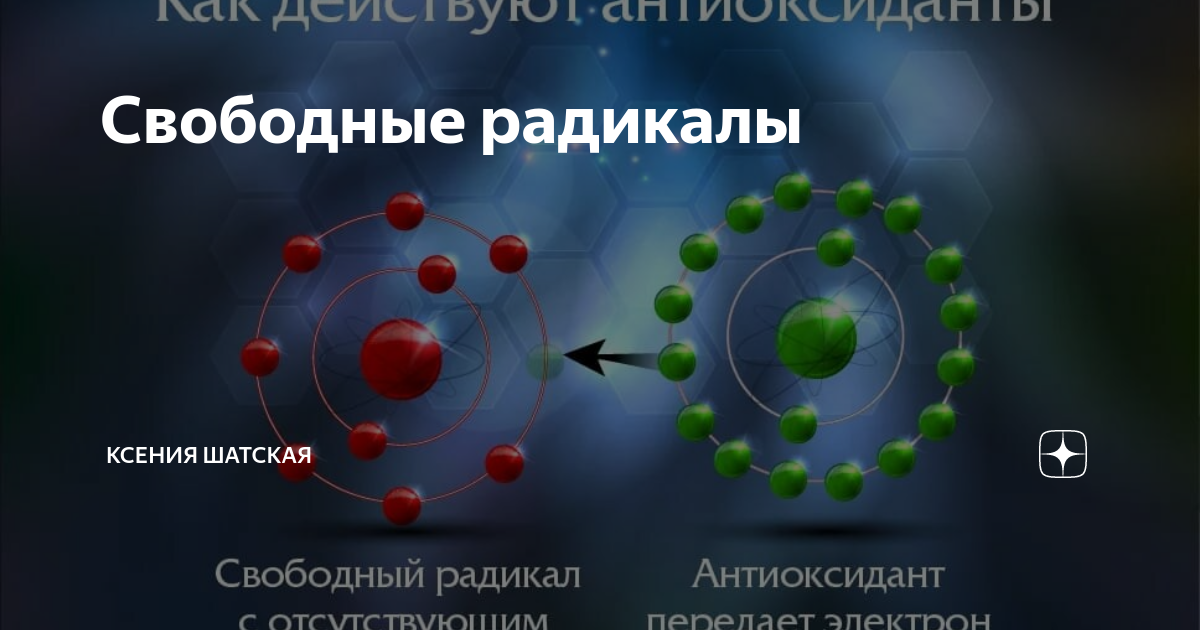
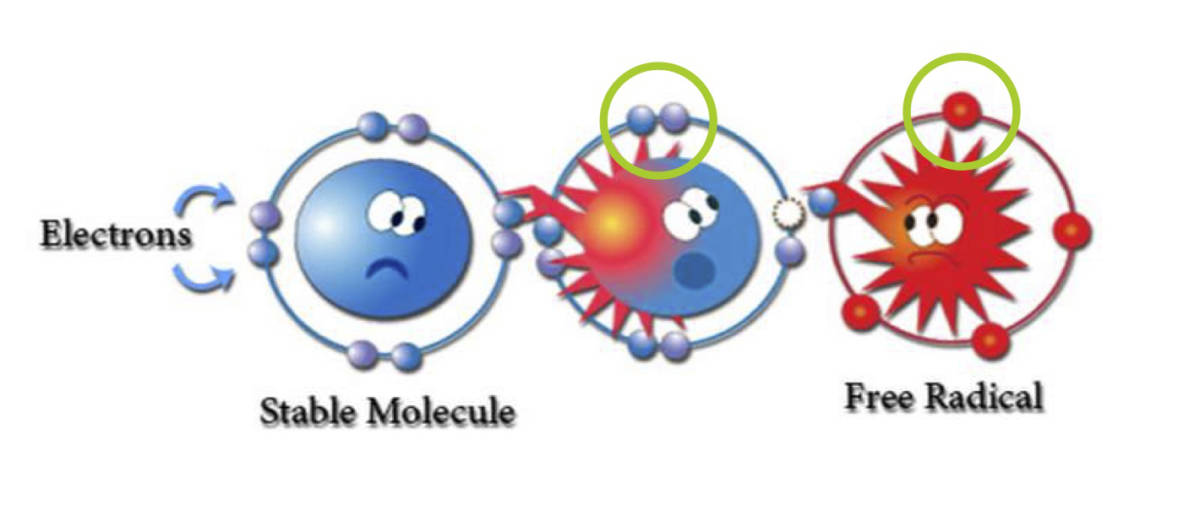
Свободные радикалы — это молекулы или атомы, имеющие неспаренный электрон на внешней оболочке. Это делает их крайне реактивными и способными повреждать другие молекулы в организме. Основными источниками свободных радикалов являются:
- Нормальные метаболические процессы в клетках
- Воздействие ультрафиолетового излучения
- Загрязнение окружающей среды
- Курение
- Употребление алкоголя
- Стресс
Согласно свободнорадикальной теории старения, предложенной Денхамом Харманом в 1950-х годах, накопление повреждений от свободных радикалов является основной причиной старения организма. Как именно это происходит?

Механизм действия свободных радикалов
Свободные радикалы атакуют важнейшие биомолекулы в клетках:
- Липиды клеточных мембран
- Белки
- ДНК
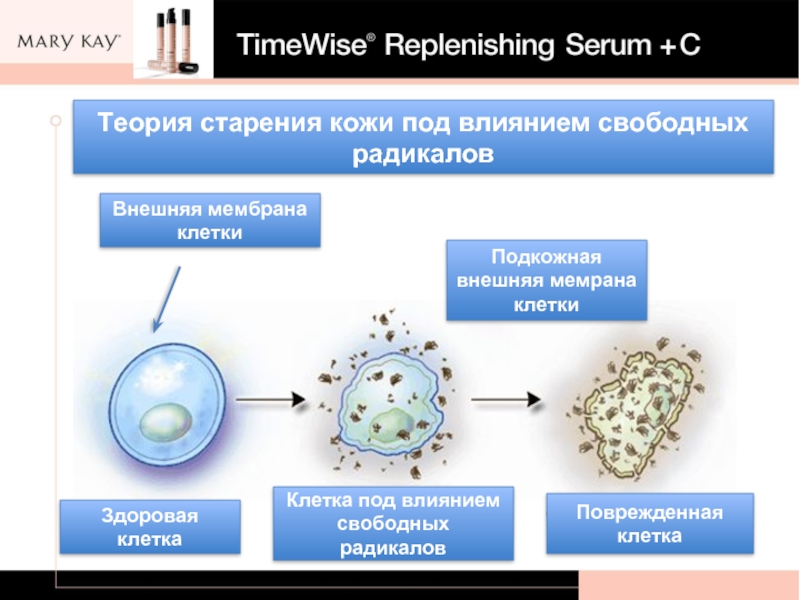
В результате нарушается целостность клеточных мембран, инактивируются ферменты, повреждается генетический материал. Все это приводит к нарушению функций клеток и их преждевременному старению.
Особенно чувствительны к окислительному стрессу митохондрии — энергетические станции клеток. Их повреждение ведет к снижению выработки энергии и ускоренному старению тканей.
Защитные механизмы организма от свободных радикалов
В процессе эволюции в организме выработались механизмы защиты от окислительного стресса. К ним относятся:
- Антиоксидантные ферменты (супероксиддисмутаза, каталаза, глутатионпероксидаза)
- Низкомолекулярные антиоксиданты (витамины C, E, глутатион)
- Системы репарации ДНК
Однако с возрастом активность этих систем снижается, что усиливает окислительное повреждение клеток. Возникает порочный круг: окислительный стресс ускоряет старение, а старение ослабляет защиту от свободных радикалов.

Способы борьбы с окислительным стрессом
Для замедления процессов старения рекомендуется:
- Употреблять больше продуктов, богатых антиоксидантами (овощи, фрукты, ягоды, зеленый чай)
- Ограничить воздействие вредных факторов (курение, алкоголь, ультрафиолет)
- Заниматься умеренными физическими нагрузками
- Избегать стрессов
- Принимать антиоксидантные добавки по рекомендации врача
Эти меры помогут снизить окислительный стресс и замедлить процессы старения организма.
Критика и современный взгляд на свободнорадикальную теорию старения
Несмотря на популярность, свободнорадикальная теория старения подвергается критике. Основные аргументы критиков:
- Прием антиоксидантов не всегда увеличивает продолжительность жизни в экспериментах
- Некоторые организмы с высоким уровнем окислительного стресса живут дольше
- Свободные радикалы играют важную роль в передаче клеточных сигналов
Современный взгляд рассматривает окислительный стресс как один из факторов старения, но не единственную его причину. Важную роль играют также:
- Укорочение теломер
- Накопление поврежденных белков
- Эпигенетические изменения
- Истощение стволовых клеток
Тем не менее, свободнорадикальная теория остается одной из ведущих в изучении механизмов старения. Она позволила лучше понять роль окислительного стресса и разработать методы борьбы с ним.
Перспективы применения теории в антивозрастной медицине
- Разработка новых антиоксидантных препаратов
- Создание косметических средств с антиоксидантами
- Методики активации собственных антиоксидантных систем организма
- Диагностика уровня окислительного стресса
Перспективными направлениями являются:
- Таргетная доставка антиоксидантов в митохондрии
- Активация систем репарации ДНК
- Регуляция сигнальных функций свободных радикалов
Эти подходы позволят более эффективно бороться с окислительным стрессом и замедлять процессы старения на клеточном уровне.
Заключение
Свободнорадикальная теория старения, несмотря на критику, остается одной из ведущих концепций в изучении механизмов старения. Она позволила:

- Лучше понять роль окислительного стресса в процессах старения
- Разработать методы диагностики и коррекции окислительных повреждений
- Создать новые подходы в anti-age медицине и косметологии
Дальнейшие исследования в этой области помогут более эффективно бороться с возрастными изменениями и увеличить период активного долголетия.
Свободнорадикальная теория старения — что именно запускает процесс старения?
Почему время разрушительно для человеческого тела и что именно запускает процессы старения? Одна из теорий, объясняющих неизбежную деградацию организма, связывает ее с чрезмерной активностью свободных радикалов.
Узнайте об особенностях Международной школы Anti-Age Expert, а также о возможностях для совершенствования врачебной практики изо дня в день. Также в программе вебинаров — увлекательные обзоры инноваций в антивозрастной медицине и разборы сложнейших клинических случаев с рекомендациями, которые действительно работают
Узнать подробнееЧто такое свободные радикалы?
Свободные радикалы — это побочный продукт нормального функционирования клеток. Когда они производят энергию, то одновременно вырабатываются нестабильные молекулы кислорода, свободные радикалы.
Эти молекулы имеют свободный электрон, и они связываются с другими молекулами организма, препятствуя их нормальному функционированию.
Свободные радикалы могут образовываться как в результате естественного процесса, так и вследствие диеты, стрессов, курения, алкоголя, физических упражнений или в результате воздействия солнца или загрязнения воздуха.
Суть свободнорадикальной теории старения
Сегодня свободнорадикальная теория старения считается одной из фундаментальных. Она была предложена американским химиком Денхамом Харманом в 50-х годах прошлого века.
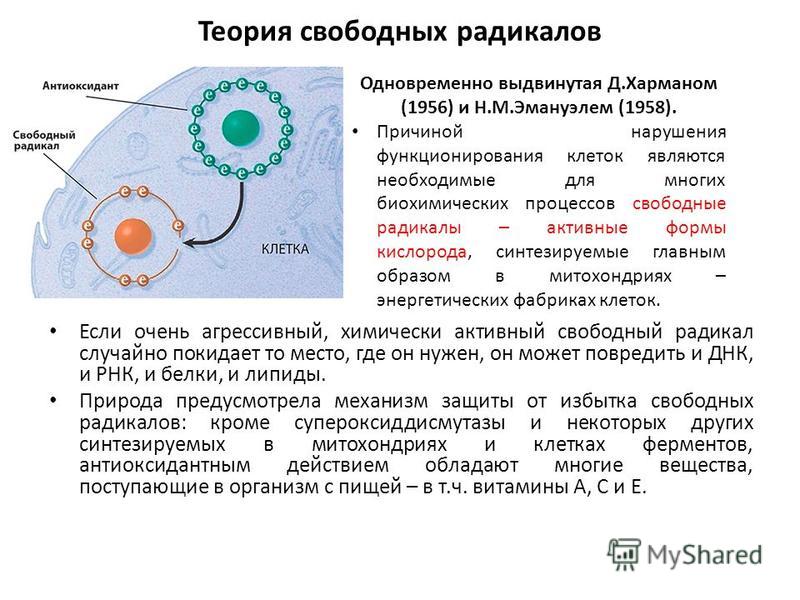
Согласно этой теории, свободные радикалы — активные формы кислорода (АФК) — являются основной причиной старения, вызывая окислительные клеточные повреждения. Свободные радикалы необходимы для многих биохимических процессов, и они образуются как побочные продукты во время некоторых биохимических реакций или как субстраты для других биохимических реакций в каждой клетке.
Свободнорадикальная теория старения состоит в том, что организмы стареют, потому что клетки накапливают повреждения свободными радикалами с течением времени. В общем, «свободный радикал» — это любая молекула, имеющая единственный неспаренный электрон на внешней оболочке.
В то время как некоторые свободные радикалы, такие как меланин, стабильны в течение многих лет, большинство биологически значимых свободных радикалов довольно реактивны. Для большинства биологических структур повреждение свободными радикалами тесно связано с повреждением окисления.
Свободные радикалы и старение
Свободнорадикальная теория старения утверждает, что многие изменения, происходящие с возрастом в нашем теле, вызваны свободными радикалами. Если агрессивный, химически активный свободный радикал покидает то место, где это необходимо, он может повредить ДНК, а также РНК, белки и липиды.
Перекисное окисление чрезвычайно опасно для полиненасыщенных жирных кислот, которые являются компонентом клеточных мембран, поскольку продукты реакции (пероксиды и гидропероксиды) также обладают высоким кислородным потенциалом.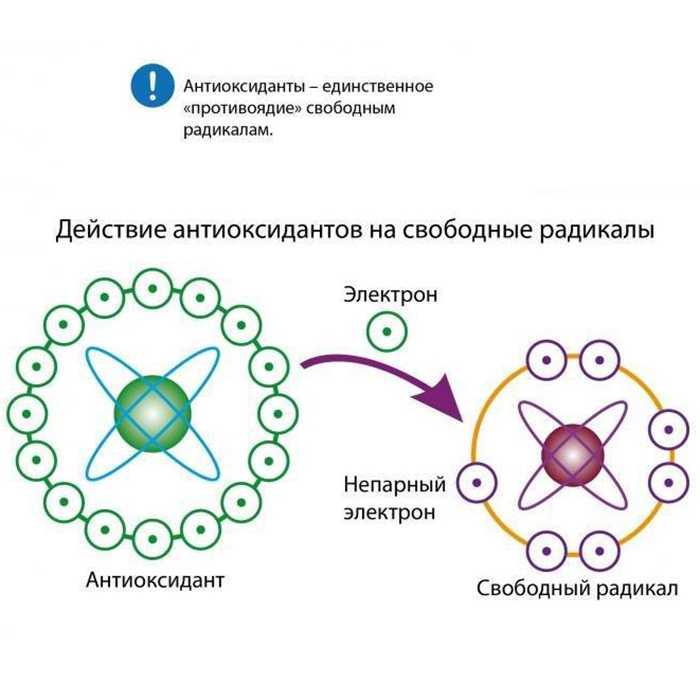 В результате процесс повреждения клеток становится лавинообразным.
В результате процесс повреждения клеток становится лавинообразным.
Повреждение макромолекул (и всей клетки) под действием АФК называется окислительным (оксидативным) стрессом. Он вызывает старение, а также широкий спектр возрастных патологических процессов (сердечно-сосудистые заболевания, возрастная метаболическая иммунодепрессия, дисфункция мозга, катаракта, рак и т. Д.).
Некоторые исследования на примере дрожжей и дрозофил показали, что уменьшение окислительного повреждения может продлить продолжительность жизни. Кроме того, у мышей вмешательства, которые усиливают окислительное повреждение, обычно сокращают продолжительность жизни.
Онлайн обучениеAnti-Age медицине
Изучайте тонкости антивозрастной медицины из любой точки мира. Для удобства врачей мы создали обучающую онлайн-платформу Anti-Age Expert: Здесь последовательно выкладываются лекции наших образовательных программ, к которым открыт доступ 24/7.
Защита от свободных радикалов
Природа предусмотрела механизмы защиты от избытка свободных радикалов, и большинство АФК обезвреживаются до того, как нанесут урон каким-либо клеточным структурам.
Основными факторами антиоксидантной защиты организма являются специальные ферменты: супероксиддисмутаза и некоторые другие. Некоторые антиоксидантные химические вещества поступают в организм с пищей. К ним относятся витамин A, витамин C и витамин E. Современная фармакология разрабатывает антиоксидантные добавки, которые представляют собой лекарства, защищающие организм от свободных радикалов.
Однако тот факт, что продукты взаимодействия АФК с макромолекулами постоянно находятся в органах и тканях, указывает на то, что системы, защищающие организм от свободных радикалов, недостаточно эффективны и что клетки постоянно подвергаются опасности окислительного стресса.
При этом вопрос, достаточно ли снижения уровня окислительного повреждения ниже нормального для увеличения продолжительности жизни, остается открытым и спорным. Например, как выяснилось недавно, у круглых червей (Caenorhabditis elegans) блокирование выработки естественной антиоксидантной супероксиддисмутазы увеличило продолжительность жизни.
В любом случае рекомендуется придерживаться здоровой диеты, не курить, ограничить потребление алкоголя, делать упражнения и избегать прямого воздействия солнечных лучей. Эти меры полезны для вашего здоровья в целом, а также могут замедлить выработку свободных радикалов.
Краткие выводы
-
Сегодня свободнорадикальная теория старения считается одной из фундаментальных.
-
Согласно этой теории, свободные радикалы — активные формы кислорода (АФК) — являются основной причиной старения, вызывая окислительные клеточные повреждения.

-
Свободные радикалы могут образовываться как в результате естественного процесса, так и вследствие диеты, стрессов, курения, алкоголя, физических упражнений или в результате воздействия солнца или загрязнения воздуха.
-
Повреждение клеток свободными радикалами называется окислительным (оксидативным) стрессом. Он вызывает старение, а также широкий спектр возрастных патологических процессов (сердечно-сосудистые заболевания, возрастная метаболическая иммунодепрессия, дисфункция мозга, катаракта, рак и т. Д.).
-
Некоторые исследования на примере дрожжей и дрозофил показали, что уменьшение окислительного повреждения может продлить продолжительность жизни.
-
В любом случае рекомендуется придерживаться здоровой диеты, не курить, ограничить потребление алкоголя, делать упражнения и избегать прямого воздействия солнечных лучей.

Получайте знания, основанные на доказательной медицине из первых уст ведущих мировых специалистов. В рамках Модульной Школы Anti-Age Expert каждый месяц проходят очные двухдневные семинары, где раскрываются тонкости anti-age медицины для врачей более 25 специальностей
Узнать подробнееСписок использованной литературы
-
Harman, Denham. «Free radical theory of aging.» Free Radicals: From Basic Science to Medicine. Birkhäuser Basel, 1993. 124–143.
-
Finkel, Toren, and Nikki J. Holbrook. «Oxidants, oxidative stress and the biology of ageing.» Nature 408.6809 (2000): 239–247.
-
Dai, Dao-Fu, et al. «Mitochondrial oxidative stress in aging and healthspan.» Longev Healthspan 3.6 (2014): 10–1186.
-
Stadtman, Earl R.
 «Protein oxidation and aging.» Free radical research 40.12 (2006): 1250–1258.
«Protein oxidation and aging.» Free radical research 40.12 (2006): 1250–1258.
-
Berlett, Barbara S., and Earl R. Stadtman. «Protein oxidation in aging, disease, and oxidative stress.» Journal of Biological Chemistry 272.33 (1997): 20313–20316.
Теории старения: окислительный стресс
Подробный материал опубликован в пятом номере журнала Les Nouvelles Esthétiques за 2017 год
В 2020 году только в России словосочетание «купить антиоксиданты» гуглили в интернете более полутора миллионов раз. То есть люди интересуются этой группой веществ, их ищут и заказывают косметические ингредиенты, подавляющие окислительный стресс и деятельность активных форм кислорода. Высокий спрос на антиоксиданты не удивляет: свободнорадикальная теория старения — одна из самых распространенных в биологии старения. Рассмотрим ее поближе.
Свободнорадикальная теория (или теория окислительного стресса) говорит о том, что между факторами агрессии и защиты клеток кожи возникает дисбаланс. Факторы агрессии — это активные формы кислорода, углерода, азота, в том числе нерадикальной природы. Большая часть свободных радикалов возникает как побочный продукт функционирования митохондрий. Но кроме того, радикалы в нормальных условиях образуются также в ходе многочисленных химических реакций, катализируемых оксидазами, что усиливает явления окислительного стресса.
Факторы агрессии — это активные формы кислорода, углерода, азота, в том числе нерадикальной природы. Большая часть свободных радикалов возникает как побочный продукт функционирования митохондрий. Но кроме того, радикалы в нормальных условиях образуются также в ходе многочисленных химических реакций, катализируемых оксидазами, что усиливает явления окислительного стресса.
Свободные радикалы: как они действуют?
Основы этой теории старения в 1956 году изложил американский биохимик Денхам Харман. В то время популярными были более сложные теории накопленных мутаций и повреждения белков. Биологи посчитали теорию американца слишком простой, для объяснения столь сложного процесса, как старение. Все изменилось в конце 60-х, когда появились данные о супероксиддисмутазе — ферменте организмов млекопитающих, который катализирует нейтрализацию высокотоксичных кислородных радикалов.
Свободные радикалы в первую очередь повреждают мембранные липиды, содержащие большое количество ненасыщенных жирных кислот. Под действием радикалов, липиды превращаются в токсичные пероксиды — один из компонентов морфологического маркера старения соматических клеток, известного как липофусцин. Этот пигмент отвечает за
появление возрастных пятен
Под действием радикалов, липиды превращаются в токсичные пероксиды — один из компонентов морфологического маркера старения соматических клеток, известного как липофусцин. Этот пигмент отвечает за
появление возрастных пятен
Другая мишень радикалов — ДНК. При ее повреждении образуется 8-окси-гуанозин, накопление которого с возрастом ассоциировано с возникновением «асоциальных», раковых клеток. Третью группу веществ, которую повреждают радикалы, составляют белки. Об этом наука узнала сравнительно недавно: лишь в 1988 году появился метод определения поврежденных белков по аминокислотам. Поскольку для всех трех компонентов характерны возраст-зависимые окислительные повреждения, то ученые предположили, что это и есть основа естественного старения организма.
Метаболические процессы и «скорость жизни»
Свободнорадикальная теория сподвигла немалое количество исследователей на изучение широкого спектра антиоксидантов и их возможностей: замедление старения, лечение возрастных заболеваний и увеличение продолжительности жизни. Но хотя эксперименты на животных показали хорошие результаты, исследования на организме человека разочаровали. Например, в 2007 году опубликовали итоги работы доктора Горана Бжелаковича: мета-анализ данных 232 606 человек показал достоверный рост смертности в случае длительного приема антиоксидантов (бета-каротина, витаминов A и E).
Но хотя эксперименты на животных показали хорошие результаты, исследования на организме человека разочаровали. Например, в 2007 году опубликовали итоги работы доктора Горана Бжелаковича: мета-анализ данных 232 606 человек показал достоверный рост смертности в случае длительного приема антиоксидантов (бета-каротина, витаминов A и E).
Повреждающим де йствием свободных радикалов пытались объяснить уже существовавшую в то время «теорию скорости жизни», которая говорила о наличии обратной зависимости между скоростью метаболических процессов и продолжительностью жизни. Предполагалось следующее: чем крупнее животное, тем выше удельная скорость его метаболических реакций — то есть и жить крупные животные должны больше.
Оказалось, однако, что к млекопитающим теория не применима. Исследование на мышах с гипер- и гипоактивностью антиоксидантных ферментных систем различий в продолжительности жизни не выявило. Более того, выяснилось, что мыши, потребляющие больше кислорода, живут дольше, что прямо противоречит теории.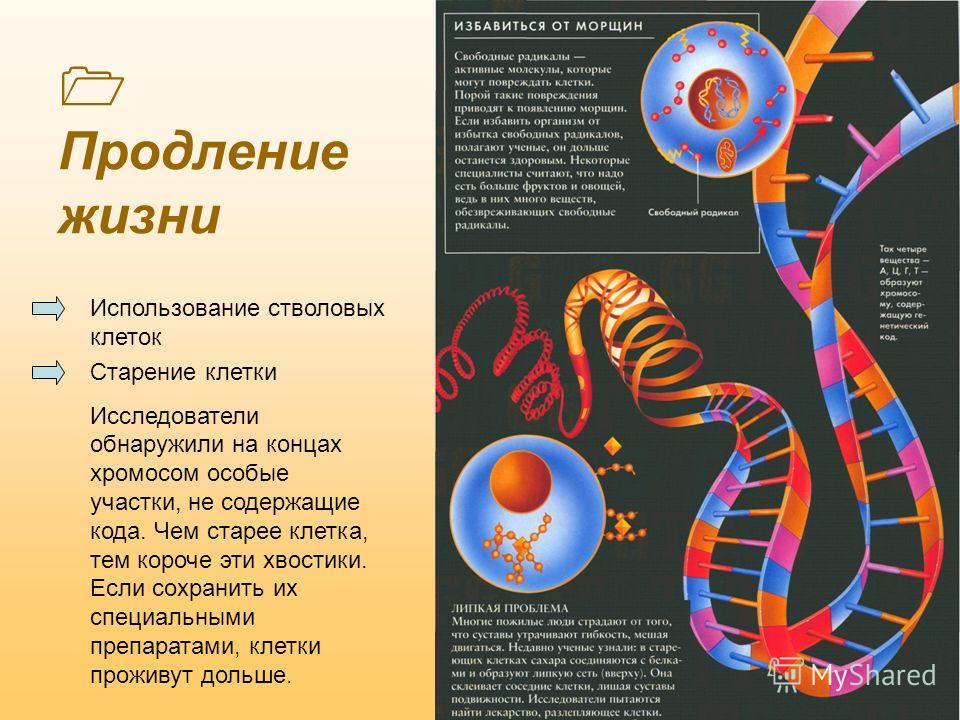
Перспективы теории в современной косметологии
Сегодня свободным радикалам по-прежнему, уделяют серьезное внимание, правда, не как повреждающим, а как
сигнальным молекулам
Ученые выяснили, что в малых дозах они играют горметическую роль, то есть оказывают умеренный стимулирующий эффект на организм. Так, у червей гиперболическая оксигенация повышает устойчивость к последующему воздействию сублетальных концентраций кислорода и продлевает жизнь. У возрастных мышей регулярные физические нагрузки уменьшают окислительное повреждение ДНК, липидов и белков за счет роста активности антиоксидантных
ферментов репарации ДНК
Показано, что прием антиоксидантов (витаминов C и E) на фоне физических упражнений устраняет позитивный эффект всех видов нагрузок. Таким образом, можно сделать вывод, что свободные радикалы, по всей видимости, не сокращают существенно продолжительность жизни, однако их кумулятивный эффект на физиологическое старение кожи доказан.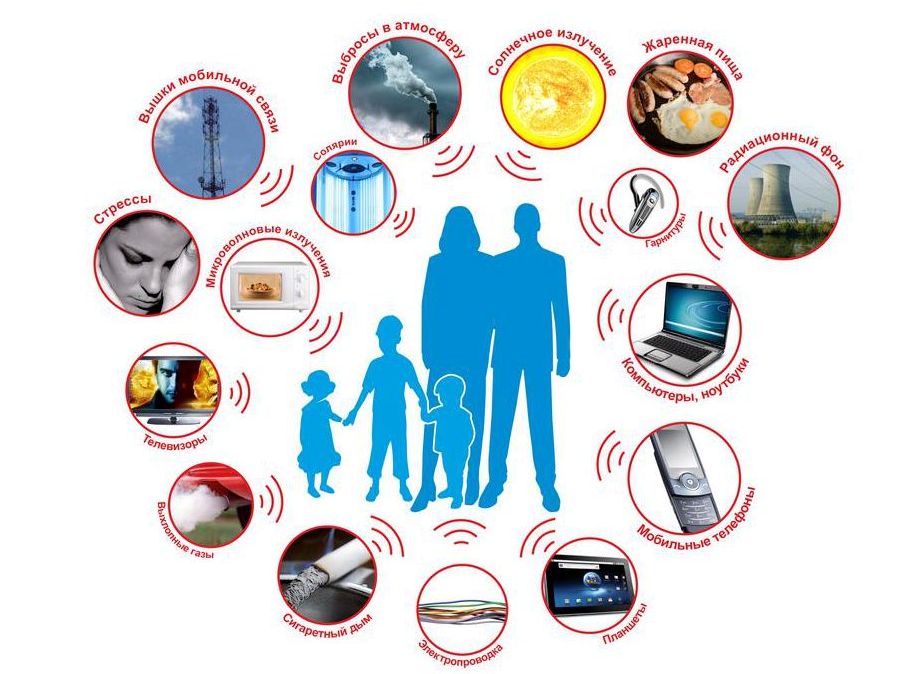 Поэтому для эффективного антивозрастного ухода за кожей не следует забывать о том, чтобы поддерживать
активацию собственных антиоксидантных систем клетки, а также механизмов защиты и репарации ДНК.
Поэтому для эффективного антивозрастного ухода за кожей не следует забывать о том, чтобы поддерживать
активацию собственных антиоксидантных систем клетки, а также механизмов защиты и репарации ДНК.
Свободнорадикальная теория старения мертва. Да здравствует теория повреждений!
- Список журналов
- Антиоксидный окислительно-восстановительный сигнал
- PMC33
Антиоксиданты и окислительно-восстановительный сигнал
Антиоксидный окислительно-восстановительный сигнал. 2014 1 февраля; 20(4): 727–731.
doi: 10.1089/ars.2013.5228
Информация об авторе Примечания к статье Информация об авторских правах и лицензиях Отказ от ответственности
Свободнорадикальная теория старения утверждает, что старение вызвано накоплением повреждений, вызванных активными формами кислорода (АФК). Хотя эта концепция оказалась очень полезной для определения вклада окислительного повреждения в процесс старения, все больше исследований противоречат ей. Представление о том, что окислительные повреждения представляют собой лишь одну из многих причин старения, также имеет ограничения, поскольку не объясняет причинно-следственных связей и неизбежности накопления повреждений. Здесь обсуждается, что неверность, неоднородность и несовершенство каждого биологического процесса могут быть причиной неизбежного накопления побочных продуктов и других форм повреждения. Хотя АФК являются прототипами побочных продуктов, их вклад в старение определяется метаболической организацией клетки, ее защитными системами и генотипом. Эти факторы контролируются естественным отбором и, подобно диетическим и генетическим вмешательствам, увеличивающим продолжительность жизни, изменяют состав кумулятивных повреждений и скорость накопления их различных форм. Окислительное повреждение, как и другие специфические типы повреждений, рассматриваемые по отдельности или в сочетании, не являются причиной старения.
Хотя эта концепция оказалась очень полезной для определения вклада окислительного повреждения в процесс старения, все больше исследований противоречат ей. Представление о том, что окислительные повреждения представляют собой лишь одну из многих причин старения, также имеет ограничения, поскольку не объясняет причинно-следственных связей и неизбежности накопления повреждений. Здесь обсуждается, что неверность, неоднородность и несовершенство каждого биологического процесса могут быть причиной неизбежного накопления побочных продуктов и других форм повреждения. Хотя АФК являются прототипами побочных продуктов, их вклад в старение определяется метаболической организацией клетки, ее защитными системами и генотипом. Эти факторы контролируются естественным отбором и, подобно диетическим и генетическим вмешательствам, увеличивающим продолжительность жизни, изменяют состав кумулятивных повреждений и скорость накопления их различных форм. Окислительное повреждение, как и другие специфические типы повреждений, рассматриваемые по отдельности или в сочетании, не являются причиной старения.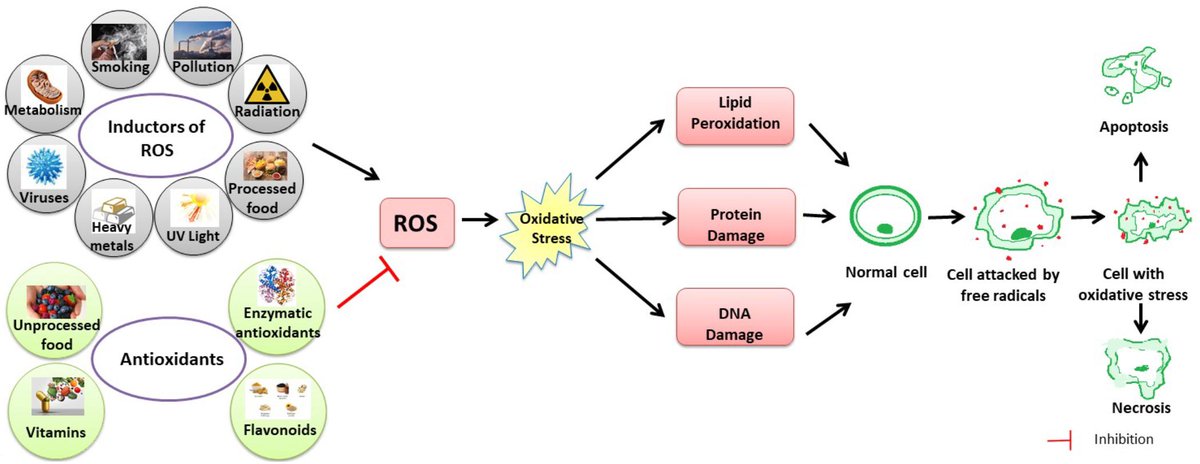 Вместо этого биологическое несовершенство, которое ведет к неизбежному накоплению повреждений в виде умеренно вредных молекулярных частиц, может помочь определить истинный корень старения. Свободнорадикальные и другие специализированные теории повреждения послужили своей цели в понимании процесса старения, но в нынешнем виде они ограничивают дальнейший прогресс в этой области. Антиоксидант. Окислительно-восстановительный сигнал. 20, 727–731.
Вместо этого биологическое несовершенство, которое ведет к неизбежному накоплению повреждений в виде умеренно вредных молекулярных частиц, может помочь определить истинный корень старения. Свободнорадикальные и другие специализированные теории повреждения послужили своей цели в понимании процесса старения, но в нынешнем виде они ограничивают дальнейший прогресс в этой области. Антиоксидант. Окислительно-восстановительный сигнал. 20, 727–731.
Свободнорадикальная теория старения (26) впервые была описана Денхамом Харманом в 1950-х годах (11). Он предполагает, что организмы стареют, потому что они накапливают окислительные повреждения. Это повреждение происходит из-за активных форм кислорода (АФК), которые представляют собой частично восстановленные метаболиты молекулярного кислорода, генерируемые как продукты метаболических реакций или как побочные продукты различных клеточных процессов, таких как дыхание. На протяжении многих лет и по сей день эта теория является самой популярной концепцией в области старения, и ежегодно публикуются тысячи публикаций. Многочисленные исследования показывают, что АФК и окислительные повреждения увеличиваются с возрастом (28) и что уменьшение окислительных повреждений увеличивает продолжительность жизни различных модельных организмов (дрожжей, нематод, плодовых мушек, мышей, 9).0019 и т.д. ), а также то, что повышенное производство АФК сокращает продолжительность жизни (16).
Многочисленные исследования показывают, что АФК и окислительные повреждения увеличиваются с возрастом (28) и что уменьшение окислительных повреждений увеличивает продолжительность жизни различных модельных организмов (дрожжей, нематод, плодовых мушек, мышей, 9).0019 и т.д. ), а также то, что повышенное производство АФК сокращает продолжительность жизни (16).
Доминирование свободнорадикальной теории почти не пострадало из-за растущего числа исследований, которые, по-видимому, противоречат ей (4, 6–8, 17, 18, 21, 23, 24, 27, 30, 31). Например, хотя в некоторых экспериментальных системах антиоксидантные белки продлевают жизнь, их сверхэкспрессия в других системах оказалась неэффективной (21). Эти результаты также сохраняются, когда система контролируется для соответствующей регуляции и уровней экспрессии этих белков (24). Повышенная антиоксидантная защита может даже привести к сокращению продолжительности жизни, тогда как снижение антиоксидантной функции может увеличить ее (31).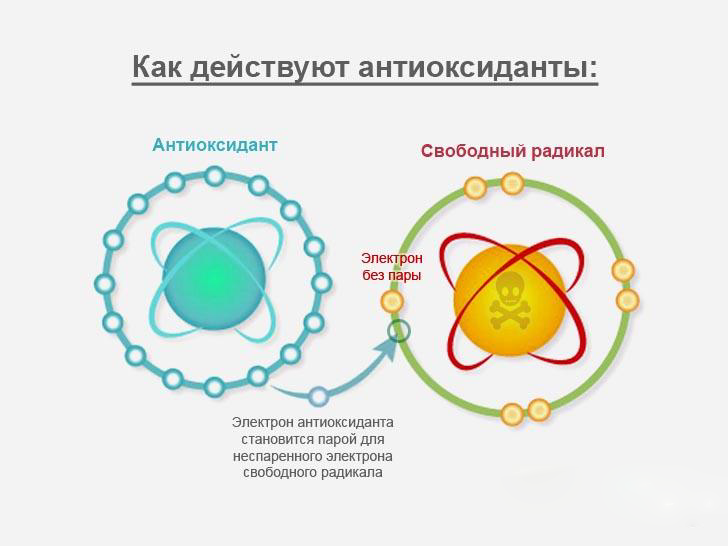 Против представления об универсальной роли АФК в процессе старения свидетельствует также наблюдение, что старение все же происходит в анаэробных условиях, где АФК мало. В частности, продолжительность жизни анаэробно выращенных дрожжевых клеток короче по сравнению с клетками, выращенными в аэробных условиях (а не дольше, как можно было бы ожидать, если АФК являются причиной старения), не регулируется антиоксидантными ферментами (тогда как эти ферменты могут регулировать его в аэробных условиях). , и дополнительно укорачивается (а не продлевается, как обычно наблюдается для этого режима питания) за счет ограничения калорийности (17).
Против представления об универсальной роли АФК в процессе старения свидетельствует также наблюдение, что старение все же происходит в анаэробных условиях, где АФК мало. В частности, продолжительность жизни анаэробно выращенных дрожжевых клеток короче по сравнению с клетками, выращенными в аэробных условиях (а не дольше, как можно было бы ожидать, если АФК являются причиной старения), не регулируется антиоксидантными ферментами (тогда как эти ферменты могут регулировать его в аэробных условиях). , и дополнительно укорачивается (а не продлевается, как обычно наблюдается для этого режима питания) за счет ограничения калорийности (17).
Чтобы согласовать теорию свободных радикалов с противоречащими ей наблюдениями, исследователи предположили, что АФК могут выполнять сигнальные функции, тем самым активируя защитные и адаптивные программы (25, 32). Также было предложено, что необходимо учитывать позиционные эффекты образования АФК и первичные мишени этих реактивных частиц (16). Действительно, если окислительный стресс возникает в локализованных областях клетки, анализ общего окислительного повреждения может не отражать фактическое повреждение, вызванное АФК. Хотя эти аргументы помогают устранить многие экспериментальные противоречия, остается много других вопросов. Например, эти аргументы не объясняют тот факт, что использование молекулярного кислорода, предшественника АФК, не всегда требуется для процесса старения. Однако эти аргументы могут даже не понадобиться, если окислительное повреждение рассматривать в контексте модели, рассматривающей старение как продукт биологического несовершенства, ведущего к неизбежному накоплению множества форм повреждения (см. ниже).
Хотя эти аргументы помогают устранить многие экспериментальные противоречия, остается много других вопросов. Например, эти аргументы не объясняют тот факт, что использование молекулярного кислорода, предшественника АФК, не всегда требуется для процесса старения. Однако эти аргументы могут даже не понадобиться, если окислительное повреждение рассматривать в контексте модели, рассматривающей старение как продукт биологического несовершенства, ведущего к неизбежному накоплению множества форм повреждения (см. ниже).
Окислительное повреждение привлекло большое внимание в области старения, поскольку его можно было контролировать с помощью установленных аналитических методов (28) и регулировать определенными ферментными системами (супероксиддисмутаза, каталаза, пероксиредоксин, глутатионпероксидаза, метионинсульфоксидредуктаза, и т. д. ). АФК непрерывно образуются в результате дыхания и других метаболических процессов, и их повреждающее действие легко понять с химической точки зрения.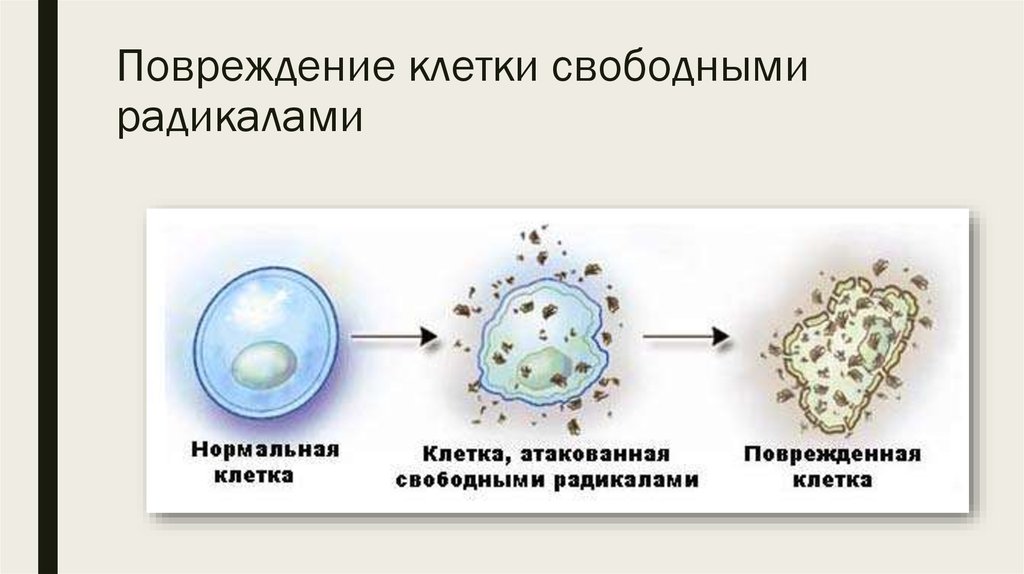 Молекулярный кислород является прототипом реактивного соединения, которое случайно реагирует с активными центрами различных ферментов, что приводит к частично восстановленным формам кислорода, АФК, которые повреждают клеточные биомолекулы (12). Однако нет оснований полагать, что какой-либо другой клеточный процесс не может генерировать побочные продукты. Многие побочные продукты ускользают от внимания исследователей, потому что экспериментальный анализ в основном сосредоточен на основных функциях белков, РНК и клеточных метаболитов, тогда как их косвенные функции редко исследуются. Тем не менее, имеется обширная литература по накоплению повреждений при старении, в которой рассматриваются процессы, выходящие за рамки окислительного повреждения (28). Это началось с идеи Оргеля об ошибках в транскрипции и трансляции, ведущих к катастрофе ошибок из-за ошибок в функции белка (22), и расширилось до других типов повреждений, включая повреждение ДНК, белков и метаболитов. Идея накопления повреждений как причинного фактора процесса старения в настоящее время поддерживается многими исследователями.
Молекулярный кислород является прототипом реактивного соединения, которое случайно реагирует с активными центрами различных ферментов, что приводит к частично восстановленным формам кислорода, АФК, которые повреждают клеточные биомолекулы (12). Однако нет оснований полагать, что какой-либо другой клеточный процесс не может генерировать побочные продукты. Многие побочные продукты ускользают от внимания исследователей, потому что экспериментальный анализ в основном сосредоточен на основных функциях белков, РНК и клеточных метаболитов, тогда как их косвенные функции редко исследуются. Тем не менее, имеется обширная литература по накоплению повреждений при старении, в которой рассматриваются процессы, выходящие за рамки окислительного повреждения (28). Это началось с идеи Оргеля об ошибках в транскрипции и трансляции, ведущих к катастрофе ошибок из-за ошибок в функции белка (22), и расширилось до других типов повреждений, включая повреждение ДНК, белков и метаболитов. Идея накопления повреждений как причинного фактора процесса старения в настоящее время поддерживается многими исследователями. Однако было неясно, каков фактический спектр повреждений в клетке и почему баланс между накоплением повреждений и устранением не может поддерживаться в организме с течением времени. Например, если супероксид-анион-радикал является повреждающим веществом, то почему клетки не удаляют его полностью с помощью супероксиддисмутазы или не уменьшают его образование в ходе метаболических процессов? Почему мозг, будучи высокоактивным метаболическим органом, имеет более низкую антиоксидантную защиту? Как можно сравнить влияние окислительного повреждения с повреждением от других процессов, таких как повреждение метаболитов, ошибки трансляции, гетерогенность транскрипции, неправильное нацеливание белков на клеточные компартменты и дисбаланс уровней взаимодействующих факторов?
Однако было неясно, каков фактический спектр повреждений в клетке и почему баланс между накоплением повреждений и устранением не может поддерживаться в организме с течением времени. Например, если супероксид-анион-радикал является повреждающим веществом, то почему клетки не удаляют его полностью с помощью супероксиддисмутазы или не уменьшают его образование в ходе метаболических процессов? Почему мозг, будучи высокоактивным метаболическим органом, имеет более низкую антиоксидантную защиту? Как можно сравнить влияние окислительного повреждения с повреждением от других процессов, таких как повреждение метаболитов, ошибки трансляции, гетерогенность транскрипции, неправильное нацеливание белков на клеточные компартменты и дисбаланс уровней взаимодействующих факторов?
Мы предполагаем, что все биомолекулы и биологические процессы несовершенны, что проявляется в непреднамеренных действиях и функциях. Таким образом, повреждения в виде побочных продуктов, всевозможных ошибок, дисбаланса клеточных компонентов и т.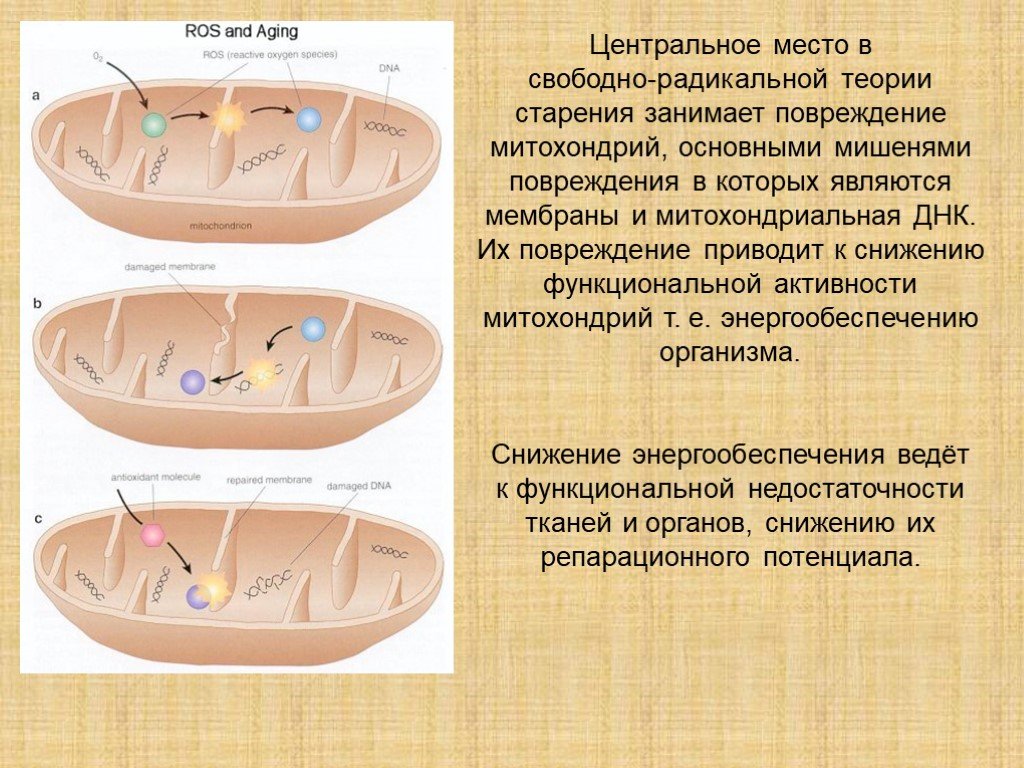 д. производятся каждым клеточным процессом (9, 10). Например, рассмотрим ферменты. Они обладают впечатляющей специфичностью, но не совершенны и генерируют незначительные продукты реакции и другие нежелательные побочные продукты (29, 20). Достоверность ферментов ограничена тем фактом, что они представляют собой гибкие полимеры, которые существуют в различных конформациях и состоят из ограниченного набора аминокислот и кофакторов. Он также подвергается риску из-за ошибок в последовательности и структуре белка, возникающих в результате ошибок в транскрипции, трансляции, фолдинге и посттрансляционных модификациях, мутаций и генетической изменчивости, а также других факторов. Другими словами, ни один фермент не совершенен, как бы хорошо ни был построен его активный центр за счет совместного действия его аминокислотных остатков и кофакторов. Помимо получения основного продукта из своего субстрата посредством своей прямой (эволюционирующей) функции, фермент производит немного чего-то еще и иногда реагирует с молекулами, отличными от своего природного субстрата, что является проявлением его непрямой (неэволюционирующей) функции.
д. производятся каждым клеточным процессом (9, 10). Например, рассмотрим ферменты. Они обладают впечатляющей специфичностью, но не совершенны и генерируют незначительные продукты реакции и другие нежелательные побочные продукты (29, 20). Достоверность ферментов ограничена тем фактом, что они представляют собой гибкие полимеры, которые существуют в различных конформациях и состоят из ограниченного набора аминокислот и кофакторов. Он также подвергается риску из-за ошибок в последовательности и структуре белка, возникающих в результате ошибок в транскрипции, трансляции, фолдинге и посттрансляционных модификациях, мутаций и генетической изменчивости, а также других факторов. Другими словами, ни один фермент не совершенен, как бы хорошо ни был построен его активный центр за счет совместного действия его аминокислотных остатков и кофакторов. Помимо получения основного продукта из своего субстрата посредством своей прямой (эволюционирующей) функции, фермент производит немного чего-то еще и иногда реагирует с молекулами, отличными от своего природного субстрата, что является проявлением его непрямой (неэволюционирующей) функции. Следует отметить, что такие побочные продукты в значительной степени не случайны. Они регулируются каталитическими свойствами каждого фермента; их химическая идентичность и скорость накопления могут меняться в процессе эволюции. Таким образом, ген, кодирующий фермент, кодирует как прямые, так и косвенные функции этого фермента, обе из которых контролируются генетически.
Следует отметить, что такие побочные продукты в значительной степени не случайны. Они регулируются каталитическими свойствами каждого фермента; их химическая идентичность и скорость накопления могут меняться в процессе эволюции. Таким образом, ген, кодирующий фермент, кодирует как прямые, так и косвенные функции этого фермента, обе из которых контролируются генетически.
Однако побочные продукты, образуемые ферментами, составляют лишь часть повреждений, вызываемых клетками, поскольку все другие клеточные компоненты и системы также несовершенны и гетерогенны. Можно ожидать, что каждая клеточная реакция и все макромолекулярные взаимодействия вызывают повреждение посредством косвенных функций биомолекул. В более широком смысле ущерб обязательно возникнет из-за несовершенства, неоднородности и шума биологических систем. Точно так же изменчивость в экспрессии генов и белков приведет к различиям между клетками, а также к различиям между отдельными организмами одного и того же вида. Многие минорные продукты клеточного метаболизма просто невозможно обнаружить, потому что не существует методов, позволяющих их анализировать, или потому, что анализируется усредненный сигнал. Концепция побочных продуктов каталитических реакций хорошо принята в химии, но биологи склонны действовать в терминах совершенных биологических систем, упуская из виду этот фундаментальный принцип. Биология увеличивает сложность, но ничего не исчезает из химии, когда дело доходит до биологии.
Концепция побочных продуктов каталитических реакций хорошо принята в химии, но биологи склонны действовать в терминах совершенных биологических систем, упуская из виду этот фундаментальный принцип. Биология увеличивает сложность, но ничего не исчезает из химии, когда дело доходит до биологии.
Клеточное повреждение, вызванное несовершенством, безусловно, включает окислительное повреждение. Однако последний, как и любая другая форма повреждения, будет представлять собой лишь часть общего повреждения, которое, независимо от его вклада в регуляцию продолжительности жизни, не будет иметь ничего общего с причиной старения (9, 10). Как клетка справляется с повреждением? Большая часть повреждений остается внутри пространства, окруженного клеточными и органеллыми мембранами. Многие клеточные побочные продукты, представляющие более серьезные повреждения и непосредственную опасность, могут быть устранены с помощью систем защиты и восстановления, которые метаболизируют или экспортируют повреждения из клетки.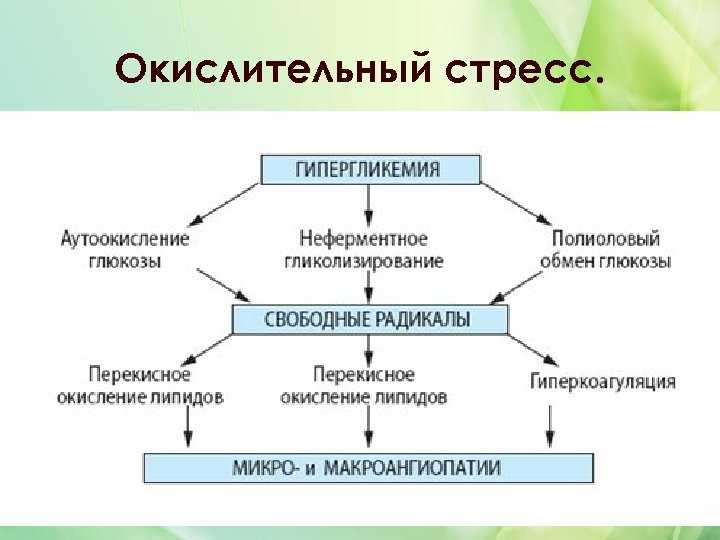 Существуют также родственные стратегии, такие как так называемые демоны Максвелла, которые представляют собой процессы, которые, порождая потомство изнутри старого ( напр. , процесс почкования у дрожжей) приводят к неравномерному распределению молекулярных повреждений между клетками (3). Однако, независимо от конкретных стратегий, помогающих устранить и перераспределить ущерб, количество форм ущерба всегда будет больше, чем количество защитных систем. Это связано с тем, что каждый биологический процесс создает повреждения, а системы очистки, удаляя определенные типы повреждений, создают другие типы повреждений. Таким образом, повреждение неизбежно будет накапливаться в клетке, если только клетка не делится, разбавляя свое повреждение. Рано или поздно, в зависимости от регуляции, навязанной естественным отбором, повреждения, накапливающиеся в постмитотических клетках, нарушат клеточную функцию, и клетка стареет и умирает. Неделящиеся клетки могут модулировать время до старения, изменяя свой метаболизм и избирательно используя назначенные защитные системы, но не могут полностью остановить процесс накопления повреждений и, следовательно, не могут избежать гибели клеток.
Существуют также родственные стратегии, такие как так называемые демоны Максвелла, которые представляют собой процессы, которые, порождая потомство изнутри старого ( напр. , процесс почкования у дрожжей) приводят к неравномерному распределению молекулярных повреждений между клетками (3). Однако, независимо от конкретных стратегий, помогающих устранить и перераспределить ущерб, количество форм ущерба всегда будет больше, чем количество защитных систем. Это связано с тем, что каждый биологический процесс создает повреждения, а системы очистки, удаляя определенные типы повреждений, создают другие типы повреждений. Таким образом, повреждение неизбежно будет накапливаться в клетке, если только клетка не делится, разбавляя свое повреждение. Рано или поздно, в зависимости от регуляции, навязанной естественным отбором, повреждения, накапливающиеся в постмитотических клетках, нарушат клеточную функцию, и клетка стареет и умирает. Неделящиеся клетки могут модулировать время до старения, изменяя свой метаболизм и избирательно используя назначенные защитные системы, но не могут полностью остановить процесс накопления повреждений и, следовательно, не могут избежать гибели клеток.
Поскольку окислительное повреждение представляет собой лишь часть общего повреждения, его поведение и влияние на клеточную функцию будут характеризовать кумулятивное повреждение при одних условиях, но не при других условиях. Следовательно, окислительное повреждение и связанные с ним системы клиренса могут регулировать продолжительность жизни, а могут и нет, в зависимости от вклада окислительного повреждения в общее повреждение. Можно ожидать значительной вариабельности роли окислительного повреждения при старении среди разных типов клеток, генотипов, метаболических состояний (9).0019 напр. , в зависимости от использования молекулярного кислорода), различных видов и различных условий окружающей среды. Эти соображения устраняют необходимость рассмотрения локализованных АФК или баланса между образованием и устранением окислительного повреждения, а также противоречивых данных о роли АФК и их клиренсе в регуляции продолжительности жизни. АФК могут просто не иметь отношения к старению при определенных условиях, таких как анаэробный рост, но могут иметь значение при других условиях, таких как гипоксия. Таким образом, вклад АФК будет в значительной степени зависеть от других процессов и будет зависеть от множества других факторов, регулирующих клеточную жизнь. Что еще более важно, ни АФК, ни какие-либо другие формы повреждения не представляют фактическую причину старения, поскольку основной причиной повреждения, которое не может быть полностью устранено, является биологическое несовершенство.
Таким образом, вклад АФК будет в значительной степени зависеть от других процессов и будет зависеть от множества других факторов, регулирующих клеточную жизнь. Что еще более важно, ни АФК, ни какие-либо другие формы повреждения не представляют фактическую причину старения, поскольку основной причиной повреждения, которое не может быть полностью устранено, является биологическое несовершенство.
Известно, что многие генетические манипуляции и условия питания увеличивают продолжительность жизни (2, 13, 14), что соответствует эволюционной основе процесса старения (15). Более того, вмешательства, которые приводят к увеличению продолжительности жизни одного организма, часто могут быть успешно применены к другим организмам. Например, ограничение калорийности или ингибирование функции мишени рапамицина (TOR) влияет на продолжительность жизни многих организмов. Считается, что эти эффекты увеличения продолжительности жизни модулируют скорость старения посредством гормезиса и других механизмов. В контексте данного обсуждения это будет означать, что эти методы лечения регулируют скорость накопления повреждений, воздействуя на молекулы, которые их вызывают. Однако формы накопленных повреждений также будут меняться в зависимости от метаболической организации клетки (1). На изменения условий окружающей среды, питательных веществ или других факторов клетка будет реагировать изменением своего метаболизма, сигнальных программ, экспрессии генов, и т.д. Новое метаболическое состояние будет сопровождаться новым ландшафтом накопления повреждений, то есть будут накапливаться разные формы повреждений, и скорость накопления общих повреждений также может быть разной. В то время как общий эффект лечения, увеличивающего продолжительность жизни, может заключаться в уменьшении кумулятивных повреждений, эти методы лечения будут делать это в основном за счет реструктуризации метаболизма, вызывая другой спектр повреждений, которые будут накапливаться с разной скоростью по сравнению с состоянием без лечения.
В контексте данного обсуждения это будет означать, что эти методы лечения регулируют скорость накопления повреждений, воздействуя на молекулы, которые их вызывают. Однако формы накопленных повреждений также будут меняться в зависимости от метаболической организации клетки (1). На изменения условий окружающей среды, питательных веществ или других факторов клетка будет реагировать изменением своего метаболизма, сигнальных программ, экспрессии генов, и т.д. Новое метаболическое состояние будет сопровождаться новым ландшафтом накопления повреждений, то есть будут накапливаться разные формы повреждений, и скорость накопления общих повреждений также может быть разной. В то время как общий эффект лечения, увеличивающего продолжительность жизни, может заключаться в уменьшении кумулятивных повреждений, эти методы лечения будут делать это в основном за счет реструктуризации метаболизма, вызывая другой спектр повреждений, которые будут накапливаться с разной скоростью по сравнению с состоянием без лечения.
Экспериментальные данные согласуются с этой идеей. Например, ограничение калорийности и дефицит TOR у дрожжей усиливают дыхание (5, 19). Хотя эти вмешательства могут увеличить АФК и некоторые формы окислительного повреждения, другие формы повреждения могут быть уменьшены. В более общем плане было бы недостаточно продемонстрировать уменьшение накопления какого-либо одного типа повреждения при определенном лечении, поскольку в этих условиях другие формы повреждения могут стать более распространенными или более значимыми для старения. Использование окислительного повреждения в качестве маркера кумулятивного повреждения может ввести в заблуждение при оценке старения и старения, хотя при некоторых условиях оно вполне может коррелировать с процессом старения.
Также важно отличать причину старения от контроля продолжительности жизни (9, 10). Естественный отбор может контролировать продолжительность жизни, влияя на скорость образования повреждений и скорость устранения их тяжелых форм, тем самым регулируя химическую идентичность различных форм повреждений и скорость их накопления.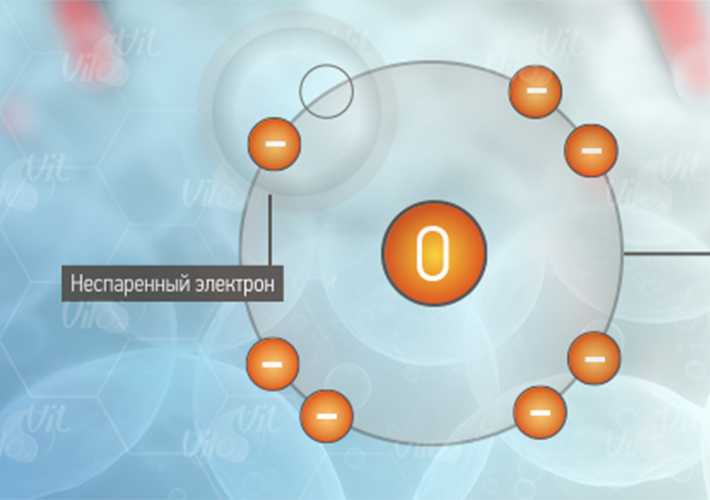 С другой стороны, несовершенство, неверность и неоднородность являются фундаментальными свойствами биологических систем. Их можно рассматривать как истинный корень старения. Таким образом, естественный отбор может замедлить или ускорить накопление повреждений и наступление перегрузок повреждений, но не может их остановить или отсрочить на неопределенное время. Мы не знаем пределов продления жизни, потому что в естественных условиях важнее способность передавать гены следующему поколению, чем достижение максимальной продолжительности жизни. Эти соображения не исключают возможности исключительной продолжительности жизни и даже бессмертия некоторых видов, способных постоянно расти или генерировать все свои соматические клетки из стволовых клеток. До тех пор, пока их клетки делятся, ослабляя легкие повреждения, или регенерируются, может быть достигнут баланс между образованием повреждений и устранением. Однако этого нельзя достичь у организмов с постмитотически необновляемыми клетками (9).
С другой стороны, несовершенство, неверность и неоднородность являются фундаментальными свойствами биологических систем. Их можно рассматривать как истинный корень старения. Таким образом, естественный отбор может замедлить или ускорить накопление повреждений и наступление перегрузок повреждений, но не может их остановить или отсрочить на неопределенное время. Мы не знаем пределов продления жизни, потому что в естественных условиях важнее способность передавать гены следующему поколению, чем достижение максимальной продолжительности жизни. Эти соображения не исключают возможности исключительной продолжительности жизни и даже бессмертия некоторых видов, способных постоянно расти или генерировать все свои соматические клетки из стволовых клеток. До тех пор, пока их клетки делятся, ослабляя легкие повреждения, или регенерируются, может быть достигнут баланс между образованием повреждений и устранением. Однако этого нельзя достичь у организмов с постмитотически необновляемыми клетками (9).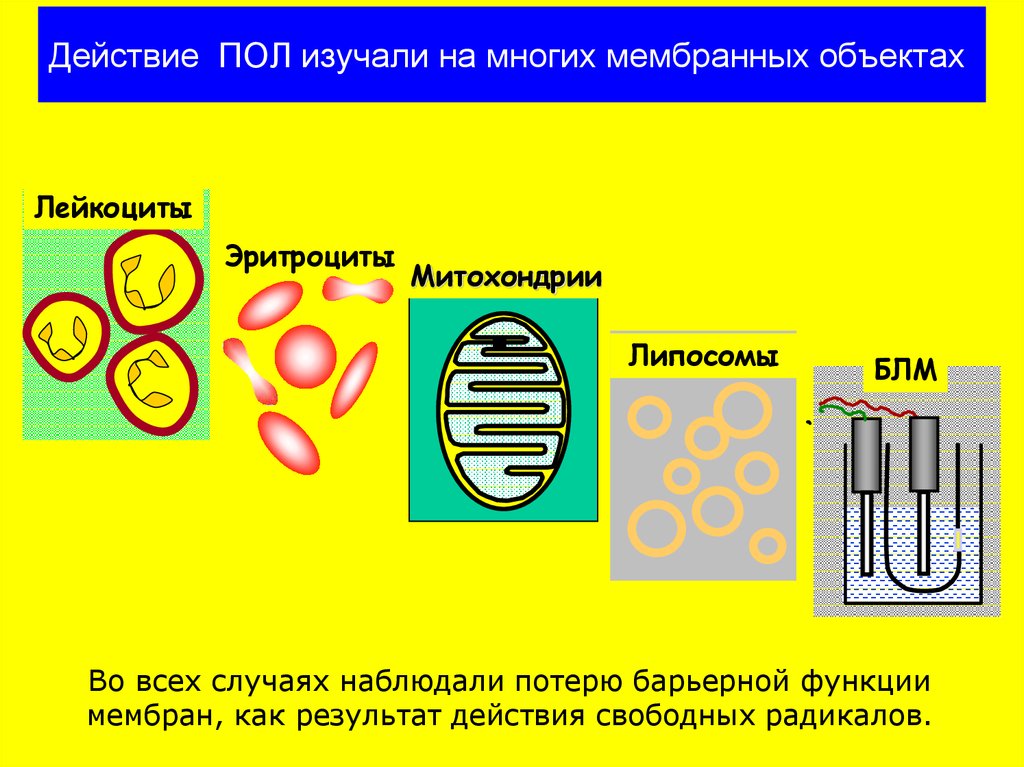 0019 напр. , у млекопитающих). Это также означает, что процесс старения возникал и исчезал много раз в ходе эволюции.
0019 напр. , у млекопитающих). Это также означает, что процесс старения возникал и исчезал много раз в ходе эволюции.
Свободнорадикальная теория старения согласуется с многочисленными исследованиями, но многие другие отчеты явно противоречат этой идее. В совокупности эти исследования выступают против универсальной роли окислительного повреждения в старении. По этой причине многие исследователи обратились к более широкой концепции, согласно которой многие формы повреждений служат причинными факторами в процессе старения, причем АФК представляют собой некоторые из основных причин, но не единственные. Хотя эта концепция привлекательна, сама по себе она имеет ограничения, поскольку не объясняет, почему клетки не могут поддерживать баланс между образованием и удалением повреждений. Хотя неизбежный характер накопления повреждений хорошо принят многими и даже рассматривается некоторыми исследователями как догма, на самом деле неясно, почему повреждения неизбежны. В данной статье рассматривается иная модель, рассматривающая биологическое несовершенство, проявляющееся в косвенных функциях биомолекул, как истинный корень старения.
Неоднородность, несовершенство и неверность биологических систем порождают повреждения от каждого биологического процесса и, следовательно, обязательно приводят к накоплению повреждений в постмитотических клетках. Этот ущерб, вызванный биологическим несовершенством, является следствием самой жизни и, в частности, присущей ей химии. Если клетки не делятся, чтобы уменьшить ущерб, накопление повреждений в конечном итоге приведет к старению клеток. Время для этого процесса будет зависеть прежде всего от метаболической организации клетки и ее генетической программы. По мере того, как назначенные системы защиты удаляют более серьезные повреждения, постепенно накапливаются легкие и легкие формы повреждений. Многие из этих форм повреждения не будут подвергаться естественному отбору, и против них не возникнет никаких систем защиты. Окислительное повреждение будет способствовать процессу старения только как часть общего повреждения. Это может быть более актуально для регулирования продолжительности жизни в одних условиях, но менее актуально в других условиях. Например, выращенные в анаэробных условиях дрожжевые клетки не генерируют значительных уровней АФК. Таким образом, эти виды, а также ферменты, защищающие от них, не играют существенной роли в этих условиях. Однако они делают это в условиях, утилизирующих кислород, например, при дыхании и гипоксии. Точно так же вклад окислительного повреждения в общее повреждение будет зависеть от типа клетки, вида, метаболического состояния клетки, питательных веществ, генотипа, и т.д. Таким образом, АФК, как и любая другая форма повреждения, могут влиять на продолжительность жизни, выступая медиаторами контроля продолжительности жизни, но фактической причиной старения является биологическая несовершенство. В первую очередь это причина повреждения, а огромное количество форм повреждения препятствует его устранению.
Например, выращенные в анаэробных условиях дрожжевые клетки не генерируют значительных уровней АФК. Таким образом, эти виды, а также ферменты, защищающие от них, не играют существенной роли в этих условиях. Однако они делают это в условиях, утилизирующих кислород, например, при дыхании и гипоксии. Точно так же вклад окислительного повреждения в общее повреждение будет зависеть от типа клетки, вида, метаболического состояния клетки, питательных веществ, генотипа, и т.д. Таким образом, АФК, как и любая другая форма повреждения, могут влиять на продолжительность жизни, выступая медиаторами контроля продолжительности жизни, но фактической причиной старения является биологическая несовершенство. В первую очередь это причина повреждения, а огромное количество форм повреждения препятствует его устранению.
Кроме того, любое возмущение клетки, которое изменяет продолжительность жизни, такое как вмешательство в диету, нокаут, нокдаун и принудительная сверхэкспрессия генов, обязательно повлияет на клеточный метаболизм, модулируя потоки через различные пути, такие как дыхание, гликолиз, метаболизм аминокислот и жирных кислот. а также механизмы клеточной регуляции. Такое метаболическое перепрограммирование будет характеризоваться различными метаболическими реакциями, которые будут генерировать различный спектр форм повреждения. Другими словами, некоторые формы повреждения будут одинаковыми, а некоторые будут разными в организме, подвергнутом вмешательству, продлевающему жизнь. Кроме того, метаболическое перепрограммирование приведет к накоплению повреждений с разной скоростью. Таким образом, стратегии увеличения продолжительности жизни действуют как за счет замедления накопления повреждений, так и за счет перевода клеточного метаболизма в состояние, при котором накапливаются различные формы повреждений. Эта концепция также применима к режимам питания, влияющим на продолжительность жизни, таким как ограничение калорий и лечение рапамицином. Например, было бы некорректно сравнивать окислительное повреждение при ad libitum и условиях ограничения калорийности и сделать вывод о вкладе окислительного повреждения в процесс старения, поскольку в этих условиях будут накапливаться различные формы повреждения.
а также механизмы клеточной регуляции. Такое метаболическое перепрограммирование будет характеризоваться различными метаболическими реакциями, которые будут генерировать различный спектр форм повреждения. Другими словами, некоторые формы повреждения будут одинаковыми, а некоторые будут разными в организме, подвергнутом вмешательству, продлевающему жизнь. Кроме того, метаболическое перепрограммирование приведет к накоплению повреждений с разной скоростью. Таким образом, стратегии увеличения продолжительности жизни действуют как за счет замедления накопления повреждений, так и за счет перевода клеточного метаболизма в состояние, при котором накапливаются различные формы повреждений. Эта концепция также применима к режимам питания, влияющим на продолжительность жизни, таким как ограничение калорий и лечение рапамицином. Например, было бы некорректно сравнивать окислительное повреждение при ad libitum и условиях ограничения калорийности и сделать вывод о вкладе окислительного повреждения в процесс старения, поскольку в этих условиях будут накапливаться различные формы повреждения. Что следует сравнивать, так это кумулятивный ущерб, а также его вклад в нарушение клеточного гомеостаза.
Что следует сравнивать, так это кумулятивный ущерб, а также его вклад в нарушение клеточного гомеостаза.
Только недавно были разработаны экспериментальные инструменты, такие как чувствительные, высокопроизводительные методы секвенирования, протеомики и профилирования метаболитов, которые можно использовать для начала оценки бесчисленных форм повреждений, возникающих в клетке. С помощью этих инструментов можно определить основные свойства клеточного повреждения, такие как химическая идентичность, количество, скорость накопления и синхронизация. Это непросто, поскольку может потребоваться провести различие, например, между метаболитами и побочными продуктами метаболизма и показать причинную роль несовершенства. Многие отдельные формы легких повреждений вносят незначительный вклад в общий ущерб, поэтому удаление любой из них может не повлиять на продолжительность жизни или физическую форму.
В качестве прототипа концепции старения свободнорадикальная теория старения послужила своей цели для развития нашего понимания старения, сначала как отдельная идея, а затем как концепция о том, что окислительное повреждение представляет собой одну из многих причин старения. Эта теория предложила экспериментально проверяемые гипотезы и внесла значительный вклад в наше современное понимание старения. Однако дальнейшие исследования выявили его слабые стороны, с которыми невозможно смириться, даже если окислительное повреждение рассматривать как компонент кумулятивного повреждения или одну из многих причин старения. Конечно, окислительные повреждения могут усиливаться с возрастом, а антиоксидантные ферменты могут защищать при некоторых условиях, но сосредоточение внимания на этих наблюдениях отвлекает от изучения истинной причины старения. Пришло время сделать вывод, что окислительная (свободнорадикальная) теория старения ограничивает дальнейшее понимание процесса старения.
Эта теория предложила экспериментально проверяемые гипотезы и внесла значительный вклад в наше современное понимание старения. Однако дальнейшие исследования выявили его слабые стороны, с которыми невозможно смириться, даже если окислительное повреждение рассматривать как компонент кумулятивного повреждения или одну из многих причин старения. Конечно, окислительные повреждения могут усиливаться с возрастом, а антиоксидантные ферменты могут защищать при некоторых условиях, но сосредоточение внимания на этих наблюдениях отвлекает от изучения истинной причины старения. Пришло время сделать вывод, что окислительная (свободнорадикальная) теория старения ограничивает дальнейшее понимание процесса старения.
| АФК | активные формы кислорода |
| TOR | мишень рапамицина |

 Barzilai N, Guarente L, Kirkwood TB, Partridge L, Rando TA и Slagboom PE. Место генетики в исследование старения. Нат Рев Генет 13: 589–594, 2012 [PubMed] [Google Scholar]
Barzilai N, Guarente L, Kirkwood TB, Partridge L, Rando TA и Slagboom PE. Место генетики в исследование старения. Нат Рев Генет 13: 589–594, 2012 [PubMed] [Google Scholar] Free Radic Biol Med 51: 1575–1582, 2011 [бесплатная статья PMC] [PubMed] [Google Scholar]
Free Radic Biol Med 51: 1575–1582, 2011 [бесплатная статья PMC] [PubMed] [Google Scholar] Trends Genet 29: 506–512, 2013 [бесплатная статья PMC] [PubMed] [Google Scholar]
Trends Genet 29: 506–512, 2013 [бесплатная статья PMC] [PubMed] [Google Scholar]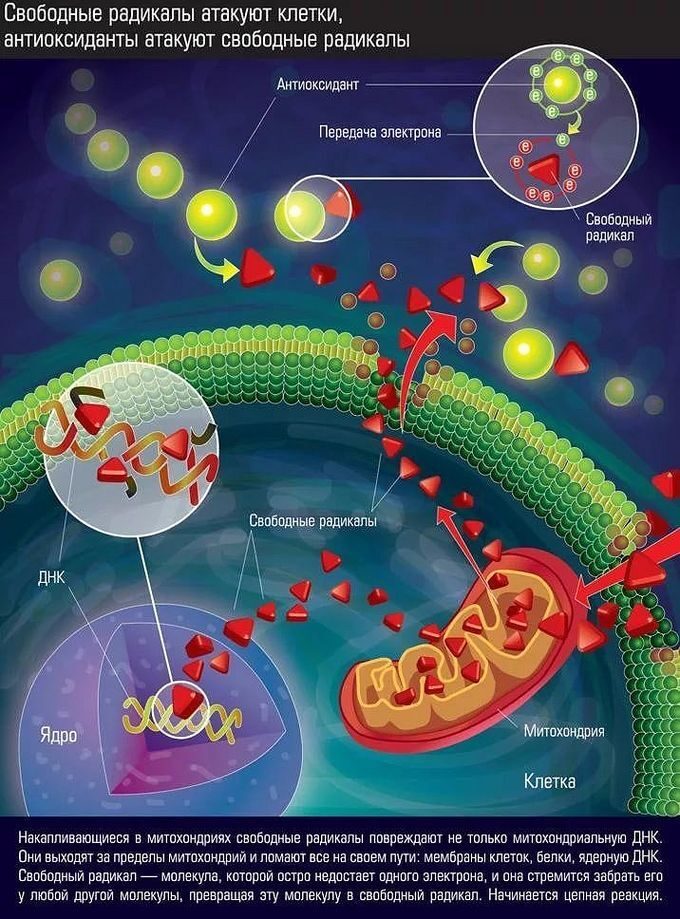 Регуляция продолжительности жизни дрожжей метионинсульфоксидредуктазой выявляет активные формы кислорода и — самостоятельные компоненты старения. Proc Natl Acad Sci USA 101: 7999–8004, 2004 [бесплатная статья PMC] [PubMed] [Google Scholar]
Регуляция продолжительности жизни дрожжей метионинсульфоксидредуктазой выявляет активные формы кислорода и — самостоятельные компоненты старения. Proc Natl Acad Sci USA 101: 7999–8004, 2004 [бесплатная статья PMC] [PubMed] [Google Scholar]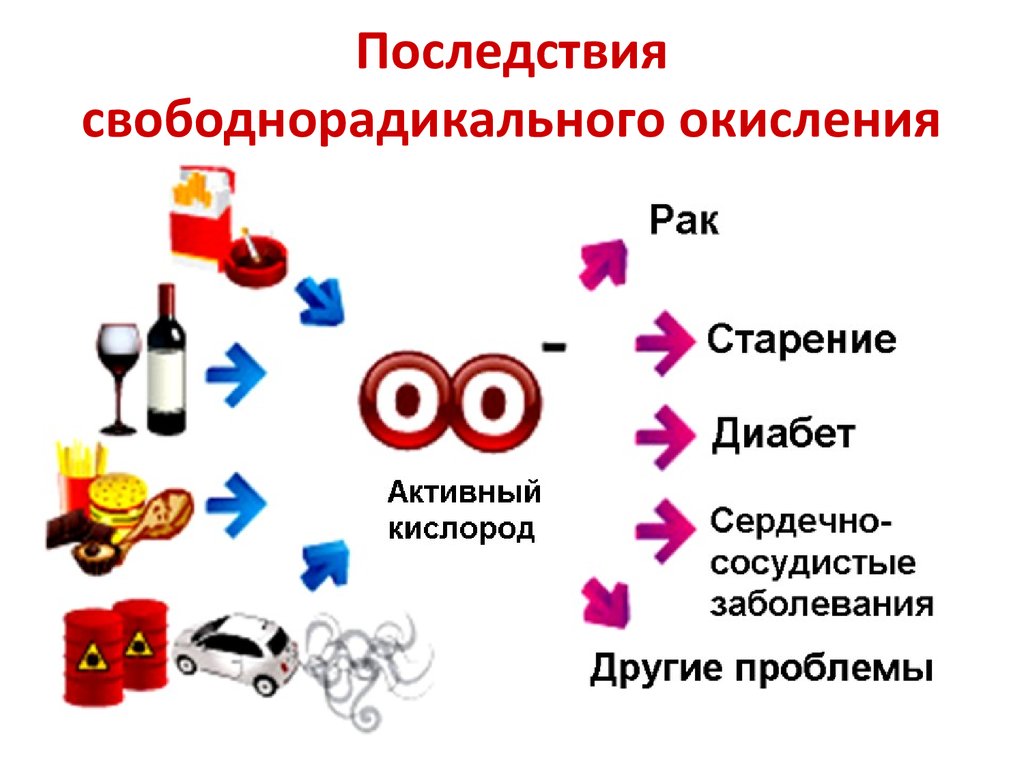 меланогастр . Free Radic Biol Med 49: 2028–2031, 2010 [бесплатная статья PMC] [PubMed] [Google Scholar]
меланогастр . Free Radic Biol Med 49: 2028–2031, 2010 [бесплатная статья PMC] [PubMed] [Google Scholar] Speakman JR. и Selman C. Теория повреждения свободными радикалами: накопление доказательств против простой связи окислительного стресса со старением и продолжительностью жизни. Bioessays 33: 255–259, 2011 [PubMed] [Google Scholar]
Speakman JR. и Selman C. Теория повреждения свободными радикалами: накопление доказательств против простой связи окислительного стресса со старением и продолжительностью жизни. Bioessays 33: 255–259, 2011 [PubMed] [Google Scholar]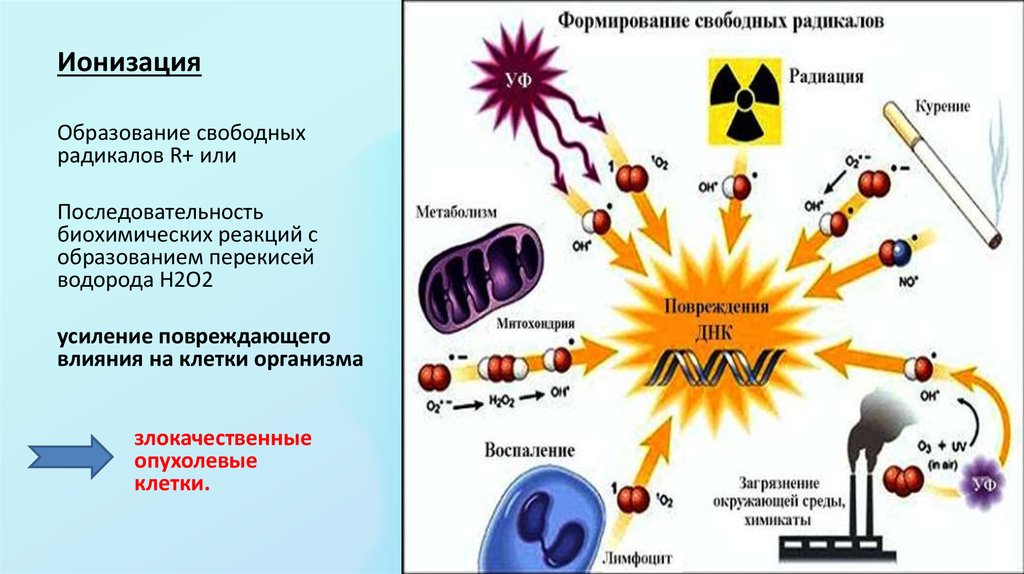 Нарушение инсулина/ Передача сигналов IGF1 продлевает продолжительность жизни, способствуя митохондриальному катаболизму L-пролина, чтобы вызвать временный сигнал ROS. Cell Metab 15: 451–465, 2012 [бесплатная статья PMC] [PubMed] [Google Scholar]
Нарушение инсулина/ Передача сигналов IGF1 продлевает продолжительность жизни, способствуя митохондриальному катаболизму L-пролина, чтобы вызвать временный сигнал ROS. Cell Metab 15: 451–465, 2012 [бесплатная статья PMC] [PubMed] [Google Scholar] 5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
 Теория свободных радикалов также может быть использована для объяснения многих структурных особенностей, которые развиваются при старении, включая перекисное окисление липидов мембран, образование возрастных пигментов, перекрестное связывание белков, повреждение ДНК и снижение функции митохондрий. Несмотря на это, остается много неясностей относительно роли окислительного повреждения в старении, и нельзя исключать альтернативные объяснения. Свободные радикалы встречаются только в следовых количествах в биологических тканях, их клеточные уровни и действие невозможно измерить in vivo, а окончательные доказательства того, что окисленные молекулы являются основной причиной старения, отсутствуют. Кроме того, старение также, вероятно, является многофакторным процессом и не может быть сведено к какой-либо одной причине. Таким образом, несмотря на свои положительные черты, доказательства свободнорадикальной теории либо коррелируют, либо неубедительны.
Теория свободных радикалов также может быть использована для объяснения многих структурных особенностей, которые развиваются при старении, включая перекисное окисление липидов мембран, образование возрастных пигментов, перекрестное связывание белков, повреждение ДНК и снижение функции митохондрий. Несмотря на это, остается много неясностей относительно роли окислительного повреждения в старении, и нельзя исключать альтернативные объяснения. Свободные радикалы встречаются только в следовых количествах в биологических тканях, их клеточные уровни и действие невозможно измерить in vivo, а окончательные доказательства того, что окисленные молекулы являются основной причиной старения, отсутствуют. Кроме того, старение также, вероятно, является многофакторным процессом и не может быть сведено к какой-либо одной причине. Таким образом, несмотря на свои положительные черты, доказательства свободнорадикальной теории либо коррелируют, либо неубедительны.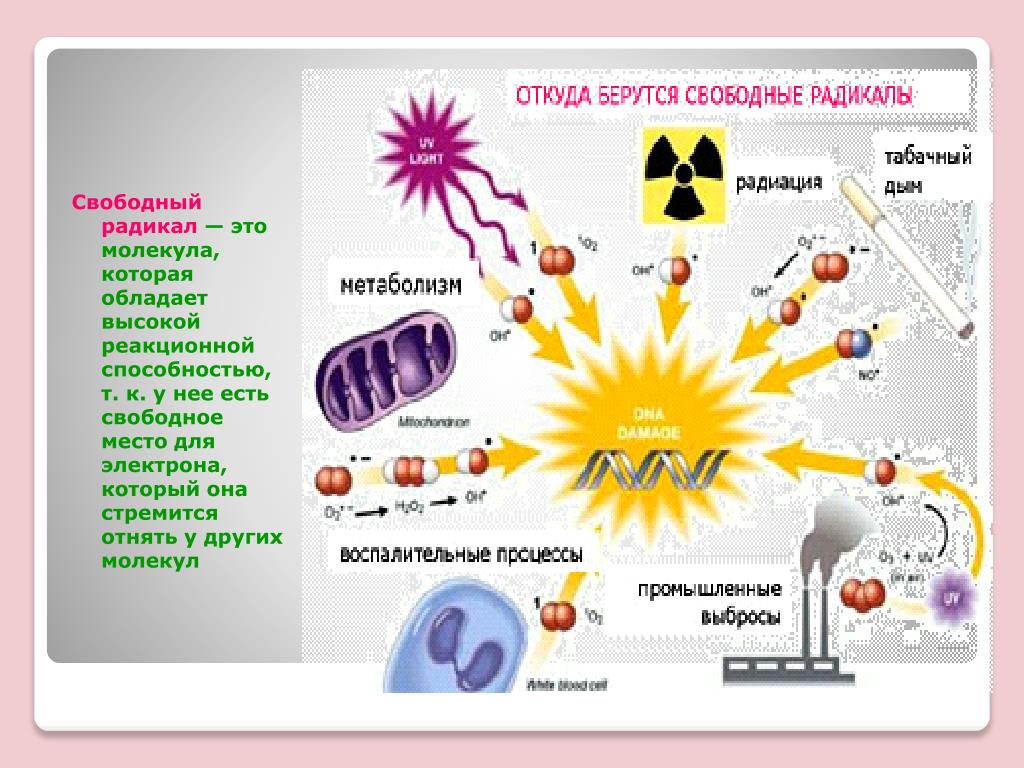
 2002.
PMID: 12142953
Обзор.
2002.
PMID: 12142953
Обзор. PMID: 36983497
Бесплатная статья ЧВК.
PMID: 36983497
Бесплатная статья ЧВК.