Что такое крем Эмла и для чего он применяется. Как правильно использовать крем Эмла. Какие побочные эффекты может вызвать крем Эмла. Когда нельзя применять крем Эмла. На что обратить внимание при использовании крема Эмла.
Что такое крем Эмла
Эмла — это местноанестезирующий крем, содержащий комбинацию двух действующих веществ: лидокаина и прилокаина. Оба компонента относятся к группе местных анестетиков амидного типа. Крем Эмла обеспечивает поверхностную анестезию кожи и слизистых оболочек за счет проникновения лидокаина и прилокаина в эпидермис и дерму.
Фармакологические свойства
Основной механизм действия крема Эмла заключается в блокаде нервных окончаний в коже и слизистых оболочках. Это приводит к временному прекращению проведения болевых импульсов в месте нанесения крема. Степень и длительность анестезии зависят от времени аппликации и дозы препарата.
После нанесения крема Эмла на неповрежденную кожу на 1-2 часа, анестезирующий эффект сохраняется около 2 часов после удаления окклюзионной повязки. При нанесении на слизистые оболочки половых органов обезболивающее действие наступает быстрее — через 5-10 минут, и длится 15-20 минут (в некоторых случаях до 45 минут).

Крем Эмла также оказывает влияние на поверхностные кровеносные сосуды, вызывая их временное сужение или расширение. Это может проявляться побледнением или покраснением кожи в месте нанесения.
Показания к применению
Крем Эмла применяется в следующих случаях:
- Поверхностная анестезия кожи перед проведением инъекций, пункций, катетеризации сосудов и других малых хирургических вмешательств
- Обезболивание при хирургической обработке трофических язв нижних конечностей
- Поверхностная анестезия слизистой оболочки половых органов перед малыми гинекологическими процедурами
- Обезболивание кожи перед косметологическими процедурами (эпиляция, удаление татуировок и др.)
Способ применения и дозы
Применение у взрослых
При нанесении на неповрежденную кожу рекомендуемые дозы и время аппликации:
- Для введения игл (катетеризация, забор крови): 2 г крема на 10 см², время аппликации 1 час (максимум 5 часов)
- Для небольших процедур на коже (удаление бородавок и др.): 1,5-2 г на 10 см², время аппликации 1 час (максимум 5 часов)
- Для процедур на больших участках кожи: 1,5-2 г на 10 см², время аппликации 2 часа (максимум 5 часов)
При обработке трофических язв: 1-2 г крема на 10 см² поверхности язвы, но не более 10 г на одну процедуру. Время аппликации 30 минут, при необходимости до 60 минут.

Для анестезии слизистой оболочки половых органов: 5-10 г крема на всю обрабатываемую поверхность. Время аппликации 5-10 минут.
Применение у детей
Дозы для детей зависят от возраста:
- 0-3 месяца: максимум 1 г на 10 см², время аппликации 1 час
- 3-12 месяцев: максимум 2 г на 20 см², время аппликации 1 час
- 1-6 лет: максимум 10 г на 100 см², время аппликации 1-5 часов
- 6-12 лет: максимум 20 г на 200 см², время аппликации 1-5 часов
Детям с атопическим дерматитом рекомендуется уменьшить время аппликации до 30 минут.
Противопоказания
Крем Эмла противопоказан в следующих случаях:
- Повышенная чувствительность к лидокаину, прилокаину или другим местным анестетикам амидного типа
- Аллергия на любой компонент препарата
- Нарушение целостности кожи в месте нанесения (активный опоясывающий герпес, атопический дерматит, раны)
- Врожденная или приобретенная метгемоглобинемия
- Недоношенные дети (родившиеся ранее 37 недели беременности)
Побочные эффекты
При применении крема Эмла возможны следующие побочные реакции:

Часто (более 1% случаев):
- Временные местные реакции в месте нанесения: побледнение, покраснение, отек кожи
Нечасто (0,1-1% случаев):
- Кожные высыпания
- Легкая боль, жжение или зуд в месте нанесения
- Аллергический контактный дерматит
- Крапивница
Редко (менее 0,1% случаев):
- Аллергические реакции, в тяжелых случаях анафилактический шок
- Метгемоглобинемия у детей
При случайном попадании крема в глаза возможно раздражение роговицы.
Особые указания и меры предосторожности
При использовании крема Эмла следует соблюдать следующие меры предосторожности:
- С осторожностью применять у пациентов с недостаточностью глюкозо-6-фосфатдегидрогеназы из-за риска развития метгемоглобинемии
- Избегать попадания крема в глаза и на поврежденные участки кожи
- Соблюдать осторожность при нанесении на большие участки кожи, особенно у пациентов с нарушениями функции печени, почек или сердечно-сосудистой системы
- Не наносить на поврежденную барабанную перепонку
- Не применять на слизистые оболочки половых органов у детей
- Соблюдать осторожность при применении перед вакцинацией (особенно БЦЖ) из-за возможного влияния на эффективность вакцины
Взаимодействие с другими препаратами
Крем Эмла может взаимодействовать со следующими препаратами:

- Метгемоглобинобразующие препараты (сульфаниламиды и др.) — повышается риск метгемоглобинемии
- Антиаритмические препараты классов I и III — возможно усиление побочных эффектов
- Ингибиторы МАО — усиливают местноанестезирующее действие лидокаина
Необходимо соблюдать осторожность при одновременном применении крема Эмла с указанными препаратами.
Передозировка
При соблюдении рекомендуемых доз риск передозировки низкий. Однако при нанесении крема на большие участки кожи или слизистых оболочек возможно развитие системных токсических эффектов.
Симптомы передозировки могут включать:
- Со стороны ЦНС: возбуждение, головокружение, судороги, угнетение сознания
- Со стороны сердечно-сосудистой системы: снижение АД, брадикардия, аритмия
- Метгемоглобинемия (особенно у детей)
При появлении симптомов передозировки необходимо прекратить применение препарата и обратиться за медицинской помощью. Лечение симптоматическое, при тяжелых неврологических симптомах может потребоваться ИВЛ и противосудорожная терапия.

Фармакокинетика
Всасывание и распределение действующих веществ крема Эмла зависит от места нанесения, дозы и времени аппликации:
- При нанесении на неповрежденную кожу системная абсорбция составляет около 3% для лидокаина и 5% для прилокаина
- Максимальная концентрация в плазме достигается через 2-4 часа после нанесения
- При нанесении на слизистые оболочки всасывание происходит быстрее — максимальная концентрация достигается через 20-45 минут
- Объем распределения лидокаина — 1,1-2,1 л/кг, прилокаина — 0,7-4,4 л/кг
- Связывание с белками плазмы: лидокаин — 65%, прилокаин — 55%
Метаболизм лидокаина и прилокаина происходит преимущественно в печени. Основные метаболиты — 2,6-ксилидин (лидокаин) и ортотолуидин (прилокаин). Период полувыведения лидокаина составляет 1,5-2 часа, прилокаина — около 1,5 часов.
Условия хранения и срок годности
Крем Эмла следует хранить при температуре не выше 30°C, не замораживать. Срок годности — 3 года. После вскрытия тубы оставшийся крем следует утилизировать.

Форма выпуска
Крем Эмла выпускается в тубах по 5 г и 30 г. В комплект входят окклюзионные наклейки для нанесения на кожу.
Производитель
Крем Эмла производится компанией Aspen Pharma Trading Limited (Ирландия).
Часто задаваемые вопросы
Можно ли использовать крем Эмла во время беременности?
Применение крема Эмла при беременности возможно, но только по назначению врача после оценки соотношения польза/риск. Лидокаин и прилокаин проникают через плацентарный барьер, однако тератогенного действия в исследованиях не выявлено.
Безопасно ли применение крема Эмла у детей?
Крем Эмла разрешен к применению у детей с рождения, но с соблюдением возрастных дозировок. Не рекомендуется использовать у недоношенных детей. У новорожденных и детей до 3 месяцев повышен риск метгемоглобинемии, поэтому требуется особая осторожность.
Сколько времени действует обезболивающий эффект крема Эмла?
Длительность анестезии зависит от места нанесения. На неповрежденной коже эффект сохраняется около 2 часов после удаления крема. На слизистых оболочках действие более кратковременное — 15-45 минут.

Можно ли использовать крем Эмла перед татуировкой?
Эмла: инструкция, цена, аналоги | крем Aspen Pharma Trading
- Фармакологические свойства
- Показания Эмла
- Применение Эмла
- Противопоказания
- Побочные эффекты
- Особые указания
- Взаимодействия
- Передозировка
- Условия хранения
- Диагнозы
- Рекомендуемые аналоги
- Торговые наименования
крем Эмла содержит лидокаин и прилокаин — местные анестетики амидного типа. За счет проникновения лидокаина и прилокаина в слои эпидермиса и дермы происходит обезболивание кожи. Степень анестезии зависит от времени аппликации и дозы.
Неповрежденная кожа. При нанесении крема Эмла на неповрежденную кожу на 1–2 ч анестезия длится около 2 ч после снятия окклюзионной наклейки. Отличий в эффективности (включая время достижения обезболивающего эффекта) и безопасности при нанесении на неповрежденную кожу между пациентами молодого и пожилого возраста не выявлено.
За счет влияния крема на поверхностные сосуды возможно временное побледнение или покраснение участка кожи. Подобные реакции развиваются быстрее (уже через 30–60 мин после нанесения крема) у пациентов с распространенным нейродермитом (атопическим нейродермитом), что свидетельствует о более быстром проникновении крема через измененную кожу.
Репродуктивная токсичность
Лидокаин. В исследованиях влияния на эмбриональное/фетальное развитие, в рамках которого крысам и кроликам лекарственное средство применяли в период органогенеза, не наблюдалось тератогенных эффектов. Токсическое воздействие на эмбрион отмечалось у кроликов при применении лекарственного средства в токсических для материнского организма дозах. Для потомства крыс, которое подвергалось воздействию токсических для материнского организма доз на поздних стадиях беременности и в период кормления грудью, характерным было снижение показателя постнатальной выживаемости.
Прилокаин. Исследования репродуктивной токсичности прилокаина не завершены.
В исследовании комбинации, в рамках которого прилокаин и лидокаин применяли у беременных крыс в период органогенеза, не выявлено влияния на эмбриональное/фетальное развитие. Однако данных о системном воздействии и клиническом значении последнего недостаточно.
Генотоксичность и канцерогенность
Лидокаин. Исследования генотоксичности лидокаина дали отрицательные результаты. Канцерогенность лидокаина не изучали. Метаболит лидокаина 2,6-ксилидин обладает генотоксическим потенциалом in vitro. В исследовании канцерогенности 2,6-ксилидина у крыс in utero, постнатально и в течение жизни было зарегистрировано образование опухолей в носовой полости, гиподерме и печени. Клиническое значение развития опухолей при кратковременном/нерегулярном применении лидокаина неизвестно.
Прилокаин. Исследования генотоксичности прилокаина дали отрицательные результаты. Канцерогенность прилокаина не изучали. Метаболит прилокаина ортотолуидин обладает генотоксическим потенциалом in vitro. В исследовании канцерогенности ортотолуидина у крыс, мышей и хомяков было зарегистрировано образование опухолей в различных органах. Клиническое значение развития опухолей при кратковременном/нерегулярном применении прилокаина неизвестно.
В исследовании канцерогенности ортотолуидина у крыс, мышей и хомяков было зарегистрировано образование опухолей в различных органах. Клиническое значение развития опухолей при кратковременном/нерегулярном применении прилокаина неизвестно.
Препарат Эмла одинаково эффективен независимо от цвета/пигментации кожи (типы кожи I–VI).
Препарат Эмла может быть применен перед подкожной или внутримышечной вакцинацией. Относительно внутрикожной вакцинации живой вакциной, например БЦЖ, см. ПРИМЕНЕНИЕ.
Слизистая оболочка половых органов. Анестезирующий эффект слизистой оболочки проявляется раньше, поскольку абсорбция происходит быстрее, чем в случаях нанесения на неповрежденную кожу.
У женщин после нанесения крема Эмла на слизистую оболочку половых органов через 5–10 мин достигается обезболивающий эффект, достаточный для проведения манипуляций с применением аргонового лазера. Продолжительность анестезии составляет 15–20 мин (с учетом индивидуальных особенностей — 5–45 мин).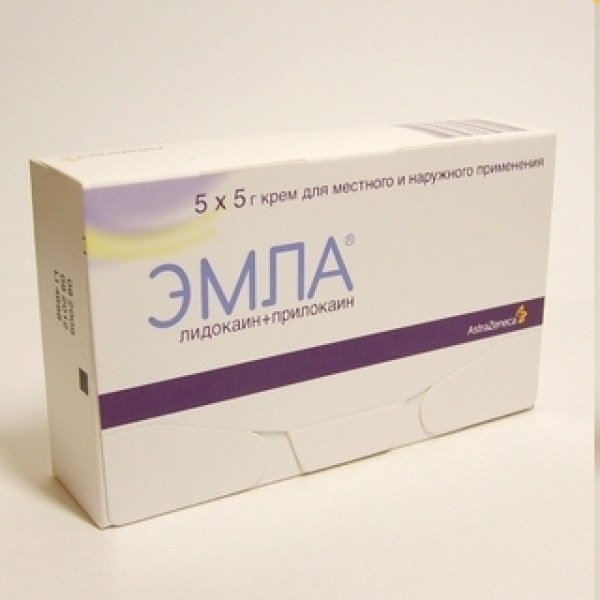
Трофические язвы нижних конечностей. После нанесения крема при обработке трофических язв нижних конечностей длительность обезболивающего эффекта составляет около 4 ч. Крем не оказывает отрицательного влияния на процесс заживления ран и бактериальную флору.
Системная абсорбция зависит от количества крема, продолжительности аппликации, толщины кожи (которая варьирует на разных участках тела) и других особенностей кожи.
Неповрежденная кожа. У взрослых после нанесения 60 г крема Эмла на неповрежденную кожу бедра площадью 400 см2 (1,5 г на 10 см2) за 3 ч системная абсорбция составляла 3% для лидокаина и 5% для прилокаина. Абсорбция происходит медленно. При указанной выше дозе Сmax в плазме крови лидокаина (в среднем — 0,12 мкг/мл) и прилокаина (в среднем — 0,07 мкг/мл) достигалась приблизительно через 4 ч после аппликации. Риск развития токсических симптомов существует лишь при уровне 5–10 мкг/мл.
Трофические язвы нижних конечностей. После нанесения на трофические язвы 5–10 г крема Эмла с экспозицией 30 мин Cmax лидокаина и прилокаина в плазме крови достигались приблизительно через 1–2,5 ч (концентрация лидокаина в пределах 0,05–0,84 мкг/мл, прилокаина — 0,02–0,08 мкг/мл).
После нанесения на трофические язвы 5–10 г крема Эмла с экспозицией 30 мин Cmax лидокаина и прилокаина в плазме крови достигались приблизительно через 1–2,5 ч (концентрация лидокаина в пределах 0,05–0,84 мкг/мл, прилокаина — 0,02–0,08 мкг/мл).
После повторного нанесения крема Эмла на трофические язвы сколько-нибудь значимого накопления лидокаина, прилокаина или их метаболитов в плазме крови не отмечали (крем Эмла наносили по 2–10 г на 30–60 мин на участок площадью в пределах 62 см2 15 раз в месяц по 3–7 сеансов в неделю).
Слизистая оболочка половых органов. Сmax в плазме крови достигается приблизительно через 35 мин после нанесения 10 г крема Эмла на слизистую оболочку влагалища с экспозицией 10 мин (в среднем концентрация лидокаина составляла 0,18 мкг/мл; прилокаина — 0,15 мкг/мл).
поверхностная анестезия кожи при проведении пункций, катетеризации сосудов и поверхностных хирургических вмешательств.
Поверхностная анестезия трофических язв нижних конечностей при хирургической обработке (механическом очищении), например для удаления фибрина, гноя и некротических тканей.
Поверхностная анестезия слизистой оболочки половых органов.
взрослые
| Неповрежденная кожа | Доза и применение | Продолжительность аппликации |
|---|---|---|
| При введении игл, например для катетеризации сосудов или забора образцов крови | ½ объема тубы (около 2 г) на 10 см2. Толстый слой крема нанести на кожу и прикрыть окклюзионной наклейкой | 1 ч; максимум 5 ч |
| При проведении небольших хирургических процедур на поверхности кожи, например удаление бородавок | 1,5–2 г на 10 см2. Толстый слой крема нанести на кожу и прикрыть окклюзионной наклейкой | 1 ч; максимум 5 ч |
| При проведении хирургических процедур на больших площадях поверхности кожи, например взятие кожи методом расщепленного лоскута | 1,5–2 г на 10 см2. Толстый слой крема нанести на кожу и прикрыть окклюзионной наклейкой | 2 ч; максимум 5 ч |
Трофические язвы нижних конечностей. При хирургической обработке (механическом очищении) трофических язв нанести 1–2 г крема на 10 см2 поверхности. Крем наносят толстым слоем на поверхность язвы, не более 10 г крема на одну процедуру. Прикрыть поверхность язвы окклюзионной наклейкой. Продолжительность аппликации крема 30 мин.
При хирургической обработке (механическом очищении) трофических язв нанести 1–2 г крема на 10 см2 поверхности. Крем наносят толстым слоем на поверхность язвы, не более 10 г крема на одну процедуру. Прикрыть поверхность язвы окклюзионной наклейкой. Продолжительность аппликации крема 30 мин.
Открытая туба предназначена для одноразового использования, после каждой процедуры неиспользованный крем выбрасывают.
При обработке язв, в ткани которых проникновение препарата затруднено, продолжительность аппликации можно увеличить до 60 мин. Хирургическую обработку раневой поверхности следует начинать не позже 10 мин после удаления крема.
При лечении трофических язв нижних конечностей крем Эмла применяют до 15 раз в течение 1–2 мес без снижения эффективности и повышения частоты развития местных реакций.
Поверхностная анестезия половых органов
Кожа половых органов. Применение перед инъекцией местных анестетиков:
- мужчины: 1 г на 10 см2.
 Толстый слой крема наносят на кожу. Продолжительность аппликации — 15 мин;
Толстый слой крема наносят на кожу. Продолжительность аппликации — 15 мин; - женщины: 1–2 г на 10 см2. Толстый слой крема наносят на кожу. Продолжительность аппликации — 60 мин.
Слизистая оболочка половых органов. Для удаления кондилом или перед инъекцией местных анестетиков: 5–10 г крема в зависимости от площади лечения наносят на всю поверхность, включая складки слизистой оболочки. Окклюзионной наклейки не требуется. Продолжительность аппликации — 5–10 мин. Хирургическую процедуру следует начинать сразу после удаления крема.
Дети
При проведении инъекций, удалении контагиозных моллюсков и других незначительных поверхностных хирургических манипуляциях: 1 г на 10 см2 поверхности, толстым слоем крем наносят на поверхность кожи и прикрывают окклюзионной наклейкой. Доза не должна превышать 1 г на 10 см2, ее следует корригировать в зависимости от площади нанесения.
| Возраст | Площадь нанесения | Продолжительность аппликации |
|---|---|---|
| 0–3 мес | Максимум 10 см2 (всего 1 г) (максимальная суточная доза) | 1 ч (примечание: не дольше) |
| 3–12 мес | Максимум 20 см2 (всего 2 г) | 1 ч |
| 1 год–6 лет | Максимум 100 см2 (всего 10 г) | 1 ч; максимум 5 ч |
| 6–12 лет | Максимум 200 см2 (всего 20 г) | 1 ч; максимум 5 ч |
Детям при атопическом дерматите необходимо уменьшить продолжительность аппликации до 30 мин.
Рекомендации относительно способа применения. Запаянную мембрану тубы проколоть шипом, находящимся в верхней внешней части крышки. Выдавить необходимое количество крема и нанести на место проведения процедуры. При обезболивании кожи применяют окклюзионные наклейки, входящие в комплект с кремом (12 шт. размером 6х7 см).
нарушение целостности кожи в месте нанесения крема (активный опоясывающий герпес, атопический дерматит или раны).
Гиперчувствительность к местным анестетикам амидного типа или любому вспомогательному веществу (например бупивакаин, этидокаин, мепивакаин).
Крем Эмла не применяют у недоношенных грудных детей (родившихся раньше полных 37 нед беременности).
истинные побочные реакции, вызванные применением местных анестетиков, возникают с частотой 1/1000 пациентов.
| Часто (>1/100) | Кожа: временные местные кожные реакции в месте нанесения, например местное побледнение, покраснение, отек |
| Нечасто (1/100–1/1000) | Кожа: после нанесения кожные высыпания, легкая боль, жжение или зуд в месте нанесения, аллергический контактный дерматит, крапивница, ангионевротический отек |
| Редко (<1/1000) | Общие: аллергические реакции, в наиболее тяжелых случаях анафилактический шок. Метгемоглобинемия у детей Метгемоглобинемия у детей |
Сообщалось об отдельных случаях местных реакций на участке нанесения крема, таких как геморрагические высыпания или петехии, особенно после длительной аппликации у детей с атопическим дерматитом или бородавками. При случайном попадании препарата в глаза может возникнуть раздражение роговицы.
пациенты с недостаточностью глюкозо-6-фосфат-дегидрогеназы, врожденной или идиопатической метгемоглобинемией более склонны к развитию препаратзависимой метгемоглобинемии.
Крем Эмла следует с осторожностью применять на коже в области глаз, поскольку препарат раздражает их слизистую оболочку. Кроме того, потеря защитных рефлексов вследствие попадания на роговицу анестетика может привести к раздражению и повреждению роговицы. При попадании крема Эмла в глаза их следует немедленно промыть водой или физиологическим р-ром (натрия хлорида) и защищать до восстановления чувствительности роговицы.
Препарат необходимо с осторожностью применять у пациентов с местной инфекцией в области применения, при травме в месте применения и при острых заболеваниях, у ослабленных больных, пациентов пожилого возраста, пациентов с тяжелой сердечной, почечной или печеночной недостаточностью.
Если во время применения препарата возникает ощущение жжения или покраснение кожи, ее необходимо промыть водой и прекратить применение, пока не исчезнет покраснение.
Эффективность применения крема у новорожденных при взятии крови из пятки не установлена.
Безопасность и эффективность применения препарата у детей в возрасте младше 3 мес исследовали лишь при применении разовой дозы. У таких детей после нанесения крема часто отмечают временное повышение уровня метгемоглобина в крови продолжительностью до 13 ч. Тем не менее этот факт, вероятно, не имеет клинического значения.
Крем Эмла нельзя наносить на поврежденную барабанную перепонку и не следует применять в ситуациях, когда препарат может проникнуть в полость среднего уха.
Крем Эмла не следует наносить на открытые раны.
Препарат не следует наносить на слизистую оболочку половых органов у детей в связи с недостаточностью данных относительно абсорбции.
При концентрации, превышающей 0,5–2,0%, лидокаин и прилокаин проявляют бактерицидные и противовирусные свойства. Поэтому в случае применения препарата при проведении вакцинации (внутрикожное введение живой вакцины, например БЦЖ) необходимо тщательное наблюдение. Не следует применять крем Эмла у детей в возрасте от 0 до 12 мес, получающих сопутствующую терапию препаратами, индуцирующими метгемоглобинемию, в связи с отсутствием достаточного клинического опыта применения.
Поэтому в случае применения препарата при проведении вакцинации (внутрикожное введение живой вакцины, например БЦЖ) необходимо тщательное наблюдение. Не следует применять крем Эмла у детей в возрасте от 0 до 12 мес, получающих сопутствующую терапию препаратами, индуцирующими метгемоглобинемию, в связи с отсутствием достаточного клинического опыта применения.
Необходимо вести наблюдение пациентов, получающих антиаритмические препараты, относящиеся к классу III (например амиодарон), учитывать результаты ЭКГ у таких пациентов, поскольку лидокаин и антиаритмические препараты класса III могут оказывать аддитивное действие.
Период беременности и кормления грудью. Данные относительно лечения кремом Эмла беременных недостаточны. Лидокаин и прилокаин проникают через плацентарный барьер и могут абсорбироваться эмбриональными тканями.
Сообщений о нарушении репродуктивного процесса, например повышении частоты пороков развития, прямого или косвенного влияния на плод, не было. Однако, применяя препарат в период беременности, необходимо анализировать соотношение польза/риск.
Однако, применяя препарат в период беременности, необходимо анализировать соотношение польза/риск.
Лидокаин и, вероятно, прилокаин, проникают в грудное молоко, но в таком малом количестве, что влияние терапевтических доз препарата на ребенка маловероятно.
Дети. Крем Эмла не следует применять у недоношенных детей грудного возраста (родившимся раньше 37 полных недель беременности).
Схему применения препарата у детей в зависимости от возраста см. в разделе ПРИМЕНЕНИЕ.
Не влияет на способность к управлению транспортными средствами и работе с другими механизмами.
Эмла может повышать образование метгемоглобина у пациентов, получающих лечение метгемоглобининдуцирующими препаратами (например сульфонамидами). При применении крема Эмла в высоких дозах у больных, получающих местные анестетики или препараты, структурно подобные местным анестетикам, например токаинид, необходимо учитывать риск системных аддитивных эффектов.
Абсорбция лидокаина через кожу обычно низкая, однако необходимо с осторожностью применять лидокаин у больных, которые принимают антиаритмические препараты І класса (токаинид, мексилетин) или другие местные анестетики, поскольку возможен риск возникновения суммарных системных эффектов. Ингибиторы МАО усиливают местноанальгезирующее действие лидокаина.
Ингибиторы МАО усиливают местноанальгезирующее действие лидокаина.
Специфических исследований взаимодействия препарата с местными анестетиками и антиаритмическими средствами, относящимися к классу III, не проводили, поэтому при их одновременном применении рекомендуется соблюдать осторожность.
при соблюдении рекомендуемого режима дозирования препарата развитие системной токсичности маловероятно. Вероятные симптомы интоксикации такие же, как и при применении других местных анестетиков: например, возбуждение ЦНС, в тяжелых случаях — угнетение ЦНС и сердечной деятельности.
Возможны повышенное потоотделение, бледность кожных покровов, головокружение, головная боль, нечеткость зрительного восприятия, шум в ушах, диплопия, снижение АД, брадикардия, аритмия, сонливость, озноб, онемение конечностей, беспокойство, судороги, шок, остановка сердца.
Очень редко сообщалось о случаях клинически значимой метгемоглобинемии у детей, поскольку прилокаин в высоких дозах может повышать уровень метгемоглобина.
Поверхностное применение 125 мг прилокаина продолжительностью 5 ч явилось причиной развития умеренной метгемоглобинемии у трехмесячного ребенка. Местное применение лидокаина 8,6–17,2 мг/кг массы тела привело к развитию тяжелой интоксикации у детей грудного возраста.
Выраженные неврологические симптомы (судороги, угнетение ЦНС) требуют симптоматического лечения: применения ИВЛ и противосудорожных препаратов. Антидотом при метгемоглобинемии является метилтионин. Вследствие медленной системной абсорбции препарата за состоянием пациента необходимо наблюдение еще в течение нескольких часов после устранения симптомов интоксикации.
С появлением первых признаков интоксикации (головокружение, тошнота, рвота, эйфория) перевести пациента в горизонтальное положение, назначить ингаляцию кислорода, при брадикардии — блокаторы М-холинорецепторов (атропин), вазоконстрикторы (норэпинефрин, фенилэфрин).
при температуре ниже 30 °С, не замораживать.
Эмла: инструкция, цена, аналоги | крем Aspen Pharma Trading
- schema.org/SiteNavigationElement»>
- Фармакологические свойства
- Показания Эмла
- Применение Эмла
- Противопоказания
- Побочные эффекты
- Особые указания
- Взаимодействия
- Передозировка
- Условия хранения
- Диагнозы
- Рекомендуемые аналоги
- Торговые наименования
крем Эмла содержит лидокаин и прилокаин — местные анестетики амидного типа. За счет проникновения лидокаина и прилокаина в слои эпидермиса и дермы происходит обезболивание кожи. Степень анестезии зависит от времени аппликации и дозы.
Неповрежденная кожа. При нанесении крема Эмла на неповрежденную кожу на 1–2 ч анестезия длится около 2 ч после снятия окклюзионной наклейки. Отличий в эффективности (включая время достижения обезболивающего эффекта) и безопасности при нанесении на неповрежденную кожу между пациентами молодого и пожилого возраста не выявлено.
За счет влияния крема на поверхностные сосуды возможно временное побледнение или покраснение участка кожи. Подобные реакции развиваются быстрее (уже через 30–60 мин после нанесения крема) у пациентов с распространенным нейродермитом (атопическим нейродермитом), что свидетельствует о более быстром проникновении крема через измененную кожу.
Подобные реакции развиваются быстрее (уже через 30–60 мин после нанесения крема) у пациентов с распространенным нейродермитом (атопическим нейродермитом), что свидетельствует о более быстром проникновении крема через измененную кожу.
Репродуктивная токсичность
Лидокаин. В исследованиях влияния на эмбриональное/фетальное развитие, в рамках которого крысам и кроликам лекарственное средство применяли в период органогенеза, не наблюдалось тератогенных эффектов. Токсическое воздействие на эмбрион отмечалось у кроликов при применении лекарственного средства в токсических для материнского организма дозах. Для потомства крыс, которое подвергалось воздействию токсических для материнского организма доз на поздних стадиях беременности и в период кормления грудью, характерным было снижение показателя постнатальной выживаемости.
Прилокаин. Исследования репродуктивной токсичности прилокаина не завершены.
В исследовании комбинации, в рамках которого прилокаин и лидокаин применяли у беременных крыс в период органогенеза, не выявлено влияния на эмбриональное/фетальное развитие. Однако данных о системном воздействии и клиническом значении последнего недостаточно.
Однако данных о системном воздействии и клиническом значении последнего недостаточно.
Генотоксичность и канцерогенность
Лидокаин. Исследования генотоксичности лидокаина дали отрицательные результаты. Канцерогенность лидокаина не изучали. Метаболит лидокаина 2,6-ксилидин обладает генотоксическим потенциалом in vitro. В исследовании канцерогенности 2,6-ксилидина у крыс in utero, постнатально и в течение жизни было зарегистрировано образование опухолей в носовой полости, гиподерме и печени. Клиническое значение развития опухолей при кратковременном/нерегулярном применении лидокаина неизвестно.
Прилокаин. Исследования генотоксичности прилокаина дали отрицательные результаты. Канцерогенность прилокаина не изучали. Метаболит прилокаина ортотолуидин обладает генотоксическим потенциалом in vitro. В исследовании канцерогенности ортотолуидина у крыс, мышей и хомяков было зарегистрировано образование опухолей в различных органах. Клиническое значение развития опухолей при кратковременном/нерегулярном применении прилокаина неизвестно.
Клиническое значение развития опухолей при кратковременном/нерегулярном применении прилокаина неизвестно.
Препарат Эмла одинаково эффективен независимо от цвета/пигментации кожи (типы кожи I–VI).
Препарат Эмла может быть применен перед подкожной или внутримышечной вакцинацией. Относительно внутрикожной вакцинации живой вакциной, например БЦЖ, см. ПРИМЕНЕНИЕ.
Слизистая оболочка половых органов. Анестезирующий эффект слизистой оболочки проявляется раньше, поскольку абсорбция происходит быстрее, чем в случаях нанесения на неповрежденную кожу.
У женщин после нанесения крема Эмла на слизистую оболочку половых органов через 5–10 мин достигается обезболивающий эффект, достаточный для проведения манипуляций с применением аргонового лазера. Продолжительность анестезии составляет 15–20 мин (с учетом индивидуальных особенностей — 5–45 мин).
Трофические язвы нижних конечностей. После нанесения крема при обработке трофических язв нижних конечностей длительность обезболивающего эффекта составляет около 4 ч.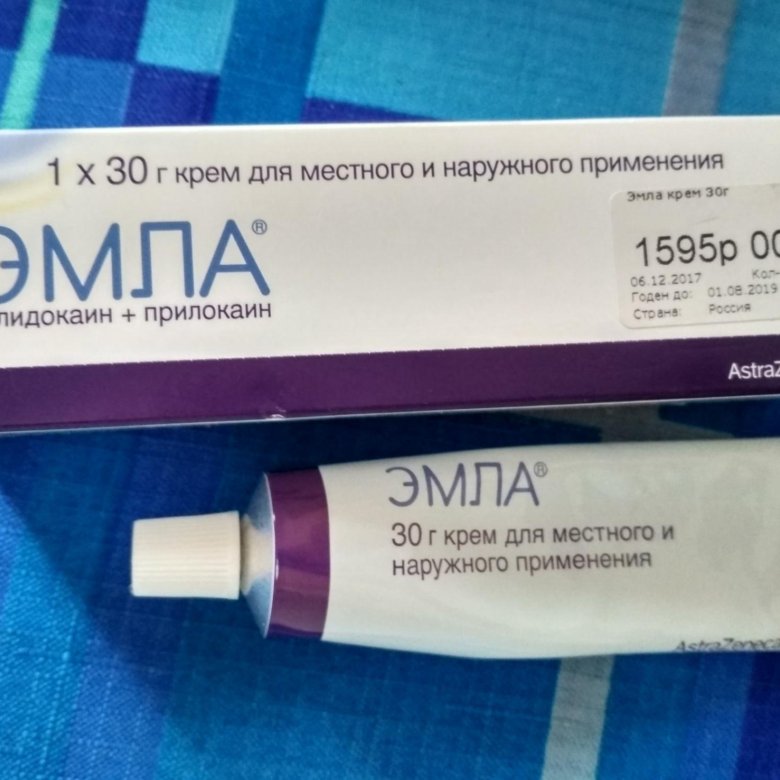 Крем не оказывает отрицательного влияния на процесс заживления ран и бактериальную флору.
Крем не оказывает отрицательного влияния на процесс заживления ран и бактериальную флору.
Системная абсорбция зависит от количества крема, продолжительности аппликации, толщины кожи (которая варьирует на разных участках тела) и других особенностей кожи.
Неповрежденная кожа. У взрослых после нанесения 60 г крема Эмла на неповрежденную кожу бедра площадью 400 см2 (1,5 г на 10 см2) за 3 ч системная абсорбция составляла 3% для лидокаина и 5% для прилокаина. Абсорбция происходит медленно. При указанной выше дозе Сmax в плазме крови лидокаина (в среднем — 0,12 мкг/мл) и прилокаина (в среднем — 0,07 мкг/мл) достигалась приблизительно через 4 ч после аппликации. Риск развития токсических симптомов существует лишь при уровне 5–10 мкг/мл.
Трофические язвы нижних конечностей. После нанесения на трофические язвы 5–10 г крема Эмла с экспозицией 30 мин Cmax лидокаина и прилокаина в плазме крови достигались приблизительно через 1–2,5 ч (концентрация лидокаина в пределах 0,05–0,84 мкг/мл, прилокаина — 0,02–0,08 мкг/мл).
После повторного нанесения крема Эмла на трофические язвы сколько-нибудь значимого накопления лидокаина, прилокаина или их метаболитов в плазме крови не отмечали (крем Эмла наносили по 2–10 г на 30–60 мин на участок площадью в пределах 62 см2 15 раз в месяц по 3–7 сеансов в неделю).
Слизистая оболочка половых органов. Сmax в плазме крови достигается приблизительно через 35 мин после нанесения 10 г крема Эмла на слизистую оболочку влагалища с экспозицией 10 мин (в среднем концентрация лидокаина составляла 0,18 мкг/мл; прилокаина — 0,15 мкг/мл).
поверхностная анестезия кожи при проведении пункций, катетеризации сосудов и поверхностных хирургических вмешательств.
Поверхностная анестезия трофических язв нижних конечностей при хирургической обработке (механическом очищении), например для удаления фибрина, гноя и некротических тканей.
Поверхностная анестезия слизистой оболочки половых органов.
взрослые
| Неповрежденная кожа | Доза и применение | Продолжительность аппликации |
|---|---|---|
| При введении игл, например для катетеризации сосудов или забора образцов крови | ½ объема тубы (около 2 г) на 10 см2. Толстый слой крема нанести на кожу и прикрыть окклюзионной наклейкой Толстый слой крема нанести на кожу и прикрыть окклюзионной наклейкой | 1 ч; максимум 5 ч |
| При проведении небольших хирургических процедур на поверхности кожи, например удаление бородавок | 1,5–2 г на 10 см2. Толстый слой крема нанести на кожу и прикрыть окклюзионной наклейкой | 1 ч; максимум 5 ч |
| При проведении хирургических процедур на больших площадях поверхности кожи, например взятие кожи методом расщепленного лоскута | 1,5–2 г на 10 см2. Толстый слой крема нанести на кожу и прикрыть окклюзионной наклейкой | 2 ч; максимум 5 ч |
Трофические язвы нижних конечностей. При хирургической обработке (механическом очищении) трофических язв нанести 1–2 г крема на 10 см2 поверхности. Крем наносят толстым слоем на поверхность язвы, не более 10 г крема на одну процедуру. Прикрыть поверхность язвы окклюзионной наклейкой. Продолжительность аппликации крема 30 мин.
Открытая туба предназначена для одноразового использования, после каждой процедуры неиспользованный крем выбрасывают.
При обработке язв, в ткани которых проникновение препарата затруднено, продолжительность аппликации можно увеличить до 60 мин. Хирургическую обработку раневой поверхности следует начинать не позже 10 мин после удаления крема.
При лечении трофических язв нижних конечностей крем Эмла применяют до 15 раз в течение 1–2 мес без снижения эффективности и повышения частоты развития местных реакций.
Поверхностная анестезия половых органов
Кожа половых органов. Применение перед инъекцией местных анестетиков:
- мужчины: 1 г на 10 см2. Толстый слой крема наносят на кожу. Продолжительность аппликации — 15 мин;
- женщины: 1–2 г на 10 см2. Толстый слой крема наносят на кожу. Продолжительность аппликации — 60 мин.
Слизистая оболочка половых органов. Для удаления кондилом или перед инъекцией местных анестетиков: 5–10 г крема в зависимости от площади лечения наносят на всю поверхность, включая складки слизистой оболочки. Окклюзионной наклейки не требуется. Продолжительность аппликации — 5–10 мин. Хирургическую процедуру следует начинать сразу после удаления крема.
Окклюзионной наклейки не требуется. Продолжительность аппликации — 5–10 мин. Хирургическую процедуру следует начинать сразу после удаления крема.
Дети
При проведении инъекций, удалении контагиозных моллюсков и других незначительных поверхностных хирургических манипуляциях: 1 г на 10 см2 поверхности, толстым слоем крем наносят на поверхность кожи и прикрывают окклюзионной наклейкой. Доза не должна превышать 1 г на 10 см2, ее следует корригировать в зависимости от площади нанесения.
| Возраст | Площадь нанесения | Продолжительность аппликации |
|---|---|---|
| 0–3 мес | Максимум 10 см2 (всего 1 г) (максимальная суточная доза) | 1 ч (примечание: не дольше) |
| 3–12 мес | Максимум 20 см2 (всего 2 г) | 1 ч |
| 1 год–6 лет | Максимум 100 см2 (всего 10 г) | 1 ч; максимум 5 ч |
| 6–12 лет | Максимум 200 см2 (всего 20 г) | 1 ч; максимум 5 ч |
Детям при атопическом дерматите необходимо уменьшить продолжительность аппликации до 30 мин.
Рекомендации относительно способа применения. Запаянную мембрану тубы проколоть шипом, находящимся в верхней внешней части крышки. Выдавить необходимое количество крема и нанести на место проведения процедуры. При обезболивании кожи применяют окклюзионные наклейки, входящие в комплект с кремом (12 шт. размером 6х7 см).
нарушение целостности кожи в месте нанесения крема (активный опоясывающий герпес, атопический дерматит или раны).
Гиперчувствительность к местным анестетикам амидного типа или любому вспомогательному веществу (например бупивакаин, этидокаин, мепивакаин).
Крем Эмла не применяют у недоношенных грудных детей (родившихся раньше полных 37 нед беременности).
истинные побочные реакции, вызванные применением местных анестетиков, возникают с частотой 1/1000 пациентов.
| Часто (>1/100) | Кожа: временные местные кожные реакции в месте нанесения, например местное побледнение, покраснение, отек |
| Нечасто (1/100–1/1000) | Кожа: после нанесения кожные высыпания, легкая боль, жжение или зуд в месте нанесения, аллергический контактный дерматит, крапивница, ангионевротический отек |
| Редко (<1/1000) | Общие: аллергические реакции, в наиболее тяжелых случаях анафилактический шок. Метгемоглобинемия у детей Метгемоглобинемия у детей |
Сообщалось об отдельных случаях местных реакций на участке нанесения крема, таких как геморрагические высыпания или петехии, особенно после длительной аппликации у детей с атопическим дерматитом или бородавками. При случайном попадании препарата в глаза может возникнуть раздражение роговицы.
пациенты с недостаточностью глюкозо-6-фосфат-дегидрогеназы, врожденной или идиопатической метгемоглобинемией более склонны к развитию препаратзависимой метгемоглобинемии.
Крем Эмла следует с осторожностью применять на коже в области глаз, поскольку препарат раздражает их слизистую оболочку. Кроме того, потеря защитных рефлексов вследствие попадания на роговицу анестетика может привести к раздражению и повреждению роговицы. При попадании крема Эмла в глаза их следует немедленно промыть водой или физиологическим р-ром (натрия хлорида) и защищать до восстановления чувствительности роговицы.
Препарат необходимо с осторожностью применять у пациентов с местной инфекцией в области применения, при травме в месте применения и при острых заболеваниях, у ослабленных больных, пациентов пожилого возраста, пациентов с тяжелой сердечной, почечной или печеночной недостаточностью.
Если во время применения препарата возникает ощущение жжения или покраснение кожи, ее необходимо промыть водой и прекратить применение, пока не исчезнет покраснение.
Эффективность применения крема у новорожденных при взятии крови из пятки не установлена.
Безопасность и эффективность применения препарата у детей в возрасте младше 3 мес исследовали лишь при применении разовой дозы. У таких детей после нанесения крема часто отмечают временное повышение уровня метгемоглобина в крови продолжительностью до 13 ч. Тем не менее этот факт, вероятно, не имеет клинического значения.
Крем Эмла нельзя наносить на поврежденную барабанную перепонку и не следует применять в ситуациях, когда препарат может проникнуть в полость среднего уха.
Крем Эмла не следует наносить на открытые раны.
Препарат не следует наносить на слизистую оболочку половых органов у детей в связи с недостаточностью данных относительно абсорбции.
При концентрации, превышающей 0,5–2,0%, лидокаин и прилокаин проявляют бактерицидные и противовирусные свойства. Поэтому в случае применения препарата при проведении вакцинации (внутрикожное введение живой вакцины, например БЦЖ) необходимо тщательное наблюдение. Не следует применять крем Эмла у детей в возрасте от 0 до 12 мес, получающих сопутствующую терапию препаратами, индуцирующими метгемоглобинемию, в связи с отсутствием достаточного клинического опыта применения.
Поэтому в случае применения препарата при проведении вакцинации (внутрикожное введение живой вакцины, например БЦЖ) необходимо тщательное наблюдение. Не следует применять крем Эмла у детей в возрасте от 0 до 12 мес, получающих сопутствующую терапию препаратами, индуцирующими метгемоглобинемию, в связи с отсутствием достаточного клинического опыта применения.
Необходимо вести наблюдение пациентов, получающих антиаритмические препараты, относящиеся к классу III (например амиодарон), учитывать результаты ЭКГ у таких пациентов, поскольку лидокаин и антиаритмические препараты класса III могут оказывать аддитивное действие.
Период беременности и кормления грудью. Данные относительно лечения кремом Эмла беременных недостаточны. Лидокаин и прилокаин проникают через плацентарный барьер и могут абсорбироваться эмбриональными тканями.
Сообщений о нарушении репродуктивного процесса, например повышении частоты пороков развития, прямого или косвенного влияния на плод, не было. Однако, применяя препарат в период беременности, необходимо анализировать соотношение польза/риск.
Однако, применяя препарат в период беременности, необходимо анализировать соотношение польза/риск.
Лидокаин и, вероятно, прилокаин, проникают в грудное молоко, но в таком малом количестве, что влияние терапевтических доз препарата на ребенка маловероятно.
Дети. Крем Эмла не следует применять у недоношенных детей грудного возраста (родившимся раньше 37 полных недель беременности).
Схему применения препарата у детей в зависимости от возраста см. в разделе ПРИМЕНЕНИЕ.
Не влияет на способность к управлению транспортными средствами и работе с другими механизмами.
Эмла может повышать образование метгемоглобина у пациентов, получающих лечение метгемоглобининдуцирующими препаратами (например сульфонамидами). При применении крема Эмла в высоких дозах у больных, получающих местные анестетики или препараты, структурно подобные местным анестетикам, например токаинид, необходимо учитывать риск системных аддитивных эффектов.
Абсорбция лидокаина через кожу обычно низкая, однако необходимо с осторожностью применять лидокаин у больных, которые принимают антиаритмические препараты І класса (токаинид, мексилетин) или другие местные анестетики, поскольку возможен риск возникновения суммарных системных эффектов. Ингибиторы МАО усиливают местноанальгезирующее действие лидокаина.
Ингибиторы МАО усиливают местноанальгезирующее действие лидокаина.
Специфических исследований взаимодействия препарата с местными анестетиками и антиаритмическими средствами, относящимися к классу III, не проводили, поэтому при их одновременном применении рекомендуется соблюдать осторожность.
при соблюдении рекомендуемого режима дозирования препарата развитие системной токсичности маловероятно. Вероятные симптомы интоксикации такие же, как и при применении других местных анестетиков: например, возбуждение ЦНС, в тяжелых случаях — угнетение ЦНС и сердечной деятельности.
Возможны повышенное потоотделение, бледность кожных покровов, головокружение, головная боль, нечеткость зрительного восприятия, шум в ушах, диплопия, снижение АД, брадикардия, аритмия, сонливость, озноб, онемение конечностей, беспокойство, судороги, шок, остановка сердца.
Очень редко сообщалось о случаях клинически значимой метгемоглобинемии у детей, поскольку прилокаин в высоких дозах может повышать уровень метгемоглобина.
Поверхностное применение 125 мг прилокаина продолжительностью 5 ч явилось причиной развития умеренной метгемоглобинемии у трехмесячного ребенка. Местное применение лидокаина 8,6–17,2 мг/кг массы тела привело к развитию тяжелой интоксикации у детей грудного возраста.
Выраженные неврологические симптомы (судороги, угнетение ЦНС) требуют симптоматического лечения: применения ИВЛ и противосудорожных препаратов. Антидотом при метгемоглобинемии является метилтионин. Вследствие медленной системной абсорбции препарата за состоянием пациента необходимо наблюдение еще в течение нескольких часов после устранения симптомов интоксикации.
С появлением первых признаков интоксикации (головокружение, тошнота, рвота, эйфория) перевести пациента в горизонтальное положение, назначить ингаляцию кислорода, при брадикардии — блокаторы М-холинорецепторов (атропин), вазоконстрикторы (норэпинефрин, фенилэфрин).
при температуре ниже 30 °С, не замораживать.
Крем с эвтектической смесью местных анестетиков (EMLA) более эффективен при венепункции по сравнению с лидокаиновой лентой у одних и тех же пациентов | JA Clinical Reports
- Статья о клиническом исследовании
- Открытый доступ
- Опубликовано:
- Томоми Мацумото 1 ,
- Томохиро Чаки ORCID: orcid.org/0000-0001-8898-3977 2 ,
- Наоюки Хирата 2 и
- …
- Мичиаки Ямакаге 2
Клинические отчеты JA том 4 , номер статьи: 73 (2018) Процитировать эту статью
7383 Доступ
7 Цитаты
3 Альтметрический
Сведения о показателях
Abstract
Введение
Хотя катетеризация вен обязательна в периоперационном периоде, она неизбежно вызывает боль при венепункции. Эвтектическая смесь местных анестетиков (EMLA) использовалась для уменьшения этой боли, и были проведены различные исследования для оценки эффективности EMLA. Но эти исследования не выявили точно эффект EMLA, потому что были большие индивидуальные различия в болевой чувствительности. Целью данного исследования является точная оценка эффективности крема EMLA для облегчения боли при венепункции по сравнению с лидокаиновой лентой у одних и тех же пациентов.
Эвтектическая смесь местных анестетиков (EMLA) использовалась для уменьшения этой боли, и были проведены различные исследования для оценки эффективности EMLA. Но эти исследования не выявили точно эффект EMLA, потому что были большие индивидуальные различия в болевой чувствительности. Целью данного исследования является точная оценка эффективности крема EMLA для облегчения боли при венепункции по сравнению с лидокаиновой лентой у одних и тех же пациентов.
Методы
Участники были случайным образом распределены в группы EL или LE. Перед входом в операционную участникам нанесли крем EMLA на одну сторону тыльной поверхности руки и лидокаиновую ленту на другую тыльную сторону руки. Местные анестетики применялись строго в соответствии с инструментами их производителей, соответственно. В группе EL участники сначала получали венепункцию на месте нанесения крема EMLA. В группе LE участники, наоборот, сначала получали венепункцию на месте лидокаиновой ленты. Перед индукцией анестезии местные анестетики удаляли с последующей венозной канюляцией. После катетеризации участники оценивали боль по визуальной аналоговой шкале (ВАШ) и вербальной оценочной шкале (VRS). Первичной конечной точкой была ВАШ, а вторичной — ВШР.
Перед индукцией анестезии местные анестетики удаляли с последующей венозной канюляцией. После катетеризации участники оценивали боль по визуальной аналоговой шкале (ВАШ) и вербальной оценочной шкале (VRS). Первичной конечной точкой была ВАШ, а вторичной — ВШР.
Результаты
Были проанализированы данные 24 пациентов. ВАШ крема EMLA был значительно ниже, чем у лидокаиновой ленты (4 [0–18] против 17 [8–45], p = 0,001, 95% ДИ от − 25 до − 6). VRS крема EMLA также был значительно ниже, чем у лидокаиновой ленты (2 [1–2] против 2 [2–3], p = 0,002, 95% ДИ от − 0,8 до − 0,2). Местные нежелательные явления со стороны кожи наблюдались у пяти пациентов при нанесении крема ЭМЛА на руки.
Выводы
Мы провели сравнительное исследование для выяснения эффективности крема EMLA при болях при венепункции по сравнению с лидокаиновой лентой у одних и тех же пациентов. Наши результаты убедительно свидетельствуют о том, что крем EMLA более эффективен для облегчения боли при венепункции, чем пластырь с лидокаином.
Регистрация испытаний
Реестр клинических испытаний UMIN, UMIN000023030. Зарегистрирован 5 июля 2016 г.
История вопроса
Венозная канюляция является обязательной процедурой для гидратации и внутривенного введения препаратов в периоперационном периоде. Однако эта процедура должна сопровождаться болью. Для ослабления этой боли были разработаны различные методы, одним из которых является применение крема эвтектической смеси местных анестетиков (EMLA). Несмотря на то, что с момента начала клинического использования крема ЭМЛА прошло несколько десятилетий и было опубликовано несколько клинических исследований, оценивающих его эффективность [1], во всех этих исследованиях участники были разделены на две группы, и каждая группа получала только одно исследование. вмешательства. Однако, поскольку существуют большие индивидуальные различия в болевой чувствительности даже к одним и тем же раздражителям, такой дизайн клинического исследования не обеспечивает точности оценки боли [2]. Целью данного исследования было точное определение эффективности крема EMLA для облегчения боли при венепункции по сравнению с лидокаиновой лентой, традиционным обезболивающим методом, у одних и тех же пациентов.
Целью данного исследования было точное определение эффективности крема EMLA для облегчения боли при венепункции по сравнению с лидокаиновой лентой, традиционным обезболивающим методом, у одних и тех же пациентов.
Методы
Это одноцентровое проспективное рандомизированное интервенционное исследование проводилось в городской больнице Томакомай, Хоккайдо, Япония, с июля 2016 г. по март 2017 г. Исследование было одобрено экспертным советом городской больницы Томакомай, Япония ( код одобрения: 1605) и зарегистрирован в Реестре клинических испытаний UMIN (идентификатор испытания UMIN: UMIN000023030). Перед участием в данном исследовании от всех пациентов были получены письменные информированные согласия. Приемлемыми участниками были пациенты в возрасте 16 лет и старше, Американское общество анестезиологов с физическим статусом I–III, которым потребовалось два венозных доступа во время плановой операции под общей анестезией. Критериями исключения были пациенты с аллергией на местные анестетики и кожными аномалиями в месте венепункции. Также исключались пациенты с тяжелыми заболеваниями печени, почек и сердца, которые могли повлиять на метаболизм лекарств. Строго в соответствии с инструкциями производителя, 1 г 5% крема EMLA®, содержащего 25 мг лидокаина и 25 мг прилокаина на грамм (Сато Сейяку, Токио, Япония), наносили на тыльную поверхность одной руки и покрывали Tegaderm™. прозрачная пленочная повязка (3 M Medical, Maplewood, MN) за 60 минут до входа в операционную, а лидокаиновая лента (YouPatch Tape® 18 мг, Yutoku Yakuhin, Saga, Japan) была наложена на тыльную поверхность другой руки за 30 минут до вход в операционную для всех участников. Все участники были случайным образом распределены в соответствии с компьютерной рандомизацией в группу EL: сначала делали венепункцию в месте нанесения крема EMLA и во вторую очередь в месте нанесения лидокаиновой ленты, или в группу LE: сначала делали венепункции в месте нанесения лидокаиновой ленты и во вторую очередь в месте нанесения крема EMLA (рис. 1). Время и дозы применения местных анестетиков строго определялись в соответствии с инструкциями соответствующих производителей.
Также исключались пациенты с тяжелыми заболеваниями печени, почек и сердца, которые могли повлиять на метаболизм лекарств. Строго в соответствии с инструкциями производителя, 1 г 5% крема EMLA®, содержащего 25 мг лидокаина и 25 мг прилокаина на грамм (Сато Сейяку, Токио, Япония), наносили на тыльную поверхность одной руки и покрывали Tegaderm™. прозрачная пленочная повязка (3 M Medical, Maplewood, MN) за 60 минут до входа в операционную, а лидокаиновая лента (YouPatch Tape® 18 мг, Yutoku Yakuhin, Saga, Japan) была наложена на тыльную поверхность другой руки за 30 минут до вход в операционную для всех участников. Все участники были случайным образом распределены в соответствии с компьютерной рандомизацией в группу EL: сначала делали венепункцию в месте нанесения крема EMLA и во вторую очередь в месте нанесения лидокаиновой ленты, или в группу LE: сначала делали венепункции в месте нанесения лидокаиновой ленты и во вторую очередь в месте нанесения крема EMLA (рис. 1). Время и дозы применения местных анестетиков строго определялись в соответствии с инструкциями соответствующих производителей. Непосредственно перед индукцией анестезии пластырь и крем удаляли и один за другим вводили два внутривенных катетера 20G Surflo® ETFE (Terumo Corp, Токио, Япония) в области, подвергшиеся местной анестезии. У всех пациентов порядок венозных канюляций соответствовал выделенной группе. После двух венозных канюлей участники оценивали боль во время введения внутривенной канюли по визуальной аналоговой шкале (ВАШ 0–100 мм; 0 мм — отсутствие боли; 100 мм — нестерпимая боль) и вербальной оценочной шкале (VRS 1–4; 1 — отсутствие боли). боль; 4, нестерпимая боль). Также наблюдали за состоянием кожи в месте применения местного анестетика для оценки любых побочных эффектов вмешательства (например, покраснение кожи, изменение цвета).
Непосредственно перед индукцией анестезии пластырь и крем удаляли и один за другим вводили два внутривенных катетера 20G Surflo® ETFE (Terumo Corp, Токио, Япония) в области, подвергшиеся местной анестезии. У всех пациентов порядок венозных канюляций соответствовал выделенной группе. После двух венозных канюлей участники оценивали боль во время введения внутривенной канюли по визуальной аналоговой шкале (ВАШ 0–100 мм; 0 мм — отсутствие боли; 100 мм — нестерпимая боль) и вербальной оценочной шкале (VRS 1–4; 1 — отсутствие боли). боль; 4, нестерпимая боль). Также наблюдали за состоянием кожи в месте применения местного анестетика для оценки любых побочных эффектов вмешательства (например, покраснение кожи, изменение цвета).
Блок-схема CONSORT. Группа EL сначала получила венепункцию на месте нанесения крема EMLA, а затем на месте лидокаиновой ленты. И наоборот, группа LE сначала получила венепункцию на месте лидокаиновой ленты, а затем на месте нанесения крема EMLA. Эвтектическая смесь местных анестетиков EMLA
Эвтектическая смесь местных анестетиков EMLA
Изображение в полный размер
Исходы
Первичным результатом была оценка боли при венепункции по ВАШ. Вторичными результатами были шкала VRS для боли при венепункции и частота побочных эффектов, включая кожные симптомы и токсичность местных анестетиков. Более того, анализ подгрупп и сравнение интенсивности боли при первой и второй венепункции также выполнялись в качестве вторичных результатов.
Статистический анализ
Оценки по ВАШ и ВРС, анализ подгрупп и сравнение интенсивности боли при первом и втором проколе у всех участников были проанализированы с помощью знакового рангового критерия Уилкоксона, тогда как сравнение интенсивности боли при первом и втором проколе в EMLA и лидокаиновые участки анализировали с помощью теста Манна-Уитни U . Частоту побочных эффектов анализировали с помощью точного критерия Фишера. Все статистические анализы проводились с использованием GraphPad Prism 7.0 (GraphPad Software, La Jolla, CA). Данные представлены в виде медианы [межквартильный размах]. Значение р менее 0,05 считалось статистически значимым. Размер выборки был рассчитан по G * степени 3,1 (Университет Генриха Гейне, Дюссельдорф, Германия). Разница в 18,1 балла по ВАШ считалась клинически значимой на основании результатов исследования Çelik et al. [3]. Размер выборки оценивали по способности обнаруживать снижение показателей ВАШ до 18,1 при стандартном отклонении 17,9 для крема EMLA и 10,6 для лидокаиновой ленты с двусторонним 5% уровнем значимости и мощностью 0,8. Расчет размера выборки показал, что в этом исследовании было необходимо 24 пациента.
Данные представлены в виде медианы [межквартильный размах]. Значение р менее 0,05 считалось статистически значимым. Размер выборки был рассчитан по G * степени 3,1 (Университет Генриха Гейне, Дюссельдорф, Германия). Разница в 18,1 балла по ВАШ считалась клинически значимой на основании результатов исследования Çelik et al. [3]. Размер выборки оценивали по способности обнаруживать снижение показателей ВАШ до 18,1 при стандартном отклонении 17,9 для крема EMLA и 10,6 для лидокаиновой ленты с двусторонним 5% уровнем значимости и мощностью 0,8. Расчет размера выборки показал, что в этом исследовании было необходимо 24 пациента.
Результаты
Всего было обследовано 24 пациента для включения в это исследование, и все участники были включены в это исследование. 12 пациентов были распределены в группу EL, а другие 12 пациентов были распределены в группу LE. Характеристики всех участников представлены в таблице 1. Показатели ВАШ для рук с кремом EMLA были значительно ниже, чем для рук с лидокаиновой лентой (4 [0–18] против 17 [8–45], p = 0,001, 95 % ДИ от - 25 до - 6) (рис. 2а). Показатели VRS для рук с кремом EMLA также были значительно ниже, чем для рук с лидокаиновой лентой (2 [1–2] против 2 [2–3], 9 баллов).0069 p = 0,002, 95% ДИ от − 0,8 до − 0,2) (рис. 2b). Анализ подгрупп показал, что VAS и VRS в группе EL и VAS в группе LE были статистически значимо ниже в группе EMLA, чем в группе лидокаина, в то время как не было статистически значимой разницы в VRS в группе LE между EMLA и лидокаином (таблица 2). . Не было статистически значимых различий при сравнении интенсивности боли при первом и втором проколе (таблица 3). Частота местных нежелательных явлений со стороны кожи была значительно выше при использовании крема EMLA (EMLA 5/24, 21% по сравнению с лидокаином 0/24, 0%, 9%).0069 p = 0,022, относительный риск 2,32, 95% ДИ от 1,24 до 10,51). В частности, четыре из 24 рук, которым наносили крем EMLA, стали бледнее после нанесения крема EMLA, а на одной из 24 рук после нанесения Tegaderm™ появилось покраснение кожи, хотя эти изменения кожи исчезли на следующий день.
2а). Показатели VRS для рук с кремом EMLA также были значительно ниже, чем для рук с лидокаиновой лентой (2 [1–2] против 2 [2–3], 9 баллов).0069 p = 0,002, 95% ДИ от − 0,8 до − 0,2) (рис. 2b). Анализ подгрупп показал, что VAS и VRS в группе EL и VAS в группе LE были статистически значимо ниже в группе EMLA, чем в группе лидокаина, в то время как не было статистически значимой разницы в VRS в группе LE между EMLA и лидокаином (таблица 2). . Не было статистически значимых различий при сравнении интенсивности боли при первом и втором проколе (таблица 3). Частота местных нежелательных явлений со стороны кожи была значительно выше при использовании крема EMLA (EMLA 5/24, 21% по сравнению с лидокаином 0/24, 0%, 9%).0069 p = 0,022, относительный риск 2,32, 95% ДИ от 1,24 до 10,51). В частности, четыре из 24 рук, которым наносили крем EMLA, стали бледнее после нанесения крема EMLA, а на одной из 24 рук после нанесения Tegaderm™ появилось покраснение кожи, хотя эти изменения кожи исчезли на следующий день. В руках, получавших лидокаин, местных нежелательных явлений не наблюдалось. Ни у одного из пациентов не возникло системных нежелательных явлений в ответ на применение местных анестетиков, включая симптомы токсичности.
В руках, получавших лидокаин, местных нежелательных явлений не наблюдалось. Ни у одного из пациентов не возникло системных нежелательных явлений в ответ на применение местных анестетиков, включая симптомы токсичности.
Полноразмерная таблица
Рис. 2Сравнение интенсивности боли между кремом EMLA и лидокаиновой лентой. a Визуальная аналоговая шкала оценивает боль при катетеризации вены. * р = 0,001. b Вербальная шкала оценивает боль при катетеризации вены. † p = 0,002. Данные представлены в виде медианы [межквартильный размах]. ЭМЛА эвтектическая смесь местных анестетиков
Изображение в натуральную величину
Таблица 2 Анализ интенсивности боли в подгруппахПолноразмерная таблица
Таблица 3 Сравнение интенсивности боли при первом и втором проколеПолноразмерная таблица
Обсуждение
венепункция до индукции общей анестезии у тех же больных. Результаты исследования показывают, что крем ЭМЛА более эффективен для обезболивания при венепункции, чем лидокаиновая лента. Новизна данного исследования заключается в том, что в нем сравниваются два метода местной анестезии у одного и того же человека. Хотя некоторые предыдущие рандомизированные контролируемые исследования крема EMLA действительно существуют, их участники были разделены на две группы, и каждая группа получала только один метод местной анестезии [1]. Как известно, существуют значительные индивидуальные различия в болевой чувствительности [2]. Следовательно, идеально, чтобы один и тот же участник оценивал влияние на обезболивание венепункции как крема EMLA, так и лидокаиновой ленты. Кроме того, в нашем исследовании количество рук, анестезированных кремом EMLA, которые были проколоты первыми, было таким же, как и количество рук, анестезированных лидокаиновой лентой, которые были проколоты первыми, по 12 рук в каждой. Эти особенности дизайна нашего исследования повышают уровень точности и достоверности наших результатов о том, что крем EMLA более эффективен для облегчения боли во время венозной катетеризации, чем лидокаиновая лента.
Результаты исследования показывают, что крем ЭМЛА более эффективен для обезболивания при венепункции, чем лидокаиновая лента. Новизна данного исследования заключается в том, что в нем сравниваются два метода местной анестезии у одного и того же человека. Хотя некоторые предыдущие рандомизированные контролируемые исследования крема EMLA действительно существуют, их участники были разделены на две группы, и каждая группа получала только один метод местной анестезии [1]. Как известно, существуют значительные индивидуальные различия в болевой чувствительности [2]. Следовательно, идеально, чтобы один и тот же участник оценивал влияние на обезболивание венепункции как крема EMLA, так и лидокаиновой ленты. Кроме того, в нашем исследовании количество рук, анестезированных кремом EMLA, которые были проколоты первыми, было таким же, как и количество рук, анестезированных лидокаиновой лентой, которые были проколоты первыми, по 12 рук в каждой. Эти особенности дизайна нашего исследования повышают уровень точности и достоверности наших результатов о том, что крем EMLA более эффективен для облегчения боли во время венозной катетеризации, чем лидокаиновая лента.
Как подтвердили наши исследования, крем EMLA обеспечивает более эффективное обезболивание, чем пластырь с лидокаином. Возможная причина такой разницы в эффективности заключается в том, что крем ЭМЛА представляет собой эвтектическую смесь местных анестетиков, которая обладает высокой проницаемостью для кожи. Однако, учитывая предыдущий отчет о том, что крем EMLA превосходит инфильтрацию 1% лидокаином для катетеризации артерий [4], механизм эффективности крема EMLA не ограничивается его высокой проницаемостью. В то время как лидокаин необходимо растворять в каком-либо растворителе для его применения в качестве наружного препарата, крем ЭМЛА не требует растворителя и обеспечивает высокую концентрацию местных анестетиков. Эти два фактора, высокая проницаемость и концентрация местных анестетиков, являются механизмами, благодаря которым крем EMLA более эффективен, чем пластырь с лидокаином.
В этом исследовании был проведен анализ подгрупп и сравнение интенсивности боли при первом и втором проколах, чтобы выяснить влияние порядка проколов на оценку интенсивности боли. Интенсивность боли при втором уколе была выше, чем при первом уколе, хотя это различие не было статистически значимым. Более того, ВРС в группе КЭ не была статистически значимой. Эти результаты позволяют предположить, что боль при втором уколе может стать более сильной, чем боль при первом уколе. Согласно предыдущим сообщениям, существует положительная связь между тревогой и болью в клинических условиях [5], а анксиолитические препараты могут уменьшать боль, вызванную медицинскими процедурами [6]. В этом исследовании была некоторая вероятность того, что участники чувствовали некоторую тревогу, вызванную болью при первой венепункции, что приводило к усилению интенсивности боли при второй пункции. Но мы оценили, что это влияние на результат этого исследования можно было не принимать во внимание, потому что компьютерная рандомизация была выполнена для уравнивания количества мест, впервые проколотых местными анестетиками.
Интенсивность боли при втором уколе была выше, чем при первом уколе, хотя это различие не было статистически значимым. Более того, ВРС в группе КЭ не была статистически значимой. Эти результаты позволяют предположить, что боль при втором уколе может стать более сильной, чем боль при первом уколе. Согласно предыдущим сообщениям, существует положительная связь между тревогой и болью в клинических условиях [5], а анксиолитические препараты могут уменьшать боль, вызванную медицинскими процедурами [6]. В этом исследовании была некоторая вероятность того, что участники чувствовали некоторую тревогу, вызванную болью при первой венепункции, что приводило к усилению интенсивности боли при второй пункции. Но мы оценили, что это влияние на результат этого исследования можно было не принимать во внимание, потому что компьютерная рандомизация была выполнена для уравнивания количества мест, впервые проколотых местными анестетиками.
С точки зрения безопасности местных анестетиков наиболее важной проблемой является токсичность местных анестетиков. В нашем исследовании концентрации лидокаина и прилокаина в сыворотке не измерялись. Они и др. измерили концентрацию лидокаина в сыворотке после нанесения 30 г 2,5% крема ЭМЛА на кожу лица и шеи [7]. Средняя пиковая концентрация лидокаина в сыворотке составила 0,44 мкг/мл через 90 минут после нанесения, несмотря на удаление крема EMLA через 60 минут после его нанесения. Хотя эта концентрация была ниже порога токсичности лидокаина, имелись значительные индивидуальные различия. Пиковая индивидуальная концентрация лидокаина в их исследовании составила 0,78 мкг/мл, что примерно в два раза превышает среднее значение. Существуют три основных фактора, ответственных за индивидуальные различия в абсорбции и концентрации местных анестетиков в сыворотке крови. Во-первых, это масса тела. Ранее были опубликованы сообщения о случаях токсичности местных анестетиков у 3-летних детей, получавших крем ЭМЛА [8, 9].]. Поэтому применение ЭМЛА у маленьких детей требует особого внимания. Второй фактор – нарушение функции печени.
В нашем исследовании концентрации лидокаина и прилокаина в сыворотке не измерялись. Они и др. измерили концентрацию лидокаина в сыворотке после нанесения 30 г 2,5% крема ЭМЛА на кожу лица и шеи [7]. Средняя пиковая концентрация лидокаина в сыворотке составила 0,44 мкг/мл через 90 минут после нанесения, несмотря на удаление крема EMLA через 60 минут после его нанесения. Хотя эта концентрация была ниже порога токсичности лидокаина, имелись значительные индивидуальные различия. Пиковая индивидуальная концентрация лидокаина в их исследовании составила 0,78 мкг/мл, что примерно в два раза превышает среднее значение. Существуют три основных фактора, ответственных за индивидуальные различия в абсорбции и концентрации местных анестетиков в сыворотке крови. Во-первых, это масса тела. Ранее были опубликованы сообщения о случаях токсичности местных анестетиков у 3-летних детей, получавших крем ЭМЛА [8, 9].]. Поэтому применение ЭМЛА у маленьких детей требует особого внимания. Второй фактор – нарушение функции печени. Местные анестетики, включая лидокаин, метаболизируются в печени (например, лидокаин метаболизируется в печени в моноэтилглицинексилидид и выводится почками). Необходимо также строгое внимание при применении ЭМЛА у пациентов с недостаточностью функции печени. Последний фактор – кожные заболевания. Барьерная функция кожи утрачивается на участках кожи с дермопатией, что приводит к чрезмерному всасыванию местных анестетиков. Юхлин и др. оценили концентрации лидокаина и прилокаина в плазме после нанесения крема EMLA и сравнили эти концентрации у пациентов с нормальной и пораженной кожей [10]. У пациентов с кожными заболеваниями абсорбция была более быстрой, чем у пациентов с нормальной кожей, что приводило к высоким концентрациям в плазме крови. Пиковые концентрации местных анестетиков у пациентов с пораженной кожей были в десятки раз выше, чем у пациентов с нормальной кожей. Это указывает на необходимость уделять пристальное внимание при применении EMLA у пациентов, у которых есть любой из трех вышеперечисленных факторов, которые могут привести к увеличению концентрации местных анестетиков в сыворотке крови, что приводит к системной токсичности местных анестетиков.
Местные анестетики, включая лидокаин, метаболизируются в печени (например, лидокаин метаболизируется в печени в моноэтилглицинексилидид и выводится почками). Необходимо также строгое внимание при применении ЭМЛА у пациентов с недостаточностью функции печени. Последний фактор – кожные заболевания. Барьерная функция кожи утрачивается на участках кожи с дермопатией, что приводит к чрезмерному всасыванию местных анестетиков. Юхлин и др. оценили концентрации лидокаина и прилокаина в плазме после нанесения крема EMLA и сравнили эти концентрации у пациентов с нормальной и пораженной кожей [10]. У пациентов с кожными заболеваниями абсорбция была более быстрой, чем у пациентов с нормальной кожей, что приводило к высоким концентрациям в плазме крови. Пиковые концентрации местных анестетиков у пациентов с пораженной кожей были в десятки раз выше, чем у пациентов с нормальной кожей. Это указывает на необходимость уделять пристальное внимание при применении EMLA у пациентов, у которых есть любой из трех вышеперечисленных факторов, которые могут привести к увеличению концентрации местных анестетиков в сыворотке крови, что приводит к системной токсичности местных анестетиков.
Другим побочным эффектом местных анестетиков является изменение цвета кожи, такое как бледность и покраснение. EMLA часто вызывает побледнение кожи, вызывая сужение сосудов [11]. Хотя этот побочный эффект имеет тенденцию исчезать в течение нескольких дней, он затрудняет венепункцию и венозную катетеризацию [12]. Факторы, влияющие на трудности катетеризации периферических вен, были исследованы Fields et al. и Пиредда и др. [13, 14]. Они сообщили о связи между трудностями катетеризации периферических вен и диабетом, внутривенным злоупотреблением наркотиками, серповидно-клеточной анемией, венами со многими клапанами, венозной хрупкостью, видимостью и пальпируемостью, а также химиотерапией, полученной через периферическую канюлю. Следовательно, во время венозной канюляции у пациентов с этими факторами лучше избегать использования EMLA для облегчения успешной канюляции.
Ограничения
Это исследование имеет два основных ограничения. Во-первых, мы оценили боль, вызванную венозной канюляцией, используя только субъективные измерения. Для объективной оценки боли следует измерить частоту сердечных сокращений и артериальное давление до и после венепункции. Но на эти параметры также легко влиял эмоциональный фактор, и точность оценки боли при венепункции была очень ограниченной. Второе ограничение заключается в том, что концентрации лидокаина и прилокаина в сыворотке не измерялись для выяснения безопасности крема EMLA и лидокаиновой ленты. Хотя ни у одного из пациентов в этом исследовании не было выявлено симптомов токсичности местных анестетиков, изменение концентраций лидокаина и прилокаина в сыворотке крови следует измерять до 9 лет.0 мин после применения ЭМЛА для подтверждения безопасности этого препарата [7].
Для объективной оценки боли следует измерить частоту сердечных сокращений и артериальное давление до и после венепункции. Но на эти параметры также легко влиял эмоциональный фактор, и точность оценки боли при венепункции была очень ограниченной. Второе ограничение заключается в том, что концентрации лидокаина и прилокаина в сыворотке не измерялись для выяснения безопасности крема EMLA и лидокаиновой ленты. Хотя ни у одного из пациентов в этом исследовании не было выявлено симптомов токсичности местных анестетиков, изменение концентраций лидокаина и прилокаина в сыворотке крови следует измерять до 9 лет.0 мин после применения ЭМЛА для подтверждения безопасности этого препарата [7].
Выводы
Мы провели это проспективное сравнительное исследование, чтобы точно определить эффективность крема EMLA и лидокаиновой ленты для облегчения боли во время венепункции у одних и тех же пациентов. Эти результаты определенно указывают на то, что крем EMLA обеспечивает более эффективное облегчение боли, возникающей в результате венозной катетеризации. Необходимо более детальное исследование для подтверждения безопасности крема ЭМЛА у различных групп пациентов и при различных клинических состояниях.
Необходимо более детальное исследование для подтверждения безопасности крема ЭМЛА у различных групп пациентов и при различных клинических состояниях.
Сокращения
- EMLA:
Эвтектическая смесь местных анестетиков
- ВАС:
Визуальные аналоговые весы
- ВРС:
Вербальная шкала оценки
Ссылки
Dalvandi A, Ranjbar H, Hatamizadeh M, Hatamizadeh M, Bernstein C. Сравнение эффективности спрея vapocoolant и лидокаин/новокаинового крема в снижении боли при внутривенной катетеризации: рандомизированное клиническое исследование. Am J Emerg Med. 2017; 35:1064–8.
Артикул Google Scholar
- «>
Nielsen CS, Staud R, Цена DD. Индивидуальные различия в болевой чувствительности: измерение, причинно-следственная связь и последствия. Джей Пейн. 2009; 10: 231–7.
Артикул Google Scholar
Челик Г., Озбек О, Йилмаз М., Думан И., Озбек С., Апилиогуллари С. Спрей Vapocoolant и крем с лидокаином/прилокаином для уменьшения боли при венепункции у пациентов, находящихся на гемодиализе: рандомизированное плацебо-контролируемое перекрестное исследование. Int J Med Sci. 2011; 8: 623–7.
Артикул Google Scholar
Смит М., Грей Б.М., Инграм С., Джукс Д.А. Двойное слепое сравнение местного лигнокаин-прилокаинового крема (EMLA) и лигнокаиновой инфильтрации для катетеризации артерий у взрослых. Бр Джей Анаст. 1990;65:240–2.
Артикул КАС Google Scholar
«>Деллемейн PL, Филдс HL. Бензодиазепины играют роль в лечении хронической боли? Боль 1994; 57: 137–152.
Артикул КАС Google Scholar
Oni G, Brown S, Kenkel J. Сравнение пяти общедоступных местных анестетиков, содержащих лидокаин, и их влияние на уровни лидокаина и его метаболита моноэтилглицинексилидида (MEGX) в сыворотке крови. Эстет Сург Дж. 2012;32:495–503.
Артикул Google Scholar
Чо Ю.С., Чанг Б.И., Пак К.В., Ким Х.О. Судороги и метгемоглобинемия после местного применения эвтектической смеси лидокаина и прилокаина у ребенка 3,5 лет с контагиозным моллюском и атопическим дерматитом.
 Педиатр Дерматол. 2016;33:e284–5.
Педиатр Дерматол. 2016;33:e284–5.Артикул Google Scholar
Тома С., Джексон Дж.Б. Токсичность лидокаина и прилокаина у пациента, получающего лечение от контагиозного моллюска. J Am Acad Дерматол. 2001;44:399–400.
Артикул КАС Google Scholar
Juhlin L, Hägglund G, Evers H. Абсорбция лидокаина и прилокаина после нанесения эвтектической смеси местных анестетиков (EMLA) на нормальную и больную кожу. Акта Дерм Венерол. 1989; 69: 18–22.
КАС пабмед Google Scholar
Сойер Дж., Феббраро С., Масуд С., Эшберн М.А., Кэмпбелл Дж.К. Нагретый пластырь лидокаин/тетракаин (Synera, Rapydan) по сравнению с кремом лидокаин/прилокаин (EMLA) для местной анестезии перед сосудистым доступом. Бр Джей Анаст. 2009 г.;102:210–5.
Артикул КАС Google Scholar
- «>
Browne J, Awad I, Plant R, McAdoo J, Shorten G. Аметокаин для местного применения (Ametop) превосходит EMLA для внутривенной катетеризации. Эвтектическая смесь местных анестетиков. Джан Джей Анаст. 1999;46:1014–8.
Артикул КАС Google Scholar
Поля JM, Piela NE, Au AK, Ku BS. Факторы риска, связанные с затрудненным венозным доступом у взрослых пациентов с ЭД. Am J Emerg Med. 2014;32:1179–82.
Артикул Google Scholar
Пиредда М., Бьяджоли В., Баррелла Б., Карписасси И., Джинелли Р., Джаннарелли Д., Де Маринис М.Г. Факторы, влияющие на трудность катетеризации периферических вен у взрослых: проспективное обсервационное исследование. Джей Клин Нурс. 2017;26:1074–84.
Артикул Google Scholar
Грачев И.Д., Фредиксон Б.Е., Апкарян А.В. Диссоциация тревоги от боли: сопоставление нейронного маркера N-ацетиласпартата с восприятием позволяет различать тесно взаимосвязанные характеристики хронической боли. Мол Психиатрия. 2001; 6: 256–8.
Артикул КАС Google Scholar
Скачать ссылки
Доступность данных и материалов
Наборы данных, использованные и/или проанализированные в ходе текущего исследования, можно получить у соответствующего автора по разумному запросу.
Информация об авторе
Авторы и организации
Отделение анестезиологии, Городская больница Томакомай, 1-5-20, Симидзу-чо, Томакомай, Хоккайдо, Япония
Томоми Мацумото Отделение
4 сиология, Саппоро Медикал Университетская школа медицины, 291, Юг 1, Запад 16, Тюо-ку, Саппоро, Хоккайдо, Япония
Томохиро Чаки, Наоюки Хирата и Митиаки Ямакаге
Авторы
- Томоми Мацумото
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Tomohiro Chaki
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Наоюки Хирата
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Мичиаки Ямакагэ
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Contributions
TM участвовала в разработке концепции и дизайна исследования, сборе данных, анализе и интерпретации данных, а также в составлении статьи. ТС внес вклад в разработку концепции и дизайна исследования, анализ и интерпретацию данных, а также составление статьи. NH и MY внесли свой вклад в пересмотр статьи на предмет важного интеллектуального содержания. Все авторы прочитали и одобрили окончательный вариант рукописи.
ТС внес вклад в разработку концепции и дизайна исследования, анализ и интерпретацию данных, а также составление статьи. NH и MY внесли свой вклад в пересмотр статьи на предмет важного интеллектуального содержания. Все авторы прочитали и одобрили окончательный вариант рукописи.
Автор, ответственный за переписку
Томохиро Чаки.
Декларации этических норм
Одобрение этических норм и согласие на участие
Это исследование было одобрено институциональным наблюдательным советом городской больницы Томакомай, Япония (код разрешения: 1605), и зарегистрировано в Реестре клинических испытаний UMIN (идентификатор испытания UMIN: UMIN000023030). Перед участием в данном исследовании от всех пациентов были получены письменные информированные согласия.
Согласие на публикацию
Неприменимо
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья распространяется на условиях международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение, и воспроизведение на любом носителе, при условии, что вы укажете автора(ов) оригинала и источник, предоставите ссылку на лицензию Creative Commons и укажете, были ли внесены изменения.
Перепечатки и разрешения
Об этой статье
Крем EMLA и связанные названия
Содержание
- Обзор
- Основные факты
- Все документы
Обзор
25 сентября 2014 года Европейское агентство по лекарственным средствам завершило обзор крема EMLA. Комитет Агентства по лекарственным средствам для человека (CHMP) пришел к выводу, что существует необходимость согласования информации о назначении крема EMLA в Европейском союзе (ЕС).
Ключевые факты
Об этом лекарстве | |
|---|---|
| Утвержденное название | Крем EMLA и сопутствующие названия |
| Международное непатентованное наименование (МНН) или общеупотребительное наименование |
|
Об этой процедуре | |
|---|---|
| Текущий статус | Окончательное решение Европейской комиссии |
| Референтный номер | EMEA/H/A-30/1388 |
| Тип | Направления по статье 30 Этот тип направления инициируется, когда государства-члены принимают разные решения в отношении некоторых лекарственных средств (например, разные показания, противопоказания или дозировка) и возникает необходимость гармонизировать по всему ЕС. |
Ключевые даты и итоги | |
|---|---|
| Дата заключения CHMP | 25.09.2014 |
| Дата решения ЕС | 28.11.2014 |
Все документы
Заключение Комитета по лекарственным средствам для человека
Окончательное решение Европейской комиссии
Описание опубликованных документов
Обратите внимание, что некоторые из перечисленных документов относятся только к определенным процедурам.
- Обзор — краткое изложение этапа процедуры
- Уведомление – письмо от государства-члена, Европейской комиссии или держателя регистрационного удостоверения с просьбой инициировать процедуру .
- Научная база – дополнительная справочная информация от инициирующего государства-члена по вопросам, приведшим к инициированию процедуры (если применимо)
- Перечень вопросов – вопросы, согласованные Комитетом, запрашивающие дополнительную информацию у держателя (держателей) регистрационного удостоверения / заявителя (заявителей) для оценки выявленных проблем
- График проведения процедуры – согласованные сроки для ответа на перечень вопросов, оценки вопросов и принятия заключения
- Перечень лекарственных средств, рассматриваемых в процедуре – соответствующие лекарственные средства/действующее(ие) вещество(а) и держатель(и) регистрационного удостоверения/заявитель(и)
- Перечень вопросов, на которые должны ответить заинтересованные стороны – запросите данные, которые должны быть представлены заинтересованными сторонами (например, работниками здравоохранения, организациями пациентов, отдельными пациентами) (если применимо)
- Форма представления данных заинтересованными сторонами – форма, которую заинтересованные стороны должны использовать для предоставления данных (если применимо)
- Научные выводы – научные выводы PRAC и/или CHMP и/или CMDh
- Отчет об оценке – оценка PRAC или CHMP и выводы по исследованным вопросам, включая различные позиции (если применимо)
- Расходящиеся позиции – расходящиеся позиции членов CHMP или CMDh в отношении процедур фармаконадзора (если применимо)
- Изменения в сводке характеристик продукта, маркировке и листке-вкладыше (измененные разделы или полностью переработанная версия) (если применимо)
- Условия регистрационного удостоверения (регистраций) – условия безопасного и эффективного использования лекарственного средства (лекарств) (если применимо)
- Условие для отмены приостановки — условие, которое должно быть выполнено для приостановки действия регистрационного удостоверения (регистраций) для отмены (если применимо)
- График реализации позиции CMDh – согласованные сроки для представления и окончательной доработки вариантов, реализующих результаты процедуры (если применимо)
Обратите внимание, что старые документы могут иметь другие названия.

 Кроме того, была включена информация, поясняющая, что исследования не показали, что крем EMLA эффективен в обеспечении адекватного обезболивания при обрезании (хирургическом удалении крайней плоти).
Кроме того, была включена информация, поясняющая, что исследования не показали, что крем EMLA эффективен в обеспечении адекватного обезболивания при обрезании (хирургическом удалении крайней плоти).