Каковы основные показания для энтерального питания через зонд у пациентов после инсульта. Какие методы зондового питания применяются при инсульте. Какие осложнения могут возникнуть при зондовом питании у пациентов с инсультом. Как предотвратить и устранить осложнения зондового питания после инсульта.
Показания для энтерального питания через зонд после инсульта
Энтеральное питание через зонд часто назначается пациентам после инсульта, которые не могут принимать пищу естественным путем. Основными показаниями являются:
- Нарушение глотания (дисфагия)
- Снижение уровня сознания
- Высокий риск аспирации
- Невозможность обеспечить адекватное пероральное питание
Зондовое питание позволяет обеспечить пациента необходимыми питательными веществами, предотвратить истощение и обезвоживание в острый период после инсульта.
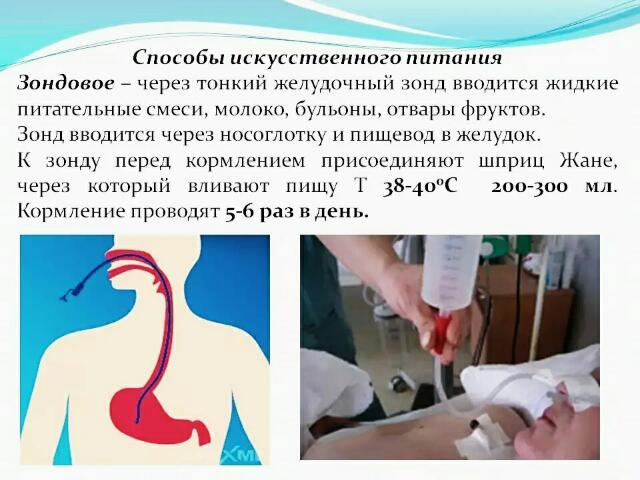
Методы энтерального питания при инсульте
Для проведения энтерального питания у пациентов после инсульта применяются следующие основные методы:
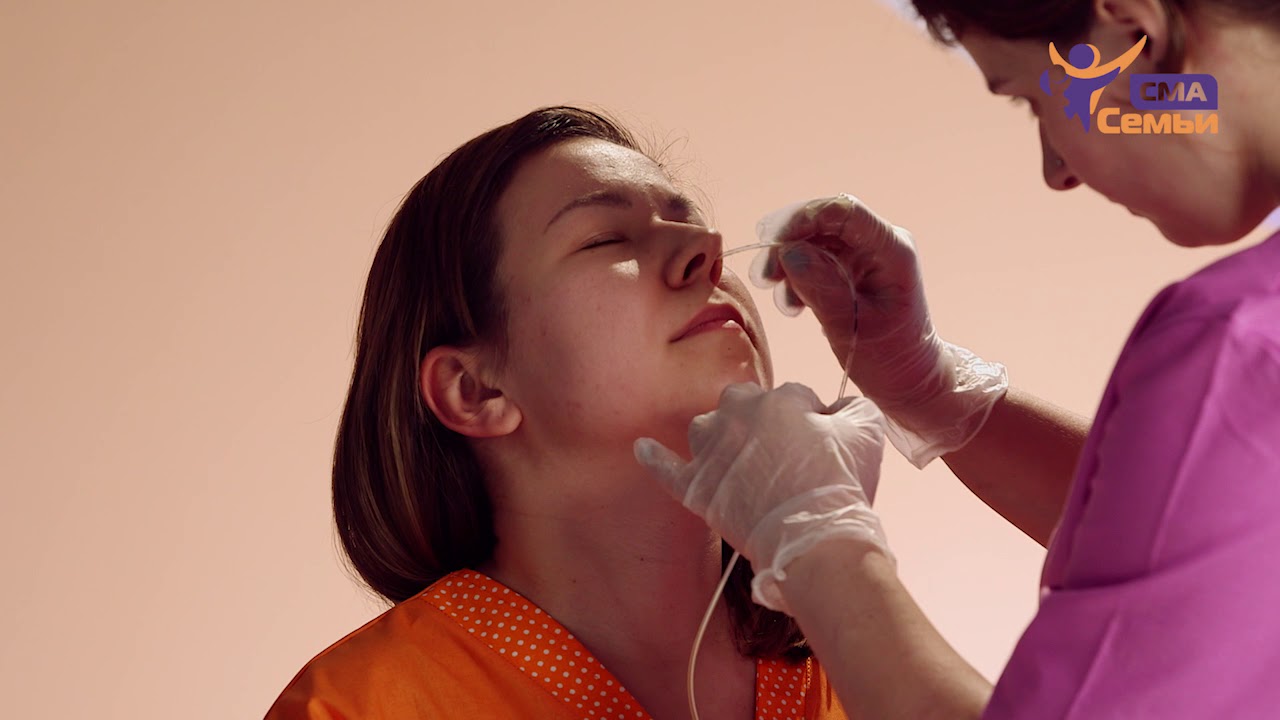
Назогастральный зонд (НГЗ)
Назогастральный зонд — это тонкая гибкая трубка, которая вводится через нос в желудок. Преимущества НГЗ:
- Простота установки у постели больного
- Возможность быстрого начала питания
- Подходит для краткосрочного использования (до 4-6 недель)
Недостатки НГЗ включают риск смещения зонда и дискомфорт для пациента.
Чрескожная эндоскопическая гастростома (ЧЭГ)
ЧЭГ предполагает установку питательной трубки непосредственно в желудок через переднюю брюшную стенку. Преимущества ЧЭГ:
- Более надежная фиксация
- Возможность длительного использования
- Меньший риск аспирации
Однако ЧЭГ требует хирургического вмешательства и связана с риском осложнений.
Осложнения энтерального питания через зонд
При проведении зондового питания у пациентов после инсульта могут возникнуть следующие осложнения:
Механические осложнения
- Смещение или закупорка зонда
- Повреждение слизистой носа и пищевода
- Аспирация содержимого желудка
Желудочно-кишечные осложнения
- Тошнота и рвота
- Диарея или запор
- Вздутие живота
Метаболические нарушения
- Дисбаланс электролитов
- Гипергликемия
- Дегидратация
Профилактика и устранение осложнений
Для предотвращения осложнений зондового питания необходимо:
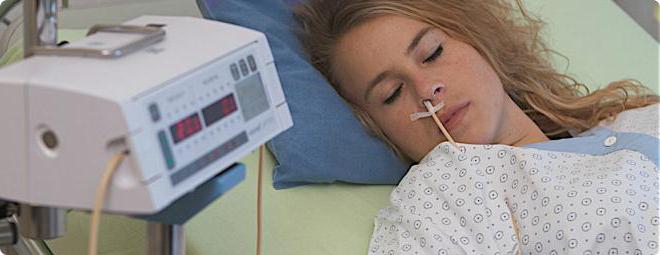
- Правильно подбирать состав и скорость введения питательных смесей
- Регулярно проверять положение зонда
- Соблюдать правила асептики при уходе за зондом
- Контролировать баланс жидкости и электролитов
- Своевременно выявлять и устранять осложнения
При возникновении осложнений может потребоваться коррекция режима питания, замена зонда или временное прекращение энтерального питания.
Когда следует начинать энтеральное питание после инсульта?
Оптимальные сроки начала зондового питания у пациентов после инсульта являются предметом обсуждения. Некоторые исследования показывают следующее:
- Раннее начало питания (в первые 24-48 часов) связано с лучшими исходами
- Отсрочка питания более чем на 7 дней повышает риск осложнений
- Оптимальный срок — в течение 72 часов после поступления в стационар
Однако решение о начале зондового питания должно приниматься индивидуально с учетом состояния пациента.
Как долго может потребоваться зондовое питание после инсульта?
Длительность зондового питания зависит от тяжести инсульта и динамики восстановления функции глотания:
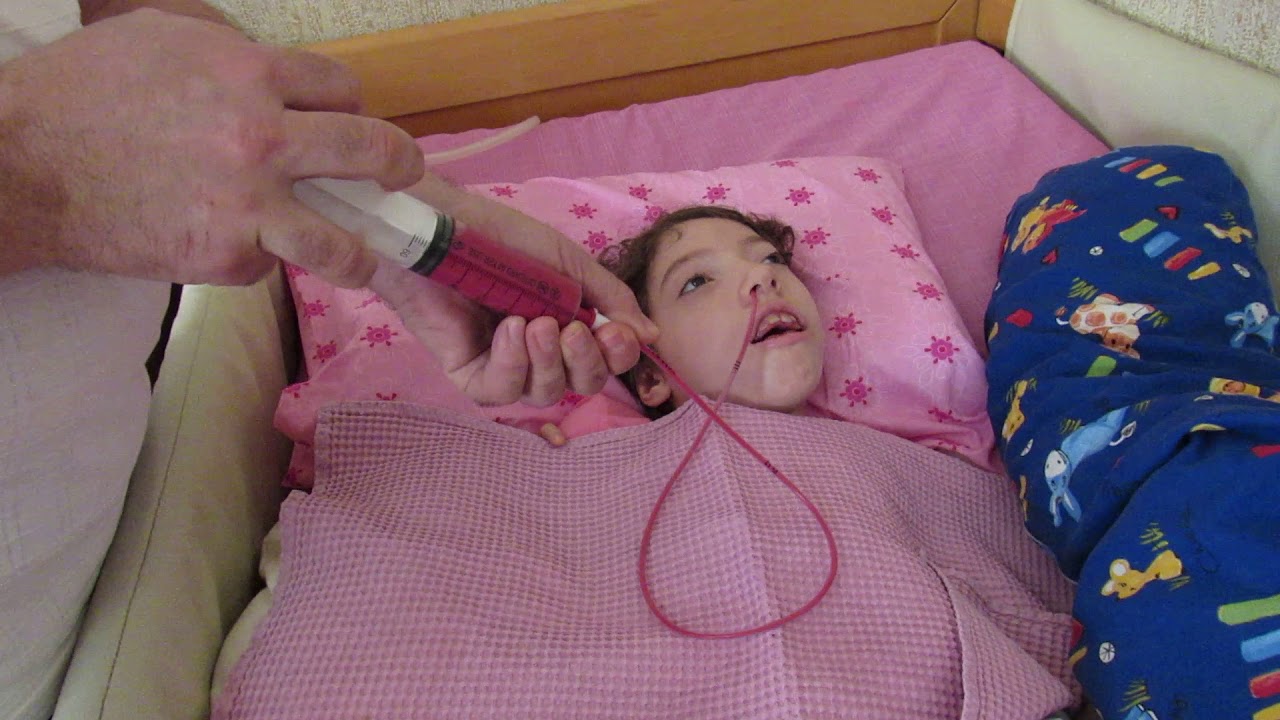
- У 30-50% пациентов дисфагия разрешается в течение 2-4 недель
- У 15-20% пациентов нарушение глотания сохраняется более 6 месяцев
- В среднем длительность зондового питания составляет 2-3 месяца
Важно регулярно оценивать возможность перехода на пероральное питание и своевременно удалять зонд при восстановлении глотания.
Можно ли сочетать зондовое и пероральное питание?
Переход от зондового к пероральному питанию обычно происходит постепенно. При этом возможно сочетание двух методов:
- Дополнение зондового питания небольшими порциями пищи через рот
- Пероральный прием пищи днем и зондовое питание ночью
- Использование загустителей для облегчения глотания жидкостей
Такой подход позволяет стимулировать восстановление глотания при сохранении адекватного питания пациента.
Особенности ухода за пациентом с зондовым питанием
Уход за пациентом, получающим энтеральное питание через зонд, включает следующие аспекты:
- Контроль положения зонда перед каждым кормлением
- Промывание зонда до и после введения питательной смеси
- Уход за полостью рта и носа
- Контроль объема вводимой смеси и остаточного содержимого желудка
- Наблюдение за стулом и диурезом
- Профилактика пролежней при длительном постельном режиме
Важно обучить родственников пациента правилам ухода при выписке из стационара.
Заключение
Энтеральное питание через зонд является важным компонентом лечения пациентов после инсульта с нарушением глотания. Правильный выбор метода питания, своевременное начало и адекватный уход позволяют улучшить исходы и качество жизни пациентов. Необходимо помнить о возможных осложнениях и своевременно их предотвращать.
Клинические рекомендации DGEM по энтеральному питанию пациентов перенесших инсульт
Клинические рекомендации DGEM по энтеральному питанию пациентов перенесших инсульт (на основании данных немецкого комитета клинического питания DGEM).
Инсульт часто сопровождается дисфагией и другими факторами, связанными с пониженным потреблением пищи.Дисфагия с аспирационной пневмонией и недостаточным питанием приводят к ухудшению прогноза после инсульта.
Данные рекомендации согласованы на нескольких консенсусных конференциях DGEM. В рекомендациях подчеркивается важность раннего скрининга и оценка дисфагии, необходимости избегать аспирации, недоедания и обезвоживания.
Такие пациенты не только склонны к обезвоживанию и недоеданию, но также имеют повышенный риск развития аспирационной пневмонией. Исследования показали увеличение риска этого осложнения до 12 раз у пациентов с инсультом и признаками дисфагии
Поэтому раннее выявление инсульта, дисфагии и подбор соответствующего питания имеют огромное клиническое значение.

Скрининг и оценка дисфагии при инсульте
Какие методы следует использовать для скрининга на дисфагию?
Как следует оценивать риск аспирации?
Рекомендация 1
Должен быть проведен формализованный скрининг на дисфагию у всех пациентов с острым инсультом (уровень рекомендации B) в рамках первичного осмотра или по прибытии пациента в стационар, в течение нескольких часов после госпитализации. Могут быть использованы следующие методы:
1. Тест глотания воды (WST)
2. Тест множественной согласованности (MST)
3. Провокационный глотательный тест (PST)
Каким пациентам показан тест на дисфагию?
Рекомендация 2
Всем пациентам с инсультом не прошедшим скрининг на дисфагию необходимо провести один из методов тестирования (B).
Рекомендация 3
Пациенты с инсультом без признаков дисфагии на основании первичной оценки этого симптома должны быть направлены на дальнейшую оценку функции глотания, если присутствуют такие предикторы дисфагии, как тяжелый неврологический дефицит, выраженная дизартрия, афазия или паралич лицевого нерва (B).
Какие методы должны быть использованы для оценки дисфагии?
Рекомендация 4
Клиническая оценка у постели больного: может быть проведена обученным персоналом (C).
Инструментальная оценка дисфагии: ограниченная возможность клинического тестирования говорит о том, что надежная, своевременная и экономически оправданная инструментальная оценка глотания у пациентов с острым инсультом может быть применена, такие как видеофлюороскопическое исследование (VFSS), а также исследование глотательных функций при помощи волоконно-оптического микроскопа (FEES).
Рекомендация 6
Оценка дисфагии должна проводиться как можно раньше.
Насколько регулярно необходимо проводить оценку дисфагии?
Рекомендация 7
В первые дни болезни клиническую оценку дисфагии у пациентов с инсультом необходимо проводить ежедневно. Если дисфагия сохраняется, клиническая оценка повторяется дважды в неделю и перед выпиской (С).
Рекомендация 8
Если дисфагия сохраняется после выписки, обследование нужно проводить делать не реже одного раза в месяц в течение 6 месяцев после инсульта (С).
Какую шкалу использовать для оценки дисфагии?
Рекомендация 9
В зависимости от метода оценки дисфагии выбирается соответствующая шкала, например
Оценка нутритивного статуса у пациентов после инсульта
Когда и каким образом следует оценивать нутритивные риски пациентов?
Рекомендация 10
Все пациенты с инсультом должны быть скринированы на предмет нутритивных рисков в течение первого дня после госпитализации.
Рекомендация 11
Пациенты с инсультом и нутритивным риском или с дисфагией должны быть обследованы более углубленно.
Есть ли необходимость в зондовом питании для пациентов со сниженным уровнем сознания и находящимся на механической вентиляции легких получают ли пользу от зондового питания
Рекомендация 12
Пациентам со сниженным уровнем сознания и находящимся на механической вентиляции часто требуется энтеральное питание в течение длительного времени и зондовое питание должно начинаться как можно раньше (C).
Есть ли необходимость в энтеральном питании через зонд для пациентов с предположительно длительной дисфагией ?
Рекомендация 13
Пациенты с длительной тяжелой дисфагией более 7 дней должны получать зондовое питание.
Когда следует начинать нутритивную поддержку пациентам с инсультом с затруднениями глотания?
Рекомендация 14
При тяжелых нарушениях глотания, при которых нормальный прием пищи не возможен и предполагаемо эти симптомы продолжаются более 1 недели необходимо подключать раннее зондовое энтеральное питание.
Какой способ энтерального питания предпочтителен?
Каковы показания для назогастрального зонда или установки гастростомы?
Рекомендация 15
Если в период острой фазы инсульта пероральное питание невозможно, необходимо проводить энтеральное питание через назогастральный зонд (A).
Рекомендация 16
Если предполагается энтеральное питание в течение длительного периода времени
(более 28 дней), следует предпочесть гастростому, которая устанавливается при стабильном клиническом состоянии (через 14 — 28 дней) (А).
Рекомендация 17
Пациенты с инсультом на ИВЛ должны получать энтеральное питание через гастростому на ранней стадии (В).
Рекомендация 18
Если назогастральный зонд случайно удален пациентом, и необходимо продолжать искусственное питание более 14 дней, следует рассмотреть возможность установки гастростомы (B), как альтернатива – установка носовой петли на назогастральный зонд (B).
Уменьшает ли установка зонда в двенадцатиперстную или тощую кишку риск аспирации у пациентов с инсультом?
Рекомендация 19
Зонд для кормления следует вводить в желудок (B). Установка желудочного зонда не представляет повышенного риска возникновения аспирационной пневмонии, по сравнению с размещением зонда в двенадцатиперстной или тощей кишки.
Подачу энтерального питания через зонд осуществлять непрерывно или болюсно?
Рекомендация 20
Если в анамнезе есть гастроэзофагеальный рефлюкс или если есть признаки гастроэзофагеального рефлюкса с аспирацией или имеется высокий риск аспирации следует осуществлять непрерывную подачу энтерального питания(В).
Рекомендация 21
При установке зонда в двенадцатиперстную или тощую кишку следует осуществлять непрерывную подачу питания.
Энтеральное питание через зонд следует осуществлять с помощью насоса или гравитационным способом?
Рекомендация 22
У пациентов с инсультом предпочтительно насос для зондового питания
Мешает ли кормление через назогастральный зонд обучению глотанию и реабилитации?
Рекомендация 23
Питание через назогастральный зонд не мешает обучению глотанию. Поэтому следует начинать терапию дисфагии как можно раньше, даже у пациентов, находящихся на зондовом питании (A).
Поэтому следует начинать терапию дисфагии как можно раньше, даже у пациентов, находящихся на зондовом питании (A).
Рекомендация 24
Если есть необъяснимое ухудшение дисфагии, необходимо эндоскопически контролировать положение зонда в глотке (B).
Следует ли пациентам с дисфагическим инсультом, находящимся на зондовом питании, быть
посоветовали дополнительно пероральное питание?
Рекомендация 25
Большинство пациентов с инсультом и дисфагией находящиеся в сознании при кормлении через зонд должны дополнительно принимать питание перорально, в соответствии с происхождением и степенью тяжести дисфагии (B).
В какой ситуации показано парентеральное питание пациентов с инсультом?
Рекомендация 26
Парентеральное показано в тех случаях, когда энтеральное питание противопоказано или невыполнимо.
Рекомендация 27
Даже у пациентов с нормальным нутритивным статусом следует проводить парентеральное питание, если энтеральное питание не удовлетворяет нутритивные потребности более семи дней.
Рекомендация 28
Если нормальное поступление жидкости невозможно обеспечить при пероральном или энтеральном питании, следует немедленно применить парентеральную гидратацию.
Какие пациенты должны получать пероральное питание (сипинг)?
Рекомендация 29
Пациенты с инсультом, которые могут есть и подвержены риску недостаточности питания, с установленной недостаточностью питания, а также с риском развития пролежней, должны получать пероральное питание (В).
Показаны ли больным с дисфагией пищевые продукты с добавлением загустителей?
Рекомендация 30
После оценки акта глотания (например, клинически или видеофлюороскопическим или эндоскопическим методами) следует обеспечить питание с загустителем в безопасной консистенции.
Рекомендация 31
Необходима консультация диетолога и организация нутритивной поддержки в случаях недостаточного потребления пищи в течение длительного периода времени (С).
Что можно есть после инсульта: основные правила и меню
Если не будете есть пищу как лекарство,
Будете есть лекарство как пищу.
Стив Джобс
Для людей, перенесших инсульт, жизненно необходимым становится решение двух задач: восстановление (реабилитация) и недопущение повторного нарушения мозгового кровообращения. Важнейшим компонентом в их решении является лечебное питание. Несмотря на различные причины, вызывающие заболевания, рацион после ишемического и геморрагического инсульта сходен.
На начальном этапе восстановления прием привычной пищи естественным путем сильно ограничен или полностью невозможен. Зачастую больной парализован, имеет нарушение глотательной функции, ему вводится большой объем лекарственных препаратов. Для того чтобы питание в этот период было полноценным, достаточным, правильно сбалансированным и легко усваивалось, применяются специальные питательные смеси.
Их смешивают с кипяченой водой комнатной температуры и применяют как жидкое питание через рот.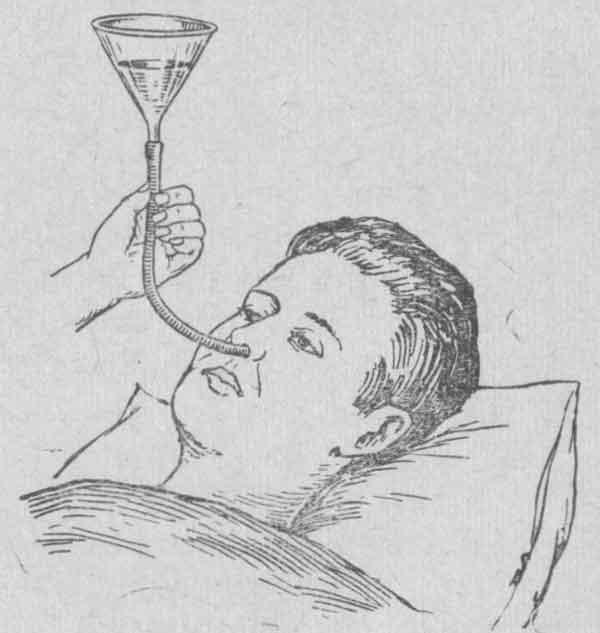
Пациентам, имеющим проблемы с глотанием, приготовленная смесь подается через специальный медицинский зонд.
В кардиологическом санаторном центре Переделкино для людей, перенесших инсульт, разработана и успешно применяется медицинская программа Восстановление.
Когда больной после выписки возвращается домой, его рацион питания можно постепенно разнообразить. Делать это можно только если он способен нормально жевать и проглатывать твердую пищу.
Питание больного после инсульта
Диета в постинсультный период содержит следующие основные правила:
1. В еде должно присутствовать достаточное количество белков.
Физиологическая суточная норма белка составляет 90-100 г. Включите в меню свежий творог, постное мясо и рыбу, яичный белок, гречневую и овсяную крупу.
2. Снижаем калорийность рациона.
Общее количество калорий в ежедневном рационе не должно превышать 2500-2600 ккал, при наличии избыточного веса — не более 2000-2200 ккал. При дефиците массы тела, энергетическая ценность должна быть несколько выше, примерно 2800-3000 ккал
При дефиците массы тела, энергетическая ценность должна быть несколько выше, примерно 2800-3000 ккал
3. Ограничиваем потребление соли, жидкости и сахара.
Переизбыток поваренной соли способствует повышению артериального давления.
Учёные из Массачусетского университета провели исследование, в рамках которого изучили статистику смертности от различного вида заболеваний. Специалисты изучили данные о зависимости между питанием и болезнями.
В результате исследования было установлено, что если человек питается, не соблюдая баланс белков, жиров и углеводов, при этом отдавая предпочтение соленой пище, то шанс возникновения инсульта или сахарного диабета увеличивается в два раза. Также пища с большим содержанием соли неблагоприятно влияет на сердце и сосуды
Количество поваренной соли снижаем до 6 г в день, а в период обострения она исключается совсем (кроме 2-3 г, содержащихся в самих продуктах). Все соленые и маринованные продукты под запретом.
Важно! Все блюда готовятся без добавления соли, можно слегка подсолить их перед едой.
Свободная жидкость (помимо содержащейся в пище) — 1,2 л Индивидуальный объем следует обговорить с лечащим врачом.
4. Исключаем из рациона животные и кулинарные жиры.
Необходимо для того чтобы снизить уровень холестерина в крови, очистить сосуды от атеросклеротических бляшек и восстановить нормальный ток крови в артериях.
Вместо них используем растительные — подсолнечное, льняное, оливковое, рапсовое масло.
5. Рацион должен содержать достаточное количество витаминов и минералов.
(о витаминах и минералах подробно в разделе «Продукты, рекомендуемые в пищу, после инсульта» )
6. Запрещены все блюда, возбуждающие деятельность нервной и сердечно-сосудистой систем.
Кофе, крепкий чай, шоколад, любые алкогольные напитки, газированные сладкие напитки.
Мясные и рыбные бульоны, острые закуски и приправы, грибные навары.
Категорически запрещается употреблять полуфабрикаты, фаст-фуд и подобные вредные продукты.
7. Дробный прием пищи.
Принимать пищу следует 4-5 раз в день, небольшими порциями. Обильная еда противопоказана.
Последний прием пищи осуществлять не позднее чем за 3-4 часа до сна.
8. Добавляем в рацион морепродукты.
Морская капуста, крабы, омары, кальмары, креветки и т.д. содержат полиненасыщенные жирные кислоты, триглицериды омега-3, которые снижают уровень холестерина и поддерживают эластичность суставов.
Диета при гипертонической болезни 3 стадии с нарушением мозгового кровообращения или с его недостаточностью
Белки — 60 г
жиры — 60 г
углеводы — 250-300 г
поваренная соль — нет
свободная жидкость — 0,6 л.
Масса суточного рациона 1,5-2 кг
энергетическая ценность 1800-2000 ккал.
Готовить без соли, подавать еду протертой, в теплом виде.
Питание дробное — 6 раз в день.
Применяется не более двух недель, т.к. данная диета физиологически неполноценная.
Рекомендуется: хлеб белый вчерашней выпечки и несдобное печенье без соли, вегетарианские супы из протертых овощей и круп (полпорции), постные мясо и рыба в молотом виде. В протертом виде или вареные морковь, картофель, свекла, цветная капуста, кабачки, тыква.
В протертом виде или вареные морковь, картофель, свекла, цветная капуста, кабачки, тыква.
Каши из различных круп на воде с молоком, протертые или хорошо разваренные. Яйца всмятку в блюдах, омлет на пару. Кефир, простокваша, творог.
Спелые и мягкие фрукты и ягоды, фруктовые овощные соки отвар шиповника.
Больным с повышенным уровнем сахара в крови следует с осторожностью употреблять бананы. Они могут вызвать неконтролируемый скачок глюкозы. Соблюдайте простые правила: не ешьте их на пустой желудок, не запивайте, не ешьте помногу за раз. Бананы должны быть свежими, с чистой кожурой, с твердой мякотью без коричневых пятен.
Мед, размоченная курага, чернослив.
Исключить: хлеб с добавление поваренной соли и печенье с пищевой содой. Мясные, рыбные и грибные бульоны, молочные супы, щи, борщи, жирные мясо и рыба, консервы, копчености, сыр, кулинарные жиры.
Пшено, ячневые и перловая крупа, макароны, бобовые. Грибы, соленые маринованные и квашеные овощи. Виноград, шоколад,, кремовые изделия. Холодные закуски, соусы, пряности.
Виноград, шоколад,, кремовые изделия. Холодные закуски, соусы, пряности.
Какао, кофе, виноградный сок, газированные и алкогольные напитки, минеральная вода с высоким содержанием натрия.
Примерное меню:
1-й завтрак: омлет паровой, овсяная каша без соли, некрепкий зеленый чай.
2-й завтрак: фруктовое желе.
Обед: курица отварная с картофельным пюре, фруктовый кисель.
Полдник: свежие фрукты или ягоды.
Ужин: творожно-морковная запеканка со сметаной.
На ночь: стакан кефира.
На весь день: хлеб белый — 200 г.
Примерное меню при заболеваниях сосудов в стадии компенсации или недостаточности кровообращения 1-2А стадии, при гипертонической болезни 1-2 стадии, атеросклерозе
1-й завтрак: омлет из двух яиц, чай с молоком.
2-й завтрак: нежирный творог.
Обед: Суп овощной, мясные котлеты, приготовленные на пару, гречневая каша.
Ужин: нежирная отварная рыба, тушеная капуста, отвар шиповника.
На ночь: стакан ряженки.
На весь день: белый хлеб — 250 г, черный — 100 г, сахар — 30 г, сливочное масло — 20г.
(Сахар лучше заменить натуральным медом)
Правильное питание необходимо, чтобы перестроить клетки головного мозга.
Льняное, подсолнечное, рапсовое, оливковое масло.
Это источники ненасыщенных жирных кислот, необходимых для нормального функционирования мозга.
Цветная капуста, сельдерей, огурцы, соя, грецкие орехи, зерна пшеницы, печень трески, рыба, мясо.
Источники фосфора, серы, цинка, кальция, железа и магния.
Фосфор и его соединения способствуют образованию клеток мозга.
Капуста, морковь, огурцы, крыжовник, земляника, лук, картофель, редис, яичный желток.
Источники серы, необходимой для насыщения клеток мозга кислородом.
Салат-латук, листья салата, подсолнечное масло, печень, яичный желток.
Источники витамина Е, который регулирует деятельность мозжечка.
Ореховое масло, орехи, цельные зерна, полированный рис.
Зеленые овощи — зелень горчицы, шпинат, капуста. Апельсины, грейпфруты, дыня, авокадо, бананы. Продукты из молока, говядина, говяжья печень.
Продукты из молока, говядина, говяжья печень.
Эта пища богата витаминами группы В, дефицит которых может привести к проблемам памяти.
Черника, клубника, малина, ежевика, клюква.
Источники физетина и флавоноидов. Укрепляют стенки сосудов, стимулируют работу головного мозга.
Картофель, петрушка, редис, лук, помидоры.
Эти продукты способствуют насыщению клеток мозга кислородом.
Уважаемые читатели, статьи носят ознакомительный характер. Перед применением рекомендаций необходимо проконсультироваться с врачом.
Энтеральное зондовое питание для пациентов с дисфагическим инсультом
Обзор
. 2015 Feb;24(3):138, 140, 142-5. doi: 10.12968/bjon.2015.24.3.138.Энн Роват 1
принадлежность
- 1 Преподаватель, Школа медсестер, акушерства и социального обеспечения, Эдинбургский университет Нейпира.

- PMID: 25679242
- DOI: 10.12968/bjon.2015.24.3.138
Обзор
Энн Роват. Бр Дж Нурс. 2015 Февраль
. 2015 Feb;24(3):138, 140, 142-5. дои: 10.12968/bjon.2015.24.3.138.Автор
Энн Роват 1
принадлежность
- 1 Преподаватель, Школа медсестер, акушерства и социального обеспечения, Эдинбургский университет Нейпира.
- PMID: 25679242
- DOI:
10.
 12968/bjon.2015.24.3.138
12968/bjon.2015.24.3.138
Абстрактный
Зонды для энтерального питания, назогастральный зонд (НГТ) или чрескожная эндоскопическая гастростомия (ЧЭГ) обычно используются для обеспечения питания, гидратации и необходимых лекарств пациентам, перенесшим инсульт, которые не могут глотать. Раннее зондовое питание связано с улучшением выживаемости после инсульта, поэтому пациентам рекомендуется начинать зондовое питание в течение 24 часов после госпитализации. Кормление NGT является предпочтительным методом кратковременного кормления в острой фазе инсульта, поскольку его преимущество заключается в том, что его легко разместить у постели больного. Однако часто возникают трудности с введением назогастрального зонда, и он может быть легко смещен возбужденными и сбитыми с толку пациентами, что может привести к потенциально фатальным осложнениям. Трубка ЧЭГ считается более безопасным методом питания пациентов с инсультом, которым требуется более длительная пищевая поддержка, но это инвазивная процедура, которая может привести к осложнениям, связанным с повышенным риском заболеваемости и смертности после инсульта. Цель этой статьи — рассмотреть осложнения, связанные с энтеральным зондовым питанием, и обсудить их профилактику и лечение пациентов с инсультом.
Цель этой статьи — рассмотреть осложнения, связанные с энтеральным зондовым питанием, и обсудить их профилактику и лечение пациентов с инсультом.
Ключевые слова: осложнения; Дисфагия; назогастральный зонд; Чрескожная эндоскопическая гастростомия; Гладить.
Похожие статьи
- Проспективное сравнение чрескожной эндоскопической гастростомы и кормления через назогастральный зонд у пациентов с острым дисфагическим инсультом.
Хамидон Б.Б., Абдулла С.А., Завави М.Ф., Сукумар Н., Аминуддин А., Раймонд А.А. Хамидон Б.Б. и др. Med J Малайзия. 2006 март; 61 (1): 59-66. Med J Малайзия. 2006. PMID: 16708735 Клиническое испытание.
- Носовая петля представляет собой альтернативу чрескожной эндоскопической гастростоме у пациентов с высоким риском дисфагического инсульта.

Андерсон М.Р., О’Коннор М., Майер П., О’Махони Д., Вудворд Дж., Кейн К. Андерсон М.Р. и соавт. Клин Нутр. 23 августа 2004 г. (4): 501-6. doi: 10.1016/j.clnu.2003.09.008. Клин Нутр. 2004. PMID: 15297085
- Энтеральное питание при лечении рака головы и шеи: предпочтительнее ли чрескожная эндоскопическая гастростомическая трубка, чем назогастральный зонд?
Mekhail TM, Adelstein DJ, Rybicki LA, Larto MA, Saxton JP, Lavertu P. Мехаил ТМ и др. Рак. 2001 г. 1 мая; 91 (9): 1785-90. Рак. 2001. PMID: 11335904
- Использование энтерального питания при лечении инсульта.
Оджо О, Брук Дж. Оджо О и др. Питательные вещества. 20 декабря 2016 г .; 8 (12): 827. дои: 10.3390/nu8120827. Питательные вещества.
 2016.
PMID: 27999383
Бесплатная статья ЧВК.
Обзор.
2016.
PMID: 27999383
Бесплатная статья ЧВК.
Обзор. - Энтеральное питание и чрескожная эндоскопическая гастростомия.
Холмс С. Холмс С. Стенд Нурс. 2004 г., 28 января — 3 февраля; 18 (20): 41–3. doi: 10.7748/ns2004.01.18.20.41.c3536. Стенд Нурс. 2004. PMID: 14976704 Обзор.
Посмотреть все похожие статьи
Цитируется
- Истощенный постинсультный мужчина с множественными заболеваниями и риском саркопении в клинике длительного инсульта: отчет о клиническом случае.
Тай С.Л., Исхак Н.Х., Али М.Ф., Завави Н.С.М., Абд Азиз Н.А. Тай С.Л. и соавт. Малайский семейный врач. 2023 2 марта; 18:12. doi: 10.51866/cr.281. Электронная коллекция 2023. Малайский семейный врач.
 2023.
PMID: 37139474
Бесплатная статья ЧВК.
2023.
PMID: 37139474
Бесплатная статья ЧВК. - Сравнение между чрескожной эндоскопической гастростомией и назогастральным кормлением у 160 пациентов с нарушениями глотания: двухлетнее последующее исследование.
Ду Г, Лю Ф, Ма Х, Чен С, Дай М, Вэй Л, Лю З. Ду Г и др. Clin Interv Старение. 2022 5 декабря; 17:1803-1810. doi: 10.2147/CIA.S389891. Электронная коллекция 2022. Clin Interv Старение. 2022. PMID: 36506851 Бесплатная статья ЧВК.
- Время установки чрескожной эндоскопической гастростомической трубки у пациентов, перенесших инсульт, не влияет на смертность, осложнения или исходы.
Редди К.М., Ли П., Гор П.Дж., Чизман А., Аль-Хаммади Н., Вестрич Д.Дж., Тейлор Дж. Редди К.М. и др. World J Gastrointest Pharmacol Ther. 2022 5 сентября; 13 (5): 77-87.
 дои: 10.4292/wjgpt.v13.i5.77. Epub 2022 9 мая.
World J Gastrointest Pharmacol Ther. 2022.
PMID: 36157266
Бесплатная статья ЧВК.
дои: 10.4292/wjgpt.v13.i5.77. Epub 2022 9 мая.
World J Gastrointest Pharmacol Ther. 2022.
PMID: 36157266
Бесплатная статья ЧВК. - Роль фармацевта в выборе наилучшего выбора лекарственной формы у пациентов с дисфагией.
Зуккари Г., Масис С., Алфей С., Маркитто Л., Руссо Э. Зуккари Г. и соавт. J Pers Med. 2022 12 августа; 12 (8): 1307. дои: 10.3390/jpm12081307. J Pers Med. 2022. PMID: 36013259 Бесплатная статья ЧВК.
- Библиометрический анализ тенденций мировых исследований постинсультной пневмонии: текущее состояние развития и границы исследований.
Ли С, Ю Дж, Шу С. Ли Х и др. Фронт общественного здравоохранения. 2022 2 августа; 10:950859. doi: 10.3389/fpubh.2022.950859. Электронная коллекция 2022. Фронт общественного здравоохранения.
 2022.
PMID: 35983361
Бесплатная статья ЧВК.
2022.
PMID: 35983361
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
Использование энтерального питания при лечении инсульта
Питательные вещества. 2016 декабрь; 8(12): 827.
Опубликовано в сети 20 декабря 2016 г. doi: 10.3390/nu8120827
1, * и 2
900 02 Информация об авторе Примечания к статье Информация об авторских правах и лицензиях Отказ от ответственности В этой статье обсуждается Использование энтерального питания при лечении инсульта. Инсульт является основной причиной инвалидности, включая дисфагию. Клинические проявления затруднения глотания у пациентов, перенесших инсульт, могут привести к недостаточности питания, что влияет на состояние здоровья и клинические исходы, включая заболеваемость, смертность и затраты на службу здравоохранения. Распространенность недостаточности питания после острого инсульта может варьироваться от 8% до 34%. Поэтому становится актуальной необходимость разработки и внедрения методов энтеральной нутритивной поддержки у больных, перенесших инсульт. Для поддержки пациентов с инсультом, которые не могут удовлетворить свои потребности в питании только за счет перорального питания, можно использовать ряд энтеральных зондов и методов питания, хотя каждый из этих подходов имеет свои преимущества и ограничения. На основании этого обзора получены доказательства того, что энтеральное питание является полезным методом обеспечения питания пациентов с дисфагией после инсульта для улучшения их нутритивного статуса и укрепления их здоровья. Однако существуют проблемы с использованием энтерального зондового питания у этих пациентов.
Распространенность недостаточности питания после острого инсульта может варьироваться от 8% до 34%. Поэтому становится актуальной необходимость разработки и внедрения методов энтеральной нутритивной поддержки у больных, перенесших инсульт. Для поддержки пациентов с инсультом, которые не могут удовлетворить свои потребности в питании только за счет перорального питания, можно использовать ряд энтеральных зондов и методов питания, хотя каждый из этих подходов имеет свои преимущества и ограничения. На основании этого обзора получены доказательства того, что энтеральное питание является полезным методом обеспечения питания пациентов с дисфагией после инсульта для улучшения их нутритивного статуса и укрепления их здоровья. Однако существуют проблемы с использованием энтерального зондового питания у этих пациентов.
Ключевые слова: энтеральное питание, инсульт, чрескожная эндоскопическая гастростомия, назогастральный зонд, энтеральное зондовое питание. У большинства из этих людей есть неврологические заболевания, такие как инсульт, которые влияют на процесс глотания, вызывая дисфагию.
Независимо от основного заболевания, продукты для поддержки питания обеспечивают организм белком, энергией, минералами и витаминами. Эти продукты можно давать в виде пероральных пищевых добавок (ONS), когда нет противопоказаний, таких как дисфагия, или их можно вводить через зонд для энтерального питания [1]. Существует ряд зондов для энтерального питания с различными показаниями, которые можно использовать при лечении пациентов после инсульта. Краткосрочные вмешательства включают введение назогастрального зонда (НГТ), в то время как долгосрочная нутритивная поддержка включает введение чрескожной эндоскопической гастростомы (ЧЭГ) [2]. Однако у обоих подходов есть преимущества и недостатки. В этой статье обсуждаются важные аспекты планирования индивидуальной помощи и ведения пациентов, перенесших инсульт.
В руководстве Национального института здравоохранения и качества медицинской помощи (NICE) [3] используется определение инсульта, данное Всемирной организацией здравоохранения (ВОЗ): «быстро развивающиеся клинические признаки очагового (иногда глобального) нарушения мозговой функции, длящиеся более 24 часов». ч или привести к смерти без видимой причины, кроме причины сосудистого происхождения». Инсульт имеет сосудистое происхождение, так как связан с нарушением притока крови к мозгу, что может произойти в результате окклюзии (ишемический инсульт) или разрыва кровеносного сосуда (геморрагический инсульт) [4]. В Великобритании и США 85% и 87%, соответственно, обусловлены ишемической этиологией, а основными факторами риска являются курение и гиперхолестеринемия, тогда как основным фактором риска геморрагического инсульта является артериальная гипертензия [5,6,7,8]. Эти клинические проявления следует отличать от транзиторных ишемических атак (ТИА), которые являются симптомами инсульта, разрешающимися в течение 24 часов, и представляют собой быстро обратимые эпизоды фокальных неврологических состояний, которые могут привести к инсульту [3,9].]. Во всем мире инсульт остается второй наиболее распространенной причиной смерти, ежегодно унося примерно 6,7 миллиона жизней [10].
ч или привести к смерти без видимой причины, кроме причины сосудистого происхождения». Инсульт имеет сосудистое происхождение, так как связан с нарушением притока крови к мозгу, что может произойти в результате окклюзии (ишемический инсульт) или разрыва кровеносного сосуда (геморрагический инсульт) [4]. В Великобритании и США 85% и 87%, соответственно, обусловлены ишемической этиологией, а основными факторами риска являются курение и гиперхолестеринемия, тогда как основным фактором риска геморрагического инсульта является артериальная гипертензия [5,6,7,8]. Эти клинические проявления следует отличать от транзиторных ишемических атак (ТИА), которые являются симптомами инсульта, разрешающимися в течение 24 часов, и представляют собой быстро обратимые эпизоды фокальных неврологических состояний, которые могут привести к инсульту [3,9].]. Во всем мире инсульт остается второй наиболее распространенной причиной смерти, ежегодно унося примерно 6,7 миллиона жизней [10].
Последствия инсульта могут быть серьезными и включать в себя нарушение подвижности, коммуникации, дисфагию и депрессию [11]. Инсульт является наиболее частой причиной острой дисфагии, которая может привести к недостаточности питания и ухудшению качества жизни. Нарушение питания сразу после инсульта может снизить шансы на выживание, функциональную способность и условия проживания через полгода [12]. Распространенность недостаточности питания после острого инсульта колеблется от 8% до 34% [12]. Большинство пациентов после острого инсульта выздоравливают от дисфагии в течение первых четырех недель, хотя у 15% пациентов могут развиться длительные трудности с глотанием [11,13]. Дисфагия повлияет на способность пациентов самостоятельно поддерживать свои потребности в питании и гидратации [13].
Инсульт является наиболее частой причиной острой дисфагии, которая может привести к недостаточности питания и ухудшению качества жизни. Нарушение питания сразу после инсульта может снизить шансы на выживание, функциональную способность и условия проживания через полгода [12]. Распространенность недостаточности питания после острого инсульта колеблется от 8% до 34% [12]. Большинство пациентов после острого инсульта выздоравливают от дисфагии в течение первых четырех недель, хотя у 15% пациентов могут развиться длительные трудности с глотанием [11,13]. Дисфагия повлияет на способность пациентов самостоятельно поддерживать свои потребности в питании и гидратации [13].
В то время как 20% пациентов после инсульта могут нуждаться в энтеральном питании через зонд в острой фазе, 8% потребуется длительное энтеральное питание в течение более шести месяцев [14]. Предоставление энтерального питания не лишено риска потенциального вреда. Введение зонда ПЭГ, а не назогастрального тракта связано с меньшим желудочно-кишечным кровотечением и обеспечивает более высокую доставку корма [15].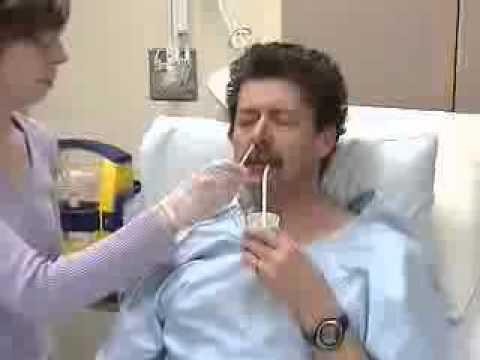 Зонды для энтерального питания полезны для обеспечения нутритивной поддержки после инсульта; однако такой подход к обеспечению питанием влияет на качество жизни пациента, вызывая дискомфорт, ограничение движений и потерю чувствительности, а также социальную интеграцию приема пищи [11]. Кроме того, из-за последствий инсульта у пациентов с дисфагией будет повышен риск регургитации и аспирации, которые являются осложнениями кормления НГТ [16].
Зонды для энтерального питания полезны для обеспечения нутритивной поддержки после инсульта; однако такой подход к обеспечению питанием влияет на качество жизни пациента, вызывая дискомфорт, ограничение движений и потерю чувствительности, а также социальную интеграцию приема пищи [11]. Кроме того, из-за последствий инсульта у пациентов с дисфагией будет повышен риск регургитации и аспирации, которые являются осложнениями кормления НГТ [16].
В руководстве Национального института здравоохранения и качества медицинской помощи (NICE) [3] указано, что крайне важно, чтобы все пациенты, перенесшие острый инсульт, проходили скрининг и оценивались на наличие проблем с глотанием должным образом обученным или лекарства. Процесс скрининга пациентов после инсульта часто используется в первую очередь для выявления тех, кто может подвергаться риску аспирации и, следовательно, требует направления на полную оценку к логопеду (SLT), который обладает навыками лечения дисфагии [17]. Обычно квалифицированная медсестра проводит скрининг пациентов с инсультом в условиях стационара неотложной помощи [17]. Пациентам с инсультом, у которых в процессе скрининга не выявлены проблемы с глотанием, может быть разрешено принимать пищу и питье перорально, пока ожидается полное обследование [17]. Таким образом, эти пациенты могут не нуждаться в нутритивной поддержке или энтеральном питании через зонд. Процесс скрининга пациентов с дисфагическим инсультом может включать тест на глотание воды, если это необходимо, и часто направлен на поиск безопасного метода обеспечения питания и гидратации этих пациентов [13,17]. Руководство NICE [3] рекомендует, чтобы, если скрининг при поступлении выявлял трудности с глотанием, оценка глотания проводилась в течение 24 часов после поступления и не более 72 часов. Дисфагия включает в себя ряд нарушений, которые могут повлиять на глотание, что может увеличить риск недоедания и обезвоживания [18]. НИЦЦА [19] также рекомендует проводить скрининг на недоедание и лиц, подверженных риску недоедания, медицинскими работниками в период госпитализации и один раз в неделю для стационарных пациентов.
Пациентам с инсультом, у которых в процессе скрининга не выявлены проблемы с глотанием, может быть разрешено принимать пищу и питье перорально, пока ожидается полное обследование [17]. Таким образом, эти пациенты могут не нуждаться в нутритивной поддержке или энтеральном питании через зонд. Процесс скрининга пациентов с дисфагическим инсультом может включать тест на глотание воды, если это необходимо, и часто направлен на поиск безопасного метода обеспечения питания и гидратации этих пациентов [13,17]. Руководство NICE [3] рекомендует, чтобы, если скрининг при поступлении выявлял трудности с глотанием, оценка глотания проводилась в течение 24 часов после поступления и не более 72 часов. Дисфагия включает в себя ряд нарушений, которые могут повлиять на глотание, что может увеличить риск недоедания и обезвоживания [18]. НИЦЦА [19] также рекомендует проводить скрининг на недоедание и лиц, подверженных риску недоедания, медицинскими работниками в период госпитализации и один раз в неделю для стационарных пациентов. Важно предусмотреть пищевую поддержку для людей, страдающих от недоедания — людей с низким индексом массы тела (<18,5 кг/м 2 ), людей с непреднамеренной потерей веса (> 10% в течение последних шести месяцев) и тех, у кого мало или совсем не ел в течение последних пяти дней или может есть мало или совсем не есть в течение пяти дней или дольше [19].
Важно предусмотреть пищевую поддержку для людей, страдающих от недоедания — людей с низким индексом массы тела (<18,5 кг/м 2 ), людей с непреднамеренной потерей веса (> 10% в течение последних шести месяцев) и тех, у кого мало или совсем не ел в течение последних пяти дней или может есть мало или совсем не есть в течение пяти дней или дольше [19].
Валидированный скрининг людей с риском недоедания включает использование универсального инструмента скрининга недоедания (MUST), который определяет риск недоедания как низкий риск (0 баллов), средний риск (1 балл) и высокий риск (2 балла или выше) ) [20]. Это позволит на раннем этапе выявить тех, кто недоедает или подвергается риску недоедания, и обеспечит проведение эффективных мероприятий. Оценка пациентов после инсульта должна включать питание и гидратацию [3]. Однако часто возникают проблемы, поскольку у пациентов могут быть трудности с общением, а проблемы с подвижностью или стоянием затрудняют измерение веса и роста [12].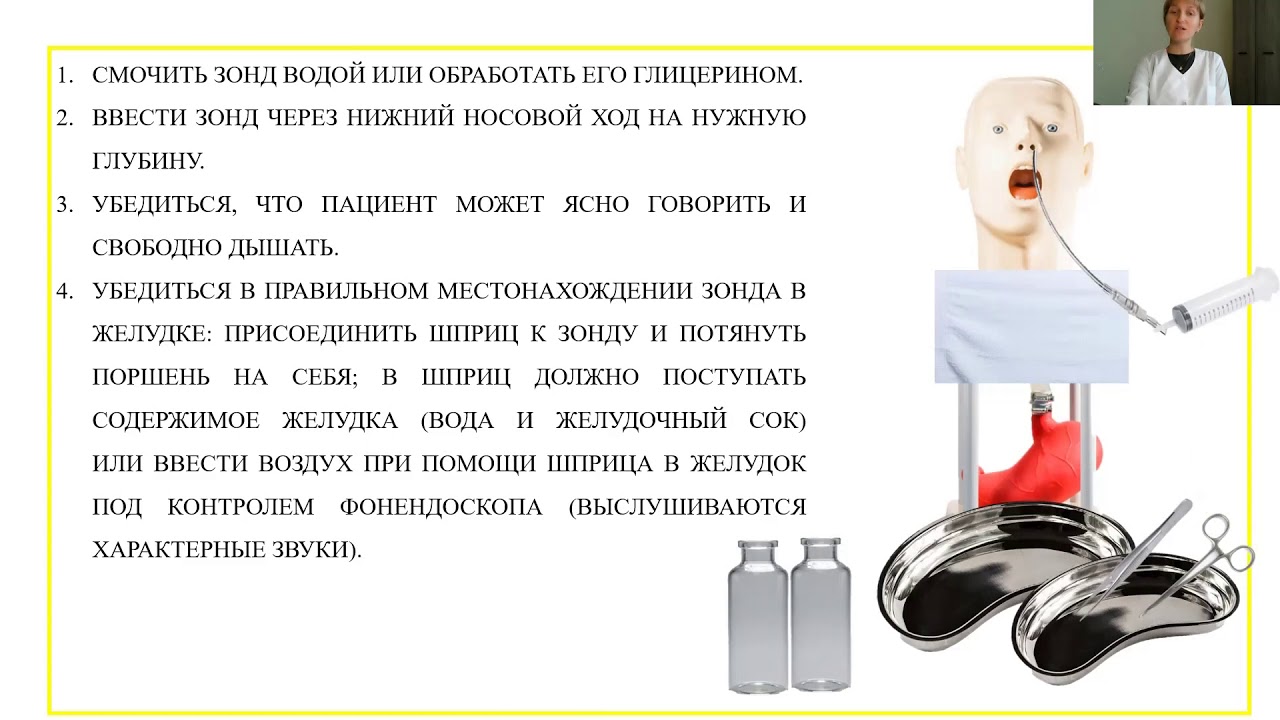
Если пациент не прошел глотательный тест и не может безопасно переносить пероральные жидкости или пищу, в течение 24 часов следует ввести назогастральный зонд [3,21]. Если пациент не может переносить назогастральный зонд, следует рассмотреть вопрос о назальной уздечке или гастростомической трубке, а также о направлении к соответствующим специалистам здравоохранения для оценки питания, индивидуального ухода и наблюдения за возможным направлением действий [3]. Важно, чтобы медицинские работники знали, что такие факторы, как дисфагия, плохая гигиена полости рта и нарушение способности к самостоятельному приему пищи, могут повлиять на состояние питания пациентов после инсульта [3]. Кроме того, может не быть необходимости в рутинных пищевых добавках для пациентов, которые адекватно питаются [3]. Тем не менее, для пациентов с риском недостаточности питания следует обеспечить пищевую поддержку в виде пероральных пищевых добавок и/или зонда для энтерального питания [3].
Роль служб поддержки питания заключается в устранении основной причины недостаточности питания или управлении высоким риском недостаточности питания [22]. Необходим комплексный подход к нутритивной поддержке [22]. В связи с этим услуги группы домашнего энтерального питания (HEN), многопрофильной команды, включающей медсестру-диетолога, диетолога и логопеда, представляют собой полезную платформу для оказания нутритивной поддержки в Великобритании [23].
Необходим комплексный подход к нутритивной поддержке [22]. В связи с этим услуги группы домашнего энтерального питания (HEN), многопрофильной команды, включающей медсестру-диетолога, диетолога и логопеда, представляют собой полезную платформу для оказания нутритивной поддержки в Великобритании [23].
В стационаре состояние питания пациентов после инсульта может ухудшиться, а недоедание после госпитализации связано с летальным исходом и плохим функциональным статусом [24]. Решения о начале нутритивной поддержки для пациентов после инсульта основываются на способе родоразрешения, будь то трубка NGT или PEG, раннее или позднее начало, продолжительность и должно ли питание предоставляться в течение дня или ночью. В Соединенном Королевстве различные режимы и подходы к обеспечению питанием были реализованы в фондах неотложной помощи Национальной службы здравоохранения (NHS) для пациентов после острого инсульта [24]. Тем не менее, важно, чтобы междисциплинарный подход к принятию решений относительно выбора назогастрального зонда или зонда ЧЭГ был предпринят [13, 23, 25].
Имеются медицинские показания для установки назогастральных трубок и ПЭГ-трубок, к ним относятся люди с острым инсультом, которые не могут переносить адекватное питание и жидкости перорально [3]. Еще одним показанием для установки трубки ЧЭГ могут быть пациенты с инсультом, которые не могут проглатывать достаточное количество пищи и жидкости перорально в течение четырех недель и имеют высокий риск недостаточности питания в долгосрочной перспективе [6, 25]. Однако размещение трубки ЧЭГ должно осуществляться по медицинским показаниям, а не по административным соображениям, и каждый случай следует рассматривать по существу, учитывая клиническую ситуацию, диагноз, прогноз и этические аспекты [25]. FOOD (Feed or Ordinary Diet) Trial Collaboration — это рандомизированное контролируемое исследование, проведенное в Великобритании с участием пациентов с дисфагией, поступивших в участвующие больницы с недавним инсультом [24]. Исходы пациентов с ЧЭГ по сравнению с НГТ продемонстрировали значительную разницу; пациенты с трубкой ЧЭГ чаще имели более высокую смертность и неблагоприятные исходы [24]. Возможным объяснением является потенциальное влияние зависимости от длительного кормления ПЭГ, поскольку пациенты, получавшие ПЭГ, все еще получали питание через трубку ПЭГ во время наблюдения по сравнению с пациентами, получавшими НГТ [24]. Кроме того, выжившие в группе ПЭГ имели более низкое качество жизни и с большей вероятностью жили в учреждениях по сравнению с теми, кто получал НГТ [24].
Возможным объяснением является потенциальное влияние зависимости от длительного кормления ПЭГ, поскольку пациенты, получавшие ПЭГ, все еще получали питание через трубку ПЭГ во время наблюдения по сравнению с пациентами, получавшими НГТ [24]. Кроме того, выжившие в группе ПЭГ имели более низкое качество жизни и с большей вероятностью жили в учреждениях по сравнению с теми, кто получал НГТ [24].
В недавнем исследовании пациентов с ишемическим инсультом и дисфагией сравнивали с пациентами с нормальной глотательной способностью [26]. Основываясь на результатах, пациенты, которым вводили назогастральный зонд, подвергались большему риску смертности по сравнению с теми, у кого не было назогастрального зонда/кормили перорально. Возможное предположение состоит в том, что введение NGT может создавать дополнительный риск пневмонии из-за колонизации ротоглотки патогенными бактериями, хотя эта позиция все еще обсуждается, поскольку считается, что большинство колоний имеют бактериальное происхождение [26].
Результаты этих исследований позволяют предположить, что существуют преимущества и ограничения использования зондов для энтерального питания у пациентов с дисфагией после инсульта. Сообщалось о плохих исходах у пациентов с трубкой ЧЭГ, у которых был больший риск развития пролежней, чем у пациентов с НГТ, возможно, из-за ограниченной подвижности и различных подходов к уходу [24]. Дополнительным соображением использования NGT в этой когорте пациентов является влияние инсульта на когнитивные способности, а уровень спутанности сознания может привести к тому, что некоторые пациенты сместят свой NGT, подвергая их дальнейшему риску осложнений [24]. Это также было подтверждено Rowat [11], который не предположил явного преимущества в отношении смертности при сравнении исходов у пациентов с назогастральной трубкой или трубкой PEG. Недостатками НГТ для энтерального питания остались риск смещения трубки, сложность удержания НГТ в желудке и практичность использования НГТ для длительного питания [11]. Однако существуют и другие проблемы с использованием трубок ПЭГ для энтерального питания, в том числе риск инфицирования места стомы, избыточная грануляция и синдром скрытого бампера [27].
Однако существуют и другие проблемы с использованием трубок ПЭГ для энтерального питания, в том числе риск инфицирования места стомы, избыточная грануляция и синдром скрытого бампера [27].
Важным элементом ухода при энтеральном зондовом питании является обеспечение регулярной гигиены полости рта, частая замена назогастрального зонда и усиление воздействия физиотерапевта за счет мобилизации малоподвижных пациентов с инсультом [26]. Эти действия могут снизить риск аспирационной пневмонии и пролежней [26]. Кроме того, СЛТ играет важную роль в лечении дисфагии у пациентов с инсультом. После клинической оценки, которая может включать использование модифицированных текстур пищи и воды, а также инструментальные методы, такие как видеофлюороскопия, СЛТ может рекомендовать различные виды упражнений для пациента [13]. В зависимости от вида лечебной физкультуры и ее интенсивности у некоторых пациентов с дисфагическим инсультом может восстановиться глотание и вернуться к пероральной диете [13].
Введение назогастрального зонда у пациентов после инсульта затруднено из-за их трудностей в общении, неспособности глотать и возможной спутанности сознания [28]. Поэтому доступно использование различных методов для предотвращения смещения НГТ, таких как ленты, рукавицы и носовые уздечки [28]. Рукавицы и носовые уздечки могут быть эффективными, но необходимо тщательно учитывать информированное согласие и интересы пациента. Кроме того, использование ленты для фиксации назогастрального клапана на лице пациента может быть не столь эффективным, но является более широко распространенным подходом [28]. Следовательно, персонал должен быть обучен понимать все вопросы, касающиеся безопасной и этичной практики при обеспечении безопасности NGT [28].
Коллаборация FOOD Trial Collaboration обнаружила положительное влияние раннего энтерального питания на смертность [24]. Результаты этого исследования показали, что раннее энтеральное питание снижает смертность, но пациенты в большей степени зависят от медицинской помощи [24]. Другие исследования продемонстрировали эффективность энтерального питания у больных с тяжелым инсультом [29] и черепно-мозговой травмой [30]. Однако в настоящее время среди клиницистов нет единого мнения относительно потенциальной пользы раннего начала кормления назогастральным зондом [13].
Другие исследования продемонстрировали эффективность энтерального питания у больных с тяжелым инсультом [29] и черепно-мозговой травмой [30]. Однако в настоящее время среди клиницистов нет единого мнения относительно потенциальной пользы раннего начала кормления назогастральным зондом [13].
Были изучены преимущества раннего начала энтерального питания у пациентов после инсульта, которые находятся в коме, и Yamada [31] пришел к выводу, что отказ от нутритивной поддержки в течение трех дней после госпитализации является невыгодным с точки зрения питания. Тем не менее, слишком раннее начало нутритивной поддержки не было полезным с точки зрения питания по сравнению с ранним введением полного парентерального питания, поскольку Yamada [31] обнаружил, что пациенты подвержены высокому риску диареи, которая может предрасполагать пациентов к гиповолемии и потенциально вызывать ишемию.
Диарея является распространенной проблемой, связанной с энтеральным зондовым питанием, и может еще больше усугубить состояние пациентов после инсульта, которые уже подвержены риску недостаточности питания [32]. Продолжительность энтерального зондового питания была связана с риском развития диареи у пациентов после острого инсульта с частотой от 8% до 41% [32]. Продолжительность энтерального зондового питания в течение семи дней и более ассоциировалась с возникновением диареи, в то время как продолжительность менее семи дней не приводила к такому же клиническому исходу. Это важное соображение при планировании и управлении лечением после острого инсульта [32]. Кроме того, нарушение всасывания энтерального питания из-за диареи может привести к тяжелой гипопротеинемии и гипоальбуминемии [31]. Способ энтерального зондового питания может быть болюсным или непрерывным [19].]. Метод болюсного кормления обычно включает использование шприца для доставки корма пациенту в согласованное время, в то время как метод непрерывного кормления требует использования насоса и наборов для дозирования, чтобы контролировать скорость введения корма путем изменения количество капель в минуту [33]. Существуют преимущества и недостатки использования этих методов энтерального питания.
Продолжительность энтерального зондового питания была связана с риском развития диареи у пациентов после острого инсульта с частотой от 8% до 41% [32]. Продолжительность энтерального зондового питания в течение семи дней и более ассоциировалась с возникновением диареи, в то время как продолжительность менее семи дней не приводила к такому же клиническому исходу. Это важное соображение при планировании и управлении лечением после острого инсульта [32]. Кроме того, нарушение всасывания энтерального питания из-за диареи может привести к тяжелой гипопротеинемии и гипоальбуминемии [31]. Способ энтерального зондового питания может быть болюсным или непрерывным [19].]. Метод болюсного кормления обычно включает использование шприца для доставки корма пациенту в согласованное время, в то время как метод непрерывного кормления требует использования насоса и наборов для дозирования, чтобы контролировать скорость введения корма путем изменения количество капель в минуту [33]. Существуют преимущества и недостатки использования этих методов энтерального питания.
Энтеральное питание — полезный метод обеспечения питания пациентов с дисфагией после острого инсульта для удовлетворения их потребностей в питании. Это может быть доставлено с помощью питательной трубки NGT или PEG. Хотя у этих методов энтерального зондового питания есть преимущества, трудности остаются.
Оба автора, Оморогиева Оджо и Джоанн Брук, в равной степени внесли свой вклад в написание этой статьи.
Авторы заявляют об отсутствии конфликта интересов.
1. Оджо О. Использование пероральных пищевых добавок в условиях неотложной помощи. бр. Дж. Нурс. 2016;25:664–666. doi: 10.12968/bjon.2016.25.12.664. [PubMed] [CrossRef] [Google Scholar]
2. Ojo O. Зонды для энтерального питания: не идеально, но необходимо. бр. Дж. Нурс. 2015;24:910. doi: 10.12968/bjon.2015.24.18.910. [PubMed] [CrossRef] [Академия Google]
3. Национальный институт здравоохранения и передового опыта (NICE) Инсульт и транзиторная ишемическая атака у лиц старше 16 лет: диагностика и начальное лечение. Клиническое руководство [CG68] 2008 г. [(по состоянию на 1 октября 2016 г.)]. Доступно онлайн: https://www.nice.org.uk/guidance/Cg68
Клиническое руководство [CG68] 2008 г. [(по состоянию на 1 октября 2016 г.)]. Доступно онлайн: https://www.nice.org.uk/guidance/Cg68
4. Александров А.В. Что такое инсульт? В: Уильямс Дж., Перрил Л., Уоткинс С., редакторы. Сестринский уход при остром инсульте. Уайли-Блэквелл; Оксфорд, Великобритания: 2010. [Google Scholar]
5. Луенго-Фернандес Р., Грей А.М., Булл Л., Уэлч С., Катбертсон Ф., Ротвелл П.М. Качество жизни после ТИА и инсульта: десятилетние результаты Оксфордского сосудистого исследования. Неврология. 2013; 81: 1588–159.5. doi: 10.1212/WNL.0b013e3182a9f45f. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Национальная межвузовская рабочая группа по инсульту . Клинические рекомендации по инсульту. 4-е изд. Королевский колледж врачей; Лондон, Великобритания: 2012. [Google Scholar]
7. Американская ассоциация инсульта, ишемические инсульты (сгустки), 2014. [(по состоянию на 3 декабря 2016 г.)]. Доступно в Интернете: http://www.strokeassociation. org/STROKEORG/AboutStroke/TypesofStroke/IschemicClots/Ischemic-Strokes-Clots_UCM_310939_Article.jsp#.WDrwjLKLTIU
org/STROKEORG/AboutStroke/TypesofStroke/IschemicClots/Ischemic-Strokes-Clots_UCM_310939_Article.jsp#.WDrwjLKLTIU
8. Бхатнагар П., Скарборо П., Смитон Н.К., Аллендер С. Случаи всех инсультов и подтипов инсультов в Соединенном Королевстве, 1985–2008 гг.: систематический обзор. Общественное здравоохранение BMC. 2010;10:539. дои: 10.1186/1471-2458-10-539. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Рестрепо Л. Транзитная ишемическая атака. В: Витык Р.Дж., Ллинас Р.Х., редакторы. Гладить. Американский колледж врачей; Филадельфия, Пенсильвания, США: 2007. [Google Scholar]
10. Всемирная организация здравоохранения. 10 основных причин смерти. 2014. [(по состоянию на 3 декабря 2016 г.)]. Доступно на сайте: http://www.who.int/mediacentre/factsheets/fs310/en/
11. Rowat A. Энтеральное зондовое питание для пациентов с дисфагическим инсультом. бр. Дж. Нурс. 2015; 24:138–144. doi: 10.12968/bjon.2015.24.3.138. [PubMed] [CrossRef] [Google Scholar]
12. Сотрудничество в исследовании FOOD Плохой статус питания при поступлении предсказывает неблагоприятные исходы после инсульта: данные наблюдений из исследования FOOD. Гладить. 2003; 34: 1450–1456. [PubMed] [Академия Google]
Сотрудничество в исследовании FOOD Плохой статус питания при поступлении предсказывает неблагоприятные исходы после инсульта: данные наблюдений из исследования FOOD. Гладить. 2003; 34: 1450–1456. [PubMed] [Академия Google]
13. Биван Дж. Обновление вариантов лечения дисфагии после инсульта. бр. Дж. Нейроски. Нурс. 2015;11:10–19. doi: 10.12968/bjnn.2015.11.Sup2.10. [CrossRef] [Google Scholar]
14. Аудит лечения инсульта в Шотландии Аудит лечения инсульта в Шотландии: Национальный отчет о службах лечения инсульта в шотландских больницах, 2013 г. 2013. [(по состоянию на 3 декабря 2016 г.)]. Доступно в Интернете: http://tinyurl.com/lz4dbv4
15. Джиганадж С., Биван Дж., Эллендер С., Бат П.М. Вмешательства при дисфагии и нутритивная поддержка при остром и подостром инсульте. Кокрановская система баз данных. 2012; 10 doi: 10.1002/14651858.CD000323. [PubMed] [CrossRef] [Академия Google]
16. Chen S., Xian W., Cheng S., Zhou C., Zhou H., Feng J., Liu L., Chen L. Риск регургитации и аспирации у пациентов, получающих различные объемы энтерального питания. Азия Пак. Дж. Клин. Нутр. 2015;24:212–218. [PubMed] [Google Scholar]
Азия Пак. Дж. Клин. Нутр. 2015;24:212–218. [PubMed] [Google Scholar]
17. Шотландская межвузовская сеть рекомендаций (SIGN) Ведение пациентов с инсультом: выявление и лечение дисфагии, национальное клиническое руководство. 2010. [(по состоянию на 3 декабря 2016 г.)]. Доступно в Интернете: http://www.sign.ac.uk/pdf/sign119.pdf
18. Bennett B., Howard C., Barnes H., Jones A. Медикаментозное лечение пациентов с дисфагией: оценка службы. Нурс. Стоять. 2013; 27:41–48. doi: 10.7748/ns2013.06.27.41.41.e7498. [PubMed] [CrossRef] [Google Scholar]
19. Национальный институт здравоохранения и передового опыта (NICE) Нутритивная поддержка взрослых: поддержка перорального питания, энтеральное кормление через зонд и парентеральное питание (CG32) 2006. [(по состоянию на 1 октября) 2016)]. Доступно в Интернете: https://www.nice.org.uk/guidance/cg32
20. Британская ассоциация парентерального и энтерального питания (BAPEN) Универсальный инструмент скрининга недостаточности питания. 2016. [(по состоянию на 13 октября 2016 г.)]. Доступно на сайте: http://www.bapen.org.uk/pdfs/must/must_full.pdf
2016. [(по состоянию на 13 октября 2016 г.)]. Доступно на сайте: http://www.bapen.org.uk/pdfs/must/must_full.pdf
21. Catangui E.J., Slark J. Обходы в палатах под руководством медсестер: ценный вклад в оказание помощи при остром инсульте. бр. Дж. Нурс. 2012; 21:801–805. doi: 10.12968/bjon.2012.21.13.801. [PubMed] [CrossRef] [Google Scholar]
22. Стандарт качества NICE Nutrition Support in Adults Quality [QS24] 2012. [(по состоянию на 1 октября 2016 г.)]. Доступно в Интернете: https://www.nice.org.uk/guidance/qs24
23. Оджо О., Патель И. Домашнее энтеральное питание и работа в команде. J. Сообщество медсестер. 2012;26:15–18. [Google Scholar]
24. Dennis M.S., Lewis S.C., Warlow C. Влияние выбора времени и метода энтерального зондового питания у пациентов с дисфагическим инсультом (FOOD): многоцентровое рандомизированное контролируемое исследование. Ланцет. 2005; 365: 764–772. [PubMed] [Google Scholar]
25. Löser C., Aschl G., Hébuterne X., Mathus-Vliegen E.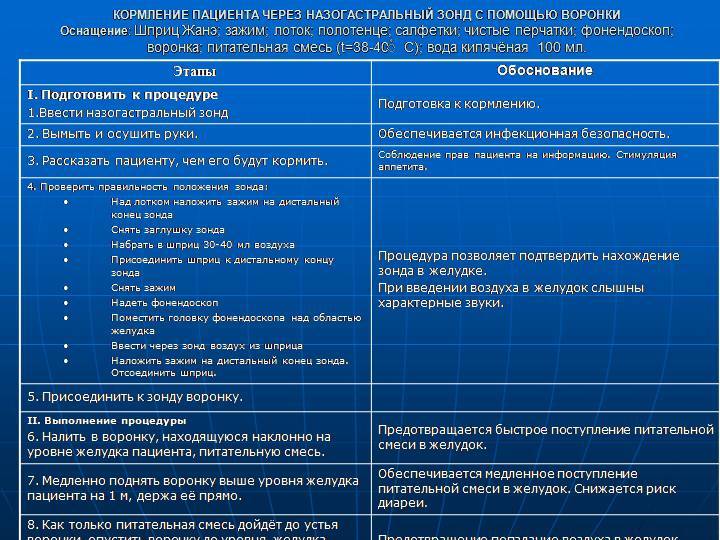 H., Muscaritoli M., Niv Y., Skelly R.H., Mathus V., Singer P. Рекомендации ESPEN по искусственным энтеральное питание — чрескожная эндоскопическая гастростомия (ЧЭГ) Clin. Нутр. 2005; 24:848–861. [PubMed] [Академия Google]
H., Muscaritoli M., Niv Y., Skelly R.H., Mathus V., Singer P. Рекомендации ESPEN по искусственным энтеральное питание — чрескожная эндоскопическая гастростомия (ЧЭГ) Clin. Нутр. 2005; 24:848–861. [PubMed] [Академия Google]
26. Арнольд М., Лиесирова К., Броег-Морвей А., Мейстерернст Дж., Шлагер М., Моно М., Сарыкая Х., Юнг С., Каги Г., Марван Э.К. Дисфагия при остром инсульте: заболеваемость, бремя и влияние на клинический исход. ПЛОС ОДИН. 2016;11:e0148424. doi: 10.1371/journal.pone.0148424. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Ojo O. Баллонные гастростомические трубки для длительного кормления по месту жительства. бр. Дж. Нурс. 2011;20:34–38. doi: 10.12968/bjon.2011.20.1.34. [PubMed] [CrossRef] [Академия Google]
28. Mahoney C., Rowat A., Macmillan M., Dennis M. Назогастральное питание пациентов, перенесших инсульт: Практика и образование. бр. Дж. Нурс. 2015;24:319–325. doi: 10.12968/bjon.2015.24.6.319. [PubMed] [CrossRef] [Google Scholar]
29. James R., Gines D., Menlove A., Horn S.D., Gassaway J., Smout R. Нутритивная поддержка (кормление через зонд) как реабилитационное вмешательство. Арка физ. Мед. Реабилит. 2005; 86: 82–92. doi: 10.1016/j.apmr.2005.07.314. [PubMed] [CrossRef] [Google Scholar]
James R., Gines D., Menlove A., Horn S.D., Gassaway J., Smout R. Нутритивная поддержка (кормление через зонд) как реабилитационное вмешательство. Арка физ. Мед. Реабилит. 2005; 86: 82–92. doi: 10.1016/j.apmr.2005.07.314. [PubMed] [CrossRef] [Google Scholar]
30. Horn S.D., Kinikini M., Moore L.W., Hammond F.M., Brandstater M.E., Smout R.J., Barrett R.S. Энтеральное питание для пациентов с черепно-мозговой травмой в реабилитационном учреждении: ассоциации с характеристиками и результатами пациента до травмы и травмы. Арка физ. Мед. Реабилит. 2015;96: 245–255. doi: 10.1016/j.apmr.2014.06.024. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Ямада С.М. Слишком раннее начало энтерального питания не является питательным преимуществом для пациентов с коматозным острым инсультом. Дж. Ниппон. Мед. Ш. 2015; 82: 186–192. doi: 10.1272/jnms.82.186. [PubMed] [CrossRef] [Google Scholar]
32. Аревало-Мансо Дж.Дж., Мартинес-Санчес П., Хуарес-Мартин Б., Фуэнтес Б.