Что вызывает появление папиллом на шее. Как выглядят папилломы на шее. Какие существуют способы удаления папиллом на шее. Когда необходимо обратиться к врачу при обнаружении папиллом на шее. Как предотвратить появление папиллом на шее.
Что такое папилломы на шее
Папилломы на шее представляют собой доброкачественные новообразования кожи, вызванные вирусом папилломы человека (ВПЧ). Они имеют вид небольших мягких наростов телесного или коричневатого цвета, часто на тонкой ножке. Размер папиллом обычно не превышает 5-10 мм.
Причины появления папиллом на шее
Основные причины возникновения папиллом на шее:
- Заражение вирусом папилломы человека
- Снижение иммунитета
- Гормональные нарушения
- Стрессы
- Неправильное питание
- Вредные привычки (курение, алкоголь)
Папилломы чаще всего появляются в местах трения одежды или украшений о кожу шеи. Это создает благоприятные условия для активизации вируса папилломы человека.
Симптомы и внешний вид папиллом на шее

- Небольшие мягкие наросты размером 2-10 мм
- Телесного, розоватого или коричневатого цвета
- На тонкой ножке или широком основании
- Гладкие или шероховатые на ощупь
- Одиночные или множественные
Обычно папилломы на шее не вызывают неприятных ощущений. Но при травмировании могут воспаляться, зудеть и кровоточить.
Диагностика папиллом на шее
Для диагностики папиллом на шее врач проводит:
- Визуальный осмотр
- Дерматоскопию (осмотр под увеличением)
- Анализ на ВПЧ
- При необходимости — биопсию
Важно отличить папилломы от других новообразований кожи, в том числе злокачественных. Поэтому при обнаружении подозрительных образований на шее нужно обязательно обратиться к дерматологу.
Методы удаления папиллом на шее
Существует несколько способов удаления папиллом на шее:
Криодеструкция
Удаление папиллом жидким азотом. Метод эффективен для небольших папиллом. Процедура практически безболезненна, не оставляет рубцов.
Электрокоагуляция
Выжигание папиллом током высокой частоты. Подходит для папиллом среднего размера. Процедура выполняется под местной анестезией.

Лазерное удаление
Радиоволновой метод
Удаление папиллом с помощью радиоволн. Бескровный и безболезненный способ, подходит для папиллом любого размера.
Хирургическое иссечение
Применяется для удаления крупных папиллом. Процедура проводится под местной анестезией, оставляет небольшой рубец.
Метод удаления папиллом подбирается индивидуально врачом в зависимости от размера, локализации и количества новообразований.
Профилактика появления папиллом на шее
Для профилактики возникновения папиллом на шее рекомендуется:
- Укреплять иммунитет
- Соблюдать правила личной гигиены
- Избегать травмирования кожи шеи
- Отказаться от вредных привычек
- Правильно питаться
- Своевременно лечить хронические заболевания
- Избегать незащищенных половых контактов
При появлении папиллом на шее не стоит заниматься самолечением. Необходимо обратиться к дерматологу для диагностики и выбора оптимального метода лечения.

Когда нужно обратиться к врачу
Обязательно посетите дерматолога, если:
- Папиллома на шее увеличивается в размерах
- Изменился цвет или форма папилломы
- Появились болезненность, зуд или кровоточивость
- Образовались новые папилломы
- Папиллома травмируется одеждой или украшениями
Своевременное обращение к врачу поможет предотвратить осложнения и подобрать эффективное лечение.
Возможные осложнения папиллом на шее
При отсутствии лечения папилломы на шее могут привести к следующим осложнениям:
- Воспаление и инфицирование
- Разрастание и увеличение количества папиллом
- Малигнизация (озлокачествление) — крайне редко
- Косметический дефект
- Психологический дискомфорт
Чтобы избежать осложнений, необходимо своевременно обращаться к врачу при обнаружении папиллом на шее и других участках тела.
Лечение папиллом на шее народными средствами
Некоторые народные средства могут помочь в борьбе с папилломами на шее:
- Сок чистотела — обладает противовирусным действием
- Касторовое масло — способствует отторжению папиллом
- Яблочный уксус — подсушивает папилломы
- Чеснок — оказывает противовирусный эффект
- Масло чайного дерева — обладает антисептическими свойствами
Важно помнить, что народные методы могут использоваться только как дополнение к основному лечению, назначенному врачом. Самолечение может быть опасным и привести к осложнениям.

Вопросы и ответы о папилломах на шее
Заразны ли папилломы на шее?
Да, папилломы вызываются вирусом и могут передаваться при тесном контакте. Однако риск заражения при случайном прикосновении невысок.
Могут ли папилломы на шее пройти сами?
В некоторых случаях при укреплении иммунитета папилломы могут исчезнуть самостоятельно. Однако чаще всего требуется лечение.
Опасны ли папилломы на шее?
В большинстве случаев папилломы на шее не представляют опасности. Однако в редких случаях возможно их озлокачествление, поэтому необходимо наблюдение у врача.
Можно ли удалять папилломы на шее самостоятельно?
Категорически не рекомендуется удалять папилломы самостоятельно. Это может привести к инфицированию, кровотечению и образованию рубцов. Удаление должно проводиться только врачом.
Папилломы на шее — распространенная проблема, с которой можно успешно бороться при правильном подходе. Своевременное обращение к врачу и соблюдение рекомендаций по профилактике помогут сохранить здоровье и красоту кожи шеи.

Методы лечения вируса папилломы человека у женщин и мужчин — клиника «Добробут»
Как и чем лечить папилломы: основные методы
Папилломы – это доброкачественные новообразования, появляющиеся на коже и выступающие над ней. Они имеют вид сосочков на тонкой ножке или широком основании и состоят из соединительной ткани. Цвет папиллом – от розоватого до коричневого. Возникают новообразования на разных участках тела – руках, ногах, шее, груди, спине, лице. Причины появления папиллом на шее и в других местах – инфицирование кожи вирусом папилломы человека (ВПЧ).
Папилломы причиняют определенные эстетические неудобства, а также легко травмируются: их можно случайно зацепить ногтем, мочалкой, расческой, бритвой, натереть одеждой, ремнем. При этом из-за попадания патогенных микроорганизмов через поврежденный эпидермис может начаться воспаление папилломы: она меняет цвет, увеличивается, зудит, иногда кровоточит и болит. Поэтому неэстетичные «наросты» на теле рекомендуется удалять.
Симптомы вируса папилломы человека
Эти доброкачественные новообразования появляются из-за инфицирования ВПЧ, который распространяется контактно, что подразумевает непосредственное соприкосновение человека с кожей/слизистой носителя или использование его предметов гигиены. Человек может и не подозревать о носительстве, так как вирус долго «спит». В результате стресса, перенесенных инфекций, гормональных сбоев, обострения хронических заболеваний, приема антибиотиков или других факторов, снижающих иммунитет, на теле появляются папилломы.
Основные симптомы вируса папилломы человека – это появление доброкачественных новообразований на коже и слизистых оболочках. ВПЧ считается канцерогенным агентом. Однако не все типы вируса папилломы человека запускают механизм образования злокачественной опухоли.
Порядка 40 типов ВПЧ поражают аногенитальную область, вызывая появление остроконечных кондилом.
Вирус папилломы может также стать «виновником»:
- плоских кондилом;
- цервикальной неоплазии;
- карциномы и других злокачественных новообразований;
- бородавок.

Вирус папилломы человека у мужчин может вызвать появление на головке члена и крайней плоти генитальных бородавок. Помимо того, что кондиломы иногда приводят к сужению крайней плоти, носитель вируса подвергает риску заражения своего полового партнера. Поэтому сдать анализ на ВПЧ необходимо как женщине, так и мужчине.
Лечение вируса папилломы человека у женщин и мужчин
Любое самолечение, включая «проверенные» народные методы, недопустимо. Оно может привести к увеличению папиллом, распространению на соседние участки (папилломатоз), озлокачествлению тканей. Как и чем лечить папилломы – определяет врач после визуального осмотра и дополнительного обследования (ПЦР-диагностика, цитологическое и/или гистологическое исследование).
Увы, специфических препаратов для терапии ВПЧ пока нет. Лечение вируса папилломы человека у женщин и мужчин – это, прежде всего, противовирусная терапия, которая угнетает активность ВПЧ и устраняет клинические проявления заболевания. Для терапии папилломавирусной инфекции используют иммунотерапию вместе с симптоматическим лечением.
Для терапии папилломавирусной инфекции используют иммунотерапию вместе с симптоматическим лечением.
Препараты для лечения ВПЧ:
- кондилин;
- подофиллин;
- солкодерм;
- ферезол;
- альфаферон;
- неовир;
- циклоферон.
Удаление папиллом
Схема лечения включает и удаление папилломатозных очагов. Крупные и/или воспалившиеся новообразования удаляют хирургическим путем. Эффективным методом избавления от папиллом считается электрокоагуляция. Процедура не требует особой подготовки и практически безболезненна (используются поверхностные анестетики). Метод безопасен, после его применения не остается рубцов. После электрокоагуляции образуется корочка, с отшелушиванием которой на коже некоторое время остается депигментированное пятнышко.
Современный щадящий метод, после которого не остается никаких следов, – это удаление папилломы лазером. Во время сеанса параллельно с прижиганием доброкачественного новообразования происходит запаивание кровеносных сосудов, поэтому процедура бескровная.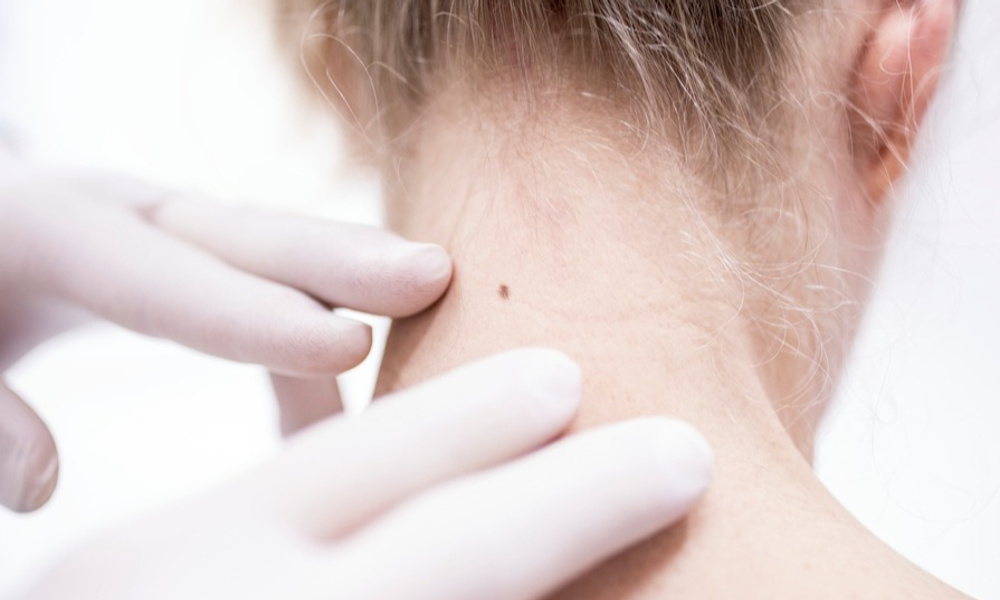 Проводится она с использованием местного анестетика. Риск повреждения соседних тканей сведен к нулю. На месте удаленной папилломы какое-то время остается красный след, исчезающий самостоятельно или после применения назначенных врачом гелей/мазей. Выполнять процедуру удаления следует не в косметическом кабинете, а в профильном медицинском учреждении и только после консультации с дерматологом или дерматологом-онкологом.
Проводится она с использованием местного анестетика. Риск повреждения соседних тканей сведен к нулю. На месте удаленной папилломы какое-то время остается красный след, исчезающий самостоятельно или после применения назначенных врачом гелей/мазей. Выполнять процедуру удаления следует не в косметическом кабинете, а в профильном медицинском учреждении и только после консультации с дерматологом или дерматологом-онкологом.
Основной способ профилактики – прививка
Прививка от вируса папилломы человека – это пока единственный способ защитить себя от рака шейки матки, который вызывается ВПЧ. Существующие сегодня вакцины безопасны. Они эффективно используются во многих странах для профилактики ВПЧ – в частности, типов 16 и 18. Предпочтительнее проводить вакцинацию до первого сексуального контакта, поэтому ВОЗ рекомендует прививать девочек в возрасте 9-13 лет.
Следует знать, что вакцины не лечат ВПЧ и связанные с ним заболевания. Подробнее об этом читайте на нашем сайте https://www. dobrobut.com.
dobrobut.com.
Связанные услуги:
Консультация дерматолога
Дерматовенерология
ВПЧ; вирус папилломы человека; папилломавирус; количественно с генотипированием — ВПЧ — 21 тип (6,11,44,16,18,26,31,33,35,39,45,51,52,53,56,58,59,66,68,73, 82) рядом с домом
Вирусы папилломы человека 6, 11 — безоболочечные ДНК-вирусы, являющиеся представителями семейства Papillomaviridae. Вирусы передаются при микротравмах кожи и слизистых оболочек, а также половым путем. При родах вирусы передаются новорожденным. ВПЧ-инфекция относится к наиболее распространенной инфекции передающейся половым путём (ИППП). К группе риска по ВПЧ-инфекции можно отнести практически всех людей, живущих половой жизнью.
ВПЧ инфицируют и размножаются в эпителии кожи, образуя доброкачественные бородавки, и в слизистых оболочках, вызывая генитальные, оральные и конъюнктивальные папилломы,может быть клинически выраженной, протекать субклинически или быть латентной. У женщин инфицируется и покрывается генитальными бородавками область преддверия влагалища, стенки влагалища, шейки матки, наружное отверстие уретры, анальная область. У мужчин поражается головка полового члена, крайняя плоть, мошонка, анальная область.
У мужчин поражается головка полового члена, крайняя плоть, мошонка, анальная область.
Показания к сдаче анализа:
1. Бородавки, кондиломы генитальной области.
2. Выявлении дисплазии эпителия при цитологическом исследовании.
3. Профилактические скрининговые исследования.
Материал для анализа
Мужчины — урогенитальный соскоб, женщины — соскоб из цервикального канала.
ВПЧ 16, 18 относятся к группе высокого и среднего риска озлокачествления пораженных клеток.
Инфицирование осуществляется следующими путями:
1. Передача ВПЧ 18, 16 типа при случайных интимных отношениях без контрацептивов.
2. Контактный способ в бытовых условиях.
3. Передача папилломавируса 16, 18 типов плоду через материнскую плаценту.
Развитие вируса папилломы человека 16, 18 типов делят на несколько этапов:
1.Инкубационный период. Характеризуется бессимптомным развитием инфекционного процесса. Длительность периода прогнозировать невозможно.
2. Этап активного роста новообразований. Наблюдается появление характерных признаков – папиллом 16 типа. Делительный процесс этих структур ускоряется и становится незакономерным, в результате возникает рост новообразований.
3. Дисплазия.
Обнаружение предракового состояния – это косвенные показатели ВПЧ 16, 18 типов. На раннем этапе заболевание легко поддается терапии. Предупреждение озлокачествления заболевания требует срочных мер.
4. Злокачественная форма заболевания. После изменения клеточной структуры происходят мутации клеток под влиянием возбудителя папилломы 16, 18 и развивается онкологический процесс.
Папилломы человека 16, 18 типа представляют собой наросты округлой формы, связанные с телом посредством тонкой ножки. Образования имеют мягкую структуру, безболезненные. По цвету наросты практически не отличаются от здоровой кожи. На слизистых оболочках часто появляются остроконечные образование – кондиломы. Такие наросты чаще локализуются группами, внешне напоминающими коралл. В случае активизации заболевания могут проявляться более выраженные признаки вируса папилломы 16 типа: жжение и раздражительность в области гениталий, появление нехарактерных выделений с неприятным запахом. ВПЧ 18 типа вызывает около 60% случаев появления онкозаболевания женских и мужских половых органов.
В случае активизации заболевания могут проявляться более выраженные признаки вируса папилломы 16 типа: жжение и раздражительность в области гениталий, появление нехарактерных выделений с неприятным запахом. ВПЧ 18 типа вызывает около 60% случаев появления онкозаболевания женских и мужских половых органов.
Диагностика
Самым точным и диагностически важным методом является полимеразная цепная реакция или анализ ПЦР.
ПЦР основывается на определении ДНК вируса в исследуемой биологической среде, полученной от обследуемого. Это может быть кровь, слюна, моча, в которые для определения вируса вводят специальный реагент.
Типы 31, 33, 35 относятся к группе с высокой степенью онкогенного риска и чаще всего приводят к таким заболеваниям, как бовеноидный папулез и интраэпителиальную неоплазию шейки матки.
Бовеноидный папулез выявляется у мужчин, и риск развития этого заболевания повышен при чрезмерном количестве сексуальных партнерш.
Неоплазия шейки матки может быть легкой, умеренной и выраженной степени. В первом случае все изменения выявляются только при цитологическом исследовании мазка. Выраженная неоплазия считается уже интраэпителиальным раком. Неоплазия у женщин часто сочетается с образованием кондилом, возникающих под влиянием вируса 6 и 11 типов.
В первом случае все изменения выявляются только при цитологическом исследовании мазка. Выраженная неоплазия считается уже интраэпителиальным раком. Неоплазия у женщин часто сочетается с образованием кондилом, возникающих под влиянием вируса 6 и 11 типов.
В случаях развития рака шейки матки, сначала появляется эрозия, затем дисплазия (3 степени, последняя – начало онкологии). Эти процессы, вызванные онкогенными ВПЧ 18, 33, 35 типов, Мужчины зачастую являются носителями ВПЧ 33, 51 и других типов. Иногда можно наблюдать появление некондиломатозных образований на теле, которые могут быстро вырастать, и так же быстро исчезать.
Показания к сдаче анализа
1. Болевые ощущения в нижней части живота, вовремя и после полового акта.
2.Наличие выделений, в том числе с примесью крови.
3. Диагностирование эрозии шейки матки.
4. Обнаружены остроконечные кондиломы во влагалище.
Диагностика
Для выявления ВПЧ у женщин, гинеколог проводит осмотр в кресле с использованием зеркала.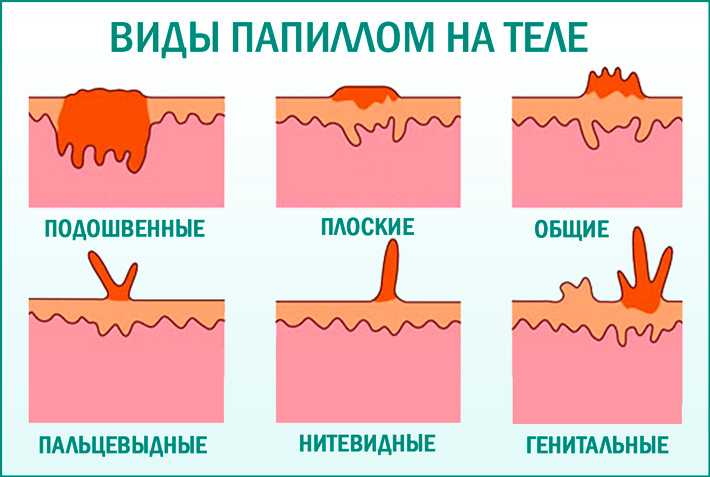 Если на слизистой оболочке влагалища, стенки матки обнаружены плоские разрастания, или же на малых половых губах, вульве – остроконечные кондиломы, необходимо взять мазок для проведения цитологических исследований.
Если на слизистой оболочке влагалища, стенки матки обнаружены плоские разрастания, или же на малых половых губах, вульве – остроконечные кондиломы, необходимо взять мазок для проведения цитологических исследований.
Когда разрастаний, вызванных ВПЧ , не обнаруживается, проводят кольпоскопию. Этот метод диагностики подразумевает изучение стенок влагалища и шейки матки под микроскопом. Если наружных проявлений не наблюдается, стенки смазывают 3% раствором уксусной кислоты – патологические образования белеют, а цвет здоровой слизистой оболочки не меняется.С помощью метода цепной реакции полимеразы (ПЦР) определяют наличие вируса в организме
ВПЧ 51, как и ВПЧ 31, относится к группе среднего онкогенного риска, путь передачи в основном половой, способствует появлению злокачественных образований половых органов. ВПЧ 51 типа помимо образований генитальных бородавок приводит к появлению гигантской кондиломы Бушке – Левенштенна. Риск возникновения злокачественных процессов повышается при частой смене половых партнёров и при гомосексуальных контактах.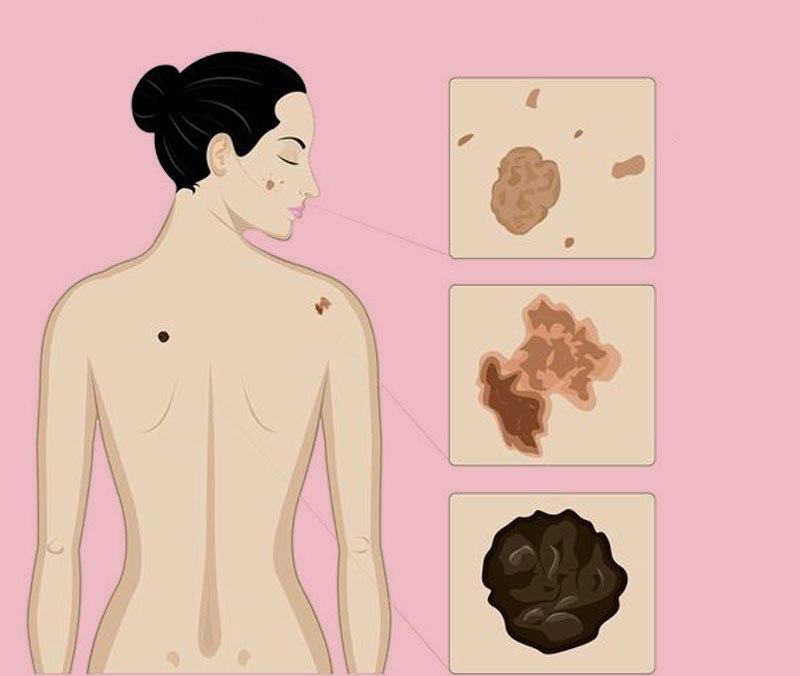
ВПЧ 52 типа, как и ВПЧ 51, принадлежит к группе вирусов, провоцирующих онкологию. Основными причинами поражения организма является понижение работы защитных механизмов, эндокринные проблемы, курение, общие заболевания с угнетением иммунитета.
ВПЧ 56 типа. Попадает в организм через микротравмы на коже и через слизистую оболочку. Процесс чаще локализуется в матке, во влагалище, уретре, на головке полового члена. В группу риска попадают пациенты с пониженной иммунной системой, отягощенной наследственностью, с обострениями хронической патологии. ВПЧ 56 относится к группе высокого онкологического риска и при подтверждении диагностических обследований требует незамедлительного вмешательства.
Диагностика
Для выявления ВПЧ у женщин, гинеколог проводит осмотр в кресле с использованием зеркала. Если на слизистой оболочке влагалища, стенки матки обнаружены плоские разрастания, или же на малых половых губах, вульве – остроконечные кондиломы, необходимо взять мазок для проведения цитологических исследований.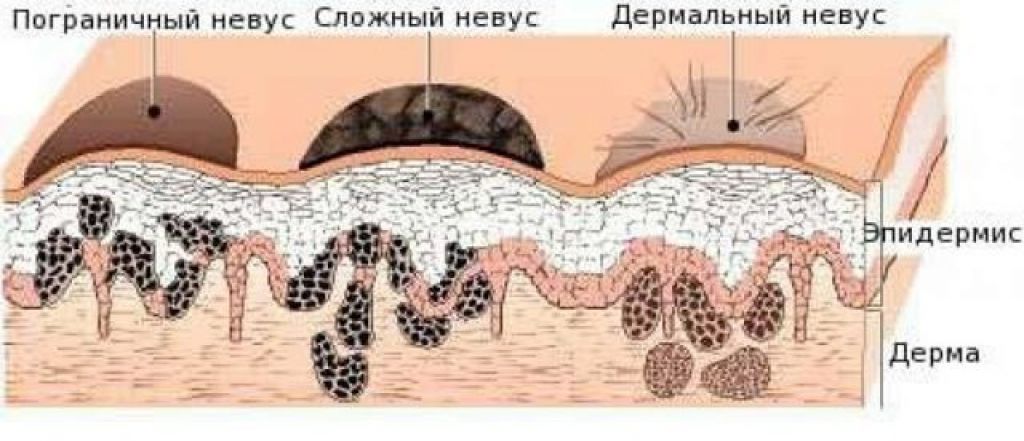
Когда разрастаний, вызванных ВПЧ, не обнаруживается, проводят кольпоскопию. Этот метод диагностики подразумевает изучение стенок влагалища и шейки матки под микроскопом. Если наружных проявлений не наблюдается, стенки смазывают 3% раствором уксусной кислоты – патологические образования белеют, а цвет здоровой слизистой оболочки не меняется. С помощью метода цепной реакции полимеразы (ПЦР) определяют наличие вируса в организме
Папилломавирусы человека, в число которых входит ВПЧ 21 типа, поражают кожу и слизистые оболочки людей, инфекция обнаруживается в местах проникновения по наличию бородавок и кондилом
В группу возбудителей под этим названием входят штаммы, вызывающие на коже появление бородавок, доброкачественных опухолей на коже.
Бородавки с вирусом, при наличии постоянно действующих факторов могут переродиться в раковые образования кожи. К таким причинам относятся:
1.Частое механическое раздражение папилломы.
2.Химическое воздействие на неё.
3. Резкое снижение иммунитета носителя вируса.
Резкое снижение иммунитета носителя вируса.
Заражение вирусом 21 типа происходит от контакта с больным человеком или бытовым путем – через вещи, на которые попал вирус
Симптоматика
Проявляются образованиями на руках в районе кистей, на пальцах и ладонях, шее, лице, у носа и губ,на подошвах.
По внешнему виду бородавки представляют собой плотный нарост ороговевшего эпителия телесного цвета, чуть светлее обычной окраски кожного покрова. Внутри нароста заметны черные точки – капилляры, которые были повреждены инфекцией. Форма бородавок преимущественно круглая, с ровными краями, они плотно прилегают к коже и не имеют ножки. Вокруг бородавок — здоровая кожа без всяких признаков покраснения, никаких болевых ощущений они не вызывают.
Перед произведением процедуры необходимо выполнить ряд требований:
1.Не жить половой жизнью два дня
2.Не принимать никаких лекарств.
3.Отказаться от химических веществ при купании
4.Не ходить в туалет 2 часа.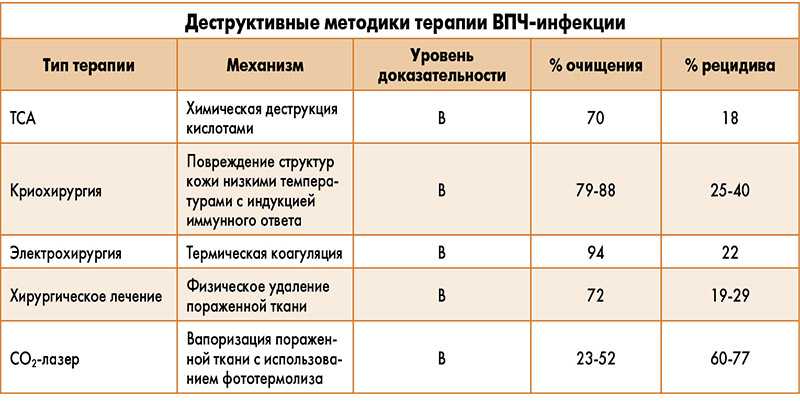
5.Не пить много жидкости.
Материал забора: Соскобе эпителиальных клеток урогенитального тракта.
Сдать анаиз на ВПЧ — 21 тип (6,11,44,16,18,26,31,33,35,39,45,51,52,53,56,58,59,66,68,73, 82) в Екатеринбурге можно по адресам ул.Большакова д.68 и ул. Викулова 33/2
Тест на вирус папилломы человека (ВПЧ): Медицинский тест MedlinePlus
Что такое тест на ВПЧ?
ВПЧ означает вирус папилломы человека. Это наиболее распространенное заболевание, передающееся половым путем (ЗППП), которым в настоящее время инфицированы миллионы американцев. ВПЧ может заражать как мужчин, так и женщин. Большинство людей с ВПЧ не знают, что они инфицированы, и у них никогда не возникает никаких симптомов или проблем со здоровьем.
Существует множество различных типов ВПЧ. Некоторые виды вызывают проблемы со здоровьем. Инфекции ВПЧ обычно группируются как ВПЧ низкого или высокого риска.
- ВПЧ низкого риска ВПЧ может вызывать появление бородавок на анусе и в области гениталий, а иногда и во рту.
 Другие инфекции ВПЧ низкого риска могут вызывать бородавки на руках, ладонях, ступнях или груди. Бородавки ВПЧ не вызывают серьезных проблем со здоровьем. Они могут исчезнуть сами по себе, или поставщик медицинских услуг может удалить их в рамках незначительной процедуры в офисе.
Другие инфекции ВПЧ низкого риска могут вызывать бородавки на руках, ладонях, ступнях или груди. Бородавки ВПЧ не вызывают серьезных проблем со здоровьем. Они могут исчезнуть сами по себе, или поставщик медицинских услуг может удалить их в рамках незначительной процедуры в офисе. - ВПЧ высокого риска. Большинство ВПЧ-инфекций высокого риска не вызывают никаких симптомов и исчезают в течение года или двух. Но некоторые инфекции ВПЧ высокого риска могут длиться годами. Эти длительные инфекции могут привести к раку. ВПЧ является причиной большинства случаев рака шейки матки. Длительно сохраняющийся ВПЧ может также вызывать другие виды рака, включая рак ануса, влагалища, полового члена, рта и горла.
Тест на ВПЧ позволяет выявить ВПЧ высокого риска у женщин. Медицинские работники обычно могут диагностировать ВПЧ низкого риска путем визуального осмотра бородавок. Так что тесты не нужны. В то время как мужчины могут быть инфицированы ВПЧ, тестирование, как правило, не рекомендуется для мужчин. Не существует утвержденного FDA теста на ВПЧ для мужчин, и большинство мужчин с ВПЧ выздоравливают от инфекции без каких-либо симптомов.
Не существует утвержденного FDA теста на ВПЧ для мужчин, и большинство мужчин с ВПЧ выздоравливают от инфекции без каких-либо симптомов.
Другие названия: генитальный вирус папилломы человека, ВПЧ высокого риска, ДНК ВПЧ, РНК ВПЧ
Для чего он используется?
Тест используется для выявления типа ВПЧ, который может привести к раку шейки матки. Это часто делается одновременно с мазком Папаниколау, процедурой, которая проверяет наличие аномальных клеток, которые также могут привести к раку шейки матки. Когда тест на ВПЧ и мазок Папаниколау делаются одновременно, это называется совместным тестированием.
Зачем мне нужен тест на ВПЧ?
Вам может потребоваться тест на ВПЧ, если вы:
- Женщина в возрасте 30–65 лет. Американское онкологическое общество рекомендует женщинам этой возрастной группы проходить тест на ВПЧ с мазком Папаниколау (совместное тестирование) каждые пять лет.
- Если вы женщина любого возраста, получившая аномальный результат мазка Папаниколау
Тестирование на ВПЧ в , а не рекомендуется для женщин моложе 30 лет, у которых были нормальные результаты мазка Папаниколау. Рак шейки матки в этой возрастной группе встречается редко, но ВПЧ-инфекция распространена. Большинство инфекций ВПЧ у молодых женщин проходят без лечения.
Рак шейки матки в этой возрастной группе встречается редко, но ВПЧ-инфекция распространена. Большинство инфекций ВПЧ у молодых женщин проходят без лечения.
Что происходит во время теста на ВПЧ?
Для проведения теста на ВПЧ вы ляжете на спину на диагностический стол с согнутыми коленями. Вы будете опираться ногами на опоры, называемые стременами. Ваш поставщик медицинских услуг будет использовать пластиковый или металлический инструмент, называемый зеркалом, чтобы открыть влагалище, чтобы можно было увидеть шейку матки. Затем ваш врач будет использовать мягкую щетку или пластиковый шпатель для сбора клеток из шейки матки. Если вы также получаете мазок Папаниколау, ваш врач может использовать один и тот же образец для обоих тестов или взять второй образец клеток.
Нужно ли мне что-то делать для подготовки к тесту?
Вам не следует проходить тест во время менструации. Вам также следует избегать определенных действий перед тестированием. За два дня до исследования вы не должны:
- Использовать тампоны
- Используйте вагинальные лекарства или противозачаточные пены
- Душ
- Займитесь сексом
Есть ли риски для теста?
Нет никаких известных рисков для теста на ВПЧ. Во время процедуры вы можете ощущать легкий дискомфорт. После этого у вас может быть небольшое кровотечение или другие выделения из влагалища.
Во время процедуры вы можете ощущать легкий дискомфорт. После этого у вас может быть небольшое кровотечение или другие выделения из влагалища.
Что означают результаты?
Ваши результаты будут представлены как отрицательные, также называемые нормальными, или положительные, также называемые ненормальными.
Отрицательный/Нормальный. ВПЧ высокого риска не обнаружено. Ваш поставщик медицинских услуг может порекомендовать вам вернуться для повторного скрининга через пять лет или раньше, в зависимости от вашего возраста и истории болезни.
Положительный/ненормальный. Обнаружен ВПЧ высокого риска. Это не значит, что у вас рак. Это означает, что у вас может быть более высокий риск заболеть раком шейки матки в будущем. Ваш поставщик медицинских услуг может назначить дополнительные тесты для мониторинга и/или диагностики вашего состояния. Эти тесты могут включать:
- Кольпоскопия, процедура, при которой врач использует специальный увеличительный прибор (кольпоскоп) для осмотра влагалища и шейки матки
- Биопсия шейки матки, процедура, при которой ваш лечащий врач берет образец ткани из шейки матки для изучения под микроскопом
- Более частое совместное тестирование (ВПЧ и мазок Папаниколау)
Если ваши результаты оказались положительными, важно регулярно или чаще сдавать анализы.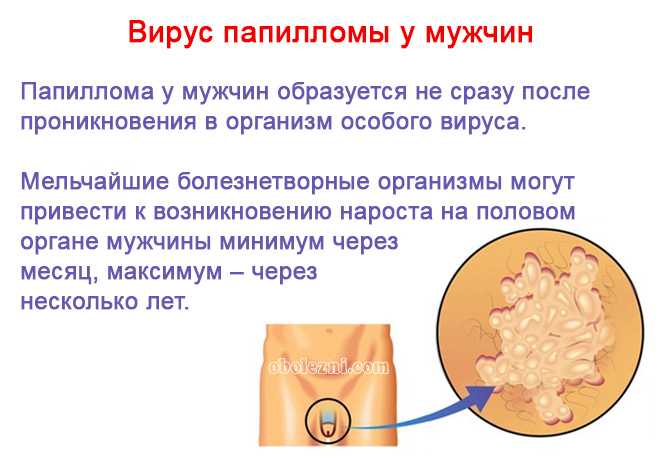 Могут пройти десятилетия, прежде чем аномальные клетки шейки матки превратятся в рак. При раннем обнаружении аномальные клетки можно лечить до они становятся раковыми. Гораздо легче предотвратить рак шейки матки, чем лечить его после того, как он развился.
Могут пройти десятилетия, прежде чем аномальные клетки шейки матки превратятся в рак. При раннем обнаружении аномальные клетки можно лечить до они становятся раковыми. Гораздо легче предотвратить рак шейки матки, чем лечить его после того, как он развился.
Узнайте больше о лабораторных тестах, референтных диапазонах и понимании результатов.
Что еще мне нужно знать о тесте на ВПЧ?
ВПЧ не лечится, но большинство инфекций проходят сами по себе. Вы можете предпринять шаги, чтобы снизить риск заражения ВПЧ. Секс только с одним партнером и безопасный секс (с использованием презерватива) могут снизить риск. Вакцинация еще более эффективна.
Вакцина против ВПЧ — это безопасный и эффективный способ защитить себя от ВПЧ-инфекций, которые обычно вызывают рак. Вакцина против ВПЧ работает лучше всего, когда ее делают тому, кто никогда не подвергался воздействию вируса. Поэтому рекомендуется давать его людям до того, как они начнут половую жизнь. Центры по контролю и профилактике заболеваний (CDC) и Американская академия педиатрии рекомендуют вакцинировать девочек и мальчиков, начиная с 11 или 12 лет. Обычно в общей сложности делается две или три прививки от ВПЧ (прививки) с интервалом в несколько месяцев. . Разница в количестве доз зависит от возраста вашего ребенка или молодого человека и рекомендаций поставщика медицинских услуг.
Обычно в общей сложности делается две или три прививки от ВПЧ (прививки) с интервалом в несколько месяцев. . Разница в количестве доз зависит от возраста вашего ребенка или молодого человека и рекомендаций поставщика медицинских услуг.
Если у вас есть вопросы о вакцине против ВПЧ, поговорите с лечащим врачом вашего ребенка и/или вашим лечащим врачом.
Ссылки
- Allina Health [Интернет]. Миннеаполис: Allina Health; Тест на ДНК ВПЧ; [цитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://wellness.allinhealth.org/library/content/1/7534 .
- Американская академия педиатрии [Интернет]. Итаска (Иллинойс): Американская академия педиатрии; c2018. Заявление о политике: Рекомендации по вакцине против ВПЧ; 27 февраля 2012 г. [цитировано 5 июня 2018 г.]; [около 4 экранов]. Доступно по адресу: http://pediatrics.aappublications.org/content/pediatrics/129./3/602.full.pdf
- Американское онкологическое общество [Интернет]. Атланта: Американское онкологическое общество, Inc.
 ; c2018. ВПЧ и тестирование на ВПЧ; [обновлено 9 октября 2017 г .; процитировано 5 июня 2018 г.]; [около 4 экранов]. Доступно по адресу: HThttps://www.cancer.org/cancer/cancer-causes/infectious-agents/hpv/hpv-and-hpv-testing.htmlTP .
; c2018. ВПЧ и тестирование на ВПЧ; [обновлено 9 октября 2017 г .; процитировано 5 июня 2018 г.]; [около 4 экранов]. Доступно по адресу: HThttps://www.cancer.org/cancer/cancer-causes/infectious-agents/hpv/hpv-and-hpv-testing.htmlTP . - Cancer.net [Интернет]. Александрия (Вирджиния): Американское общество клинической онкологии; 2005–2018 гг. ВПЧ и рак; 2017 г., февраль [цитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://www.cancer.net/navigating-cancer-care/prevention-and-healthy-living/hpv-and-cancer
- Центры по контролю и профилактике заболеваний [Интернет]. Атланта: Министерство здравоохранения и социальных служб США; Информационный бюллетень о генитальной инфекции ВПЧ; [обновлено 16 ноября 2017 г .; процитировано 5 июня 2018 г.]; [около 4 экранов]. Доступно по адресу: https://www.cdc.gov/std/hpv/stdfact-hpv.htm .
- Центры по контролю и профилактике заболеваний [Интернет]. Атланта: Министерство здравоохранения и социальных служб США; Информационный бюллетень о ВПЧ и мужчинах; [обновлено 14 июля 2017 г .
 ; процитировано 5 июня 2018 г.]; [около 4 экранов]. Доступно по адресу: https://www.cdc.gov/std/hpv/stdfact-hpv-and-men.htm
; процитировано 5 июня 2018 г.]; [около 4 экранов]. Доступно по адресу: https://www.cdc.gov/std/hpv/stdfact-hpv-and-men.htm - Центры по контролю и профилактике заболеваний [Интернет]. Атланта: Министерство здравоохранения и социальных служб США; Вакцинация против вируса папилломы человека (ВПЧ): что должен знать каждый; [обновлено 22 ноября 2016 г .; процитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://www.cdc.gov/vaccines/vpd/hpv/public/index.html .
- Лабораторные тесты онлайн [Интернет]. Вашингтон, округ Колумбия: Американская ассоциация клинической химии; c2001–2018 гг. Тест на вирус папилломы человека (ВПЧ); [обновлено 5 июня 2018 г.; процитировано 5 июня 2018 г.]; [около 2 экранов]. Доступно по адресу: https://labtestsonline.org/tests/human-papillomavirus-hpv-test
- Клиника Майо [Интернет]. Фонд Мэйо по медицинскому образованию и исследованиям; c1998–2018 гг. Тест на ВПЧ; 2018 г., 16 мая [цитировано 5 июня 2018 г.]; [около 3 экранов].
 Доступно по адресу: https://www.mayoclinic.org/tests-procedures/hpv-test/about/pac-20394355
Доступно по адресу: https://www.mayoclinic.org/tests-procedures/hpv-test/about/pac-20394355 - McGinley KF, Hey W, Sussman DO, Brown GA. Тестирование на вирус папилломы человека у мужчин. J Am Osteopath Assoc [Интернет]. март 2011 г. [цитировано 9 мая 2020 г.]; 111(3 Приложение2)S:26-8. Доступно по адресу: https://jaoa.org/article.aspx?articleid=2094178 .
- Руководство Merck для потребителей, версия [Интернет]. Кенилворт (Нью-Джерси): Merck & Co., Inc.; c2018. Инфекция вируса папилломы человека (ВПЧ); [цитировано 5 июня 2018 г.]; [около 2 экранов]. Доступно по адресу: https://www.merckmanuals.com/home/infections/sexually-transmitted-diseases-stds/human-papillomavirus-hpv-infection .
- Национальный институт рака [Интернет]. Bethesda (MD): Министерство здравоохранения и социальных служб США; Словарь терминов рака NCI: ВПЧ; [цитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://www.cancer.gov/publications/dictionaries/cancer-terms/def/hpv
- Национальный институт рака [Интернет].
 Bethesda (MD): Министерство здравоохранения и социальных служб США; Словарь терминов рака NCI: Пап-тест; [цитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://www.cancer.gov/publications/dictionaries/cancer-terms/def/pap-test .
Bethesda (MD): Министерство здравоохранения и социальных служб США; Словарь терминов рака NCI: Пап-тест; [цитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://www.cancer.gov/publications/dictionaries/cancer-terms/def/pap-test . - Национальный институт рака [Интернет]. Bethesda (MD): Министерство здравоохранения и социальных служб США; Папаниколау и ВПЧ-тестирование; [цитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://www.cancer.gov/types/cervical/pap-hpv-testing-fact-sheet
- UF Health: Университет здоровья Флориды [Интернет]. Университет Флориды; c2018. Тест на ДНК ВПЧ; [обновлено 5 июня 2018 г.; процитировано 5 июня 2018 г.]; [около 2 экранов]. Доступно по адресу: https://ufhealth.org/hpv-dna-test .
- UW Health [Интернет]. Мэдисон (Висконсин): Управление больниц и клиник Университета Висконсина; c2018. Медицинская информация: Тест на вирус папилломы человека (ВПЧ): как это делается; [обновлено 20 марта 2017 г .; процитировано 5 июня 2018 г.
 ]; [около 5 экранов]. Доступно по адресу: https://www.uwhealth.org/health/topic/medicaltest/human-papillomavirus-hpv-test/tu6451.html#tu6455
]; [около 5 экранов]. Доступно по адресу: https://www.uwhealth.org/health/topic/medicaltest/human-papillomavirus-hpv-test/tu6451.html#tu6455 - UW Health [Интернет]. Мэдисон (Висконсин): Управление больниц и клиник Университета Висконсина; c2018. Медицинская информация: Тест на вирус папилломы человека (ВПЧ): риски; [обновлено 20 марта 2017 г .; процитировано 5 июня 2018 г.]; [около 7 экранов]. Доступно по адресу: HThttps://www.uwhealth.org/health/topic/medicaltest/human-papillomavirus-hpv-test/tu6451.html#tu6457TP
- UW Health [Интернет]. Мэдисон (Висконсин): Управление больниц и клиник Университета Висконсина; c2018. Медицинская информация: Тест на вирус папилломы человека (ВПЧ): результаты; [обновлено 20 марта 2017 г .; процитировано 5 июня 2018 г.]; [около 8 экранов]. Доступно по адресу: https://www.uwhealth.org/health/topic/medicaltest/human-papillomavirus-hpv-test/tu6451.html#tu6458
- UW Health [Интернет]. Мэдисон (Висконсин): Управление больниц и клиник Университета Висконсина; c2018.
 Медицинская информация: Тест на вирус папилломы человека (ВПЧ): Обзор теста; [обновлено 20 марта 2017 г .; процитировано 5 июня 2018 г.]; [около 2 экранов]. Доступно по адресу: https://www.uwhealth.org/health/topic/medicaltest/human-papillomavirus-hpv-test/tu6451.html .
Медицинская информация: Тест на вирус папилломы человека (ВПЧ): Обзор теста; [обновлено 20 марта 2017 г .; процитировано 5 июня 2018 г.]; [около 2 экранов]. Доступно по адресу: https://www.uwhealth.org/health/topic/medicaltest/human-papillomavirus-hpv-test/tu6451.html . - UW Health [Интернет]. Мэдисон (Висконсин): Управление больниц и клиник Университета Висконсина; c2018. Медицинская информация: Тест на вирус папилломы человека (ВПЧ): зачем это делается; [обновлено 20 марта 2017 г .; процитировано 5 июня 2018 г.]; [около 3 экранов]. Доступно по адресу: https://www.uwhealth.org/health/topic/medicaltest/human-papillomavirus-hpv-test/tu6451.html#tu6453
Национальный реестр ювенильного рецидивирующего респираторного папилломатоза | Педиатрия | JAMA Отоларингология – Хирургия головы и шеи
Абстрактный
Фон Рецидивирующий респираторный папилломатоз с юношеским началом (JORRP) — нечастое, но изнурительное заболевание. Поскольку JORRP встречается редко, исследованиям в отдельных учреждениях оказалось сложно точно оценить его естественную историю.
Поскольку JORRP встречается редко, исследованиям в отдельных учреждениях оказалось сложно точно оценить его естественную историю.
Цель Охарактеризовать клинический спектр JORRP.
Дизайн Стандартизированная ретроспективная и проспективная абстракция медицинской карты.
Настройка Двадцать два педиатрических оториноларингологических центра третичной помощи на всей территории Соединенных Штатов.
Пациенты Все пациенты с JORRP моложе 18 лет, осмотренные в период с 1 января 1996 г. по 31 марта 2002 г.
Основные показатели результатов Демографические данные, возраст на момент постановки диагноза, анатомические локализации заболевания, продольное течение заболевания, частота операций, потребность в трахеотомии и медикаментозный анамнез.
Результаты В реестре 603 ребенка. Средний возраст на момент постановки диагноза составил 4,0 года. Дети перенесли в среднем 5,1 операции в год. Текущий возраст, а не возраст на момент постановки диагноза, был основным фактором, определяющим частоту хирургического вмешательства. Гортань была поражена на момент постановки диагноза у 96,1% детей, а у 87,4% была поражена только одна анатомическая область. Дети с поражением 1 локализации были значительно старше на момент постановки диагноза (средний возраст 3,9 года).лет), чем у тех, у кого было 2 сайта (средний возраст 2,9 года). У большинства (74,2%) заболевание стабилизировалось с течением времени, у 5,8% было выявлено прогрессирование папиллом в новые участки, а у 17,9% не было признаков заболевания в течение как минимум 1 года. Детям с прогрессированием заболевания диагноз был поставлен в значительно более молодом возрасте, чем у тех, кто оставался стабильным или выздоровел. Дети, которым потребовалась трахеотомия, значительно чаще имели прогрессирующее заболевание.
Дети перенесли в среднем 5,1 операции в год. Текущий возраст, а не возраст на момент постановки диагноза, был основным фактором, определяющим частоту хирургического вмешательства. Гортань была поражена на момент постановки диагноза у 96,1% детей, а у 87,4% была поражена только одна анатомическая область. Дети с поражением 1 локализации были значительно старше на момент постановки диагноза (средний возраст 3,9 года).лет), чем у тех, у кого было 2 сайта (средний возраст 2,9 года). У большинства (74,2%) заболевание стабилизировалось с течением времени, у 5,8% было выявлено прогрессирование папиллом в новые участки, а у 17,9% не было признаков заболевания в течение как минимум 1 года. Детям с прогрессированием заболевания диагноз был поставлен в значительно более молодом возрасте, чем у тех, кто оставался стабильным или выздоровел. Дети, которым потребовалась трахеотомия, значительно чаще имели прогрессирующее заболевание.
Выводы Реестр установил клиническое течение JORRP в большой репрезентативной выборке США. Молодой возраст был наиболее важным фактором, определяющим тяжесть заболевания (частота операций, степень заболевания на момент постановки диагноза и прогрессирование заболевания). Решение вопросов патогенеза и течения заболевания потребует пересмотра инструмента сбора данных и молекулярного анализа тканей.
Молодой возраст был наиболее важным фактором, определяющим тяжесть заболевания (частота операций, степень заболевания на момент постановки диагноза и прогрессирование заболевания). Решение вопросов патогенеза и течения заболевания потребует пересмотра инструмента сбора данных и молекулярного анализа тканей.
РЕЦИДИВНЫЙ РЕСПИРАТОРНЫЙ ПАПИЛЛОМАТОЗ (РРП) характеризуется повторным ростом бородавок в гортани и других отделах дыхательных путей. Вирус папилломы человека (ВПЧ), обычно типа 6 или 11, вызывает RRP. 1 ,2 Эти типы ВПЧ связаны с аногенитальными кондиломами и имеют низкий риск злокачественной трансформации. Рецидивирующий респираторный папилломатоз в педиатрических возрастных группах, обычно обозначаемый как RRP с ювенильным началом (JORRP), встречается редко, с оценками распространенности от 1,7 до 2,6 на 100 000 детей в Соединенных Штатах. 3 ,4 Хотя редко, JORRP является наиболее частым новообразованием верхних дыхательных путей у детей. 5 РРП с началом в юношеском возрасте может сохраняться в течение многих лет, приводя к физическим и эмоциональным последствиям, и не менее 110 миллионов долларов в год тратится на прямые медицинские расходы. 4
5 РРП с началом в юношеском возрасте может сохраняться в течение многих лет, приводя к физическим и эмоциональным последствиям, и не менее 110 миллионов долларов в год тратится на прямые медицинские расходы. 4
Понимание эпидемиологических характеристик JORRP позволит исследователям и врачам лучше понять, как контролировать и, в конечном счете, предотвращать заболевание. Однако низкая распространенность JORRP ограничивает количество пациентов в одном учреждении, и остается много вопросов об этом заболевании. 6 РРП с ювенильным началом чаще всего диагностируется у детей в возрасте от 2 до 3 лет. Охриплость или изменение голоса являются обычными начальными проявлениями. Реже обструкция дыхательных путей папилломами приводит к респираторному стридору или острому респираторному дистресс-синдрому. Лечение направлено на устранение обструктивных поражений, а не на устранение всей пораженной или инфицированной ткани. 7 Повторное лечение рецидивов может привести к образованию паутины и необратимому повреждению голосовых связок. РРП с началом в юношеском возрасте различается по степени тяжести: некоторым детям требуется небольшое количество лечения, в то время как другим требуется несколько операций в месяц. У большинства детей заболевание проходит, а у других сохраняется и во взрослом возрасте. 8 ,9 Исследования не выявили последовательных этнических или социально-экономических ассоциаций с возникновением JORRP или его ранними проявлениями или клиническим течением.
РРП с началом в юношеском возрасте различается по степени тяжести: некоторым детям требуется небольшое количество лечения, в то время как другим требуется несколько операций в месяц. У большинства детей заболевание проходит, а у других сохраняется и во взрослом возрасте. 8 ,9 Исследования не выявили последовательных этнических или социально-экономических ассоциаций с возникновением JORRP или его ранними проявлениями или клиническим течением.
В январе 1997 г. Центры по контролю и профилактике заболеваний запустили Национальный регистр юношеского рецидивирующего респираторного папилломатоза для сбора информации о достаточном количестве пациентов для систематической оценки естественного течения болезни. Это анализ информации реестра, собранной за 5 лет работы.
Методы
Комитеты субъектов-людей Центров по контролю и профилактике заболеваний и участвующих учреждений одобрили протокол исследования. При проведении этого исследования соблюдались рекомендации по проведению экспериментов на людях Министерства здравоохранения и социальных служб США.
Опубликованы подробные сведения о ведении Национального регистра ювенильного рецидивирующего респираторного папилломатоза. 10 Вкратце, реестр включает информацию обо всех детях моложе 18 лет с РРП, которые прошли лечение в 22 участвующих медицинских центрах третичной помощи на всей территории Соединенных Штатов. Когда реестр был инициирован 19 января97, были собраны ретроспективные данные обо всех распространенных случаях, зарегистрированных в течение предыдущего года. Инцидентные случаи были добавлены во время диагностики. Персонал регистратуры извлекал информацию из медицинских карт при каждом посещении, связанном с RRP, до тех пор, пока пациенты не выпадали из-под наблюдения, не переводились в другой медицинский центр, не зарегистрированный в реестре, или не умирали. Этот анализ включает информацию, сгруппированную по март 2002 г.
Данные из регистра представляют собой когорту детей, зарегистрированных в разном возрасте, за которыми проводились повторные измерения с различными интервалами. Мы оценили агрессивность заболевания на основе частоты операций, необходимости трахеотомии и анатомической распространенности заболевания. Мы рассчитали среднегодовую частоту хирургических вмешательств по стандартной методике. 11
Мы оценили агрессивность заболевания на основе частоты операций, необходимости трахеотомии и анатомической распространенности заболевания. Мы рассчитали среднегодовую частоту хирургических вмешательств по стандартной методике. 11
Статистический анализ проводили с использованием SYSTAT, версия 9 (SPSS Inc, Чикаго, Иллинойс). Цифры могут варьироваться в зависимости от анализа из-за отсутствия информации (например, возраст и этническая принадлежность). Мы использовали тест χ 2 для сравнения категорийных данных, тест t или тест t с парной выборкой для нормально распределенных непрерывных данных и статистику Манна-Уитни для ненормально распределенных непрерывных данных.
Полученные результаты
Реестр включал данные о 603 детях из мест по всей территории Соединенных Штатов (рис. 1). Средний возраст при постановке диагноза составил 3,1 года (диапазон от 1 месяца до 17 лет, средний возраст 4,0 года). Мальчиков немного больше, чем девочек (304 и 299 соответственно). Большинство пациентов (380 [63,0%)] были белыми, 171 (28,4%) были черными, а остальные были коренными американцами (5 [0,8%]), азиатами (5 [0,8%]) и другими или неизвестными (42 [0,8%]). 7,0%]). Этническая принадлежность была указана для 367 (60,9%) пациентов; 57 (15,5%) были идентифицированы как латиноамериканцы и 310 (84,5%) как белые или черные неиспаноязычные. Около половины (280 [46,4%)] пациентов были охвачены Medicaid.
Мальчиков немного больше, чем девочек (304 и 299 соответственно). Большинство пациентов (380 [63,0%)] были белыми, 171 (28,4%) были черными, а остальные были коренными американцами (5 [0,8%]), азиатами (5 [0,8%]) и другими или неизвестными (42 [0,8%]). 7,0%]). Этническая принадлежность была указана для 367 (60,9%) пациентов; 57 (15,5%) были идентифицированы как латиноамериканцы и 310 (84,5%) как белые или черные неиспаноязычные. Около половины (280 [46,4%)] пациентов были охвачены Medicaid.
За клиническим течением заболевания у детей наблюдали в среднем в течение 3,6 лет (диапазон от 9 месяцев до 18 лет; в среднем 4,9 года). Дети перенесли от 2 до 179 (в среднем 21,6; медиана 13,0) хирургических вмешательств в течение жизни по поводу своего заболевания. Не было отмечено существенных различий в отношении частоты операций при анализе групп пациентов по полу, этническому происхождению или страховому покрытию Medicaid. Количество операций в год колебалось от 0,4 до 21,5 (в среднем 5,1; медиана 4,3). Дети, у которых был диагностирован РРП до 4-летнего возраста, имели значительно больше ежегодных операций, чем дети, диагностированные в более старшем возрасте (рис. 2). Дети младшего возраста также ежегодно подвергались значительно большему количеству операций (рис. 3). Чтобы изучить возможные взаимодействия между возрастом на момент постановки диагноза и возрастом на момент операции, мы нанесли на график возрастную частоту операций для когорт, определенных по возрасту на момент постановки диагноза, для всех случаев (рис. 4). Когорты возраста на момент постановки диагноза показали аналогичные среднегодовые операции для каждого периода времени на момент лечения.
Дети, у которых был диагностирован РРП до 4-летнего возраста, имели значительно больше ежегодных операций, чем дети, диагностированные в более старшем возрасте (рис. 2). Дети младшего возраста также ежегодно подвергались значительно большему количеству операций (рис. 3). Чтобы изучить возможные взаимодействия между возрастом на момент постановки диагноза и возрастом на момент операции, мы нанесли на график возрастную частоту операций для когорт, определенных по возрасту на момент постановки диагноза, для всех случаев (рис. 4). Когорты возраста на момент постановки диагноза показали аналогичные среднегодовые операции для каждого периода времени на момент лечения.
Информация о степени заболевания на момент постановки диагноза была доступна для 580 детей (96,2%) (табл. 1). Большинство (507 [87,4%]) имели папилломы, ограниченные 1 местом, обычно гортанью (487 [84,0%]). У 57 человек было заболевание в 2 локализациях, у 15 — в 3 локализациях и у 1 пациента — в 4 локализациях. Пол, этническая принадлежность и покрытие Medicaid не были связаны со степенью заболевания. Дети с заболеванием, ограниченным 1 участком, были значительно старше на момент постановки диагноза (средний возраст 3,9 года; медиана возраста 3,0 года), чем дети с папилломами 2 (средний возраст 2,9 года).годы; средний возраст 2,4 года) или 3 (средний возраст 2,7 года; средний возраст 1,1 года) участков ( P = 0,02, статистика Манна-Уитни). Лица с заболеванием гортани или выше были значительно старше на момент постановки диагноза (средний возраст 4,6 года, медиана возраста 3,3 года), чем пациенты с заболеванием гортани или ниже (средний возраст 2,1 года, медиана возраста 1,7 года) (). P = 0,009, статистика Манна-Уитни). Наконец, среди детей с папилломами 1 локализации дети с поражением выше гортани были значительно старше (средний возраст 9 лет)..0 лет; средний возраст 6,8 года), чем у пациентов с поражением гортани (средний возраст 3,7 года; средний возраст 2,9 года) ( P <0,001, статистика Манна-Уитни).
Дети с заболеванием, ограниченным 1 участком, были значительно старше на момент постановки диагноза (средний возраст 3,9 года; медиана возраста 3,0 года), чем дети с папилломами 2 (средний возраст 2,9 года).годы; средний возраст 2,4 года) или 3 (средний возраст 2,7 года; средний возраст 1,1 года) участков ( P = 0,02, статистика Манна-Уитни). Лица с заболеванием гортани или выше были значительно старше на момент постановки диагноза (средний возраст 4,6 года, медиана возраста 3,3 года), чем пациенты с заболеванием гортани или ниже (средний возраст 2,1 года, медиана возраста 1,7 года) (). P = 0,009, статистика Манна-Уитни). Наконец, среди детей с папилломами 1 локализации дети с поражением выше гортани были значительно старше (средний возраст 9 лет)..0 лет; средний возраст 6,8 года), чем у пациентов с поражением гортани (средний возраст 3,7 года; средний возраст 2,9 года) ( P <0,001, статистика Манна-Уитни).
Из 469 детей с достаточной информацией для оценки клинического течения большинство (348 [74,2%]) были стабильными, без изменений в количестве анатомических участков, пораженных папилломами; у 27 (5,8%) заболевание прогрессировало на дополнительные анатомические участки, а у 94 (20,0%) заболевание регрессировало с меньшим количеством вовлеченных участков (таблица 2). Из тех, у кого болезнь регрессировала, 84 (890,4%) не болели в течение как минимум 1 года. Не было отмечено различий в клиническом течении в зависимости от пола, этнической принадлежности или охвата Medicaid. В период с 1 января 1996 г. по 31 марта 2002 г. папилломы, ограниченные гортанью, были диагностированы у 171 ребенка (инцидентные случаи). свободны или имели стабильное заболевание (рис. 5). Принимая во внимание только случайные случаи, контроль «предвзятости выжившего» и результаты были одинаково значимыми среди всех 487 детей с заболеванием, ограниченным гортанью на момент постановки диагноза. Интересно, что данные о клиническом течении были доступны для 10 из 20 детей с папилломами только над гортанью на момент постановки диагноза. Двое выздоровели, а 8 остались стабильными, папилломы были ограничены исходным местом.
Из тех, у кого болезнь регрессировала, 84 (890,4%) не болели в течение как минимум 1 года. Не было отмечено различий в клиническом течении в зависимости от пола, этнической принадлежности или охвата Medicaid. В период с 1 января 1996 г. по 31 марта 2002 г. папилломы, ограниченные гортанью, были диагностированы у 171 ребенка (инцидентные случаи). свободны или имели стабильное заболевание (рис. 5). Принимая во внимание только случайные случаи, контроль «предвзятости выжившего» и результаты были одинаково значимыми среди всех 487 детей с заболеванием, ограниченным гортанью на момент постановки диагноза. Интересно, что данные о клиническом течении были доступны для 10 из 20 детей с папилломами только над гортанью на момент постановки диагноза. Двое выздоровели, а 8 остались стабильными, папилломы были ограничены исходным местом.
Трахеотомию, как правило, выполняли детям младшего возраста, но не было статистически значимой разницы в распределении возраста на момент постановки диагноза между теми, кто получал (средний возраст 3,2 года; медиана возраста 1,8 года) и не получал (средний возраст, 3,8 года, медиана возраста 3,0 года) трахеотомия. Пол, этническая принадлежность и покрытие Medicaid были одинаковыми среди детей, которым требовалась и не требовалась трахеотомия. Трахеотомия выполнялась значительно чаще у детей, у которых RRP прогрессировал с вовлечением новых локализаций, чем у детей со стабильным или улучшающимся заболеванием (табл. 3). Связь была сильнее, когда анализ был ограничен пациентами с заболеванием, при диагнозе ограниченном гортанью. Среди детей, которым потребовалась трахеотомия, не было очевидной связи прогрессирования заболевания с возрастом, этнической принадлежностью или покрытием Medicaid.
Пол, этническая принадлежность и покрытие Medicaid были одинаковыми среди детей, которым требовалась и не требовалась трахеотомия. Трахеотомия выполнялась значительно чаще у детей, у которых RRP прогрессировал с вовлечением новых локализаций, чем у детей со стабильным или улучшающимся заболеванием (табл. 3). Связь была сильнее, когда анализ был ограничен пациентами с заболеванием, при диагнозе ограниченном гортанью. Среди детей, которым потребовалась трахеотомия, не было очевидной связи прогрессирования заболевания с возрастом, этнической принадлежностью или покрытием Medicaid.
12 детей с трахеотомией, у которых заболевание прогрессировало с вовлечением дополнительных анатомических участков, подверглись процедуре от 7 дней до 28,8 месяцев (в среднем 7,8 месяцев; медиана 3,1 месяца) до прогрессирования заболевания. 35 детей с трахеотомией, у которых РРП оставалась стабильной или регрессировала, наблюдались в среднем в течение 77 месяцев (медиана 59,3 месяца; диапазон 1,6–209,6 месяца) после процедуры, и у 15 (42,9%) канюли были на месте в последний раз. клиническая оценка.
клиническая оценка.
Несмотря на то, что все субъекты подвергались хирургическому лечению, в реестр также была включена информация об использовании вспомогательной терапии (таблица 4). Такие данные имелись у 387 больных, из них 184 (47,6%) помимо операции прошли хотя бы 1 курс терапии. Наиболее часто применялся интерферон (у 77 [41,9%] детей, получающих вспомогательную терапию). Интерферон назначался в различных формах (интерферон альфа-2b, общий интерферон, интерферон альфа-2а и интерферон альфа) в дозах от 500 000 до 7,8 млн ЕД (в среднем 3,1 млн ЕД; медиана 3 млн ЕД). Интерферон обычно вводили подкожно (80,1% времени), реже внутримышечно (10,6% времени) или внутри очага поражения (9,8% времени). Четырнадцать детей (7,6%) получали ацикловир перорально в дозах от 50 до 400 мг (в среднем 260 мг) один или два раза в день. Тринадцати (17,1%) вводили цидофовир внутриочагово в дозах от 0,19и 21,5 мг (в среднем 7,0 мг). Задокументировано, что 53 ребенка (28,8%) получали различные формы индол-3-карбинола в качестве адъювантной терапии. 67 детей (36,4%) прошли 2 различных курса вспомогательной терапии, при этом распределение используемых препаратов было сходным. Использование вспомогательной терапии было одинаковым в 22 центрах регистра, за исключением 1, где все пациенты, включенные в исследование, получали вспомогательную терапию. Не было никаких существенных различий в лекарствах, используемых в разных больницах. В целом, дети, получавшие вспомогательную терапию, чаще оперировались до терапии (среднегодовые операции 6,3 против 4,2; 9).0189 P <0,001, статистика Манна-Уитни) и были диагностированы в более молодом возрасте (средний возраст 2,4 против 4,1 года; P <0,001, статистика Манна-Уитни), чем те, у кого этого не было.
67 детей (36,4%) прошли 2 различных курса вспомогательной терапии, при этом распределение используемых препаратов было сходным. Использование вспомогательной терапии было одинаковым в 22 центрах регистра, за исключением 1, где все пациенты, включенные в исследование, получали вспомогательную терапию. Не было никаких существенных различий в лекарствах, используемых в разных больницах. В целом, дети, получавшие вспомогательную терапию, чаще оперировались до терапии (среднегодовые операции 6,3 против 4,2; 9).0189 P <0,001, статистика Манна-Уитни) и были диагностированы в более молодом возрасте (средний возраст 2,4 против 4,1 года; P <0,001, статистика Манна-Уитни), чем те, у кого этого не было.
Комментарий
Данные Национального регистра ювенильного рецидивирующего респираторного папилломатоза у 603 детей со средней продолжительностью наблюдения 4,9 года дают наиболее полную картину эпидемиологических характеристик и клинического течения JORRP на сегодняшний день. Реестр документирует значительную заболеваемость, связанную с JORRP. Детям было проведено 10 361 хирургическое вмешательство, а в среднем учащиеся перенесли 5,1 операции в год. Предыдущие исследования 1 ,6 ,12 сообщили, что ранний возраст при постановке диагноза был в значительной степени связан с агрессивностью заболевания (определяемой частотой операций). Тем не менее, когортный анализ, который мы провели, показал, что текущий возраст, а не возраст на момент постановки диагноза, был основным фактором, определяющим частоту хирургического вмешательства. Скорее всего, это связано с тем, что у детей младшего возраста дыхательные пути меньше, и поэтому им требуются более частые операции для поддержания проходимости, но нельзя исключать изменения иммунной компетентности или вирусной нагрузки с возрастом.
Реестр документирует значительную заболеваемость, связанную с JORRP. Детям было проведено 10 361 хирургическое вмешательство, а в среднем учащиеся перенесли 5,1 операции в год. Предыдущие исследования 1 ,6 ,12 сообщили, что ранний возраст при постановке диагноза был в значительной степени связан с агрессивностью заболевания (определяемой частотой операций). Тем не менее, когортный анализ, который мы провели, показал, что текущий возраст, а не возраст на момент постановки диагноза, был основным фактором, определяющим частоту хирургического вмешательства. Скорее всего, это связано с тем, что у детей младшего возраста дыхательные пути меньше, и поэтому им требуются более частые операции для поддержания проходимости, но нельзя исключать изменения иммунной компетентности или вирусной нагрузки с возрастом.
Наши результаты согласуются с предыдущими выводами о том, что JORRP обычно затрагивает гортань. 9 Наши данные, представляющие большую тщательно наблюдаемую когорту детей из основных центров третичной медицинской помощи на всей территории Соединенных Штатов, задокументировали сильную связь между возрастом на момент постановки диагноза и степенью и прогрессированием заболевания. Наблюдалась значительная тенденция к уменьшению возраста на момент постановки диагноза, связанная с увеличением числа пораженных участков. Что еще более важно, существовала значительная связь между более молодым возрастом при постановке диагноза и появлением папиллом ниже гортани. Почти у 6% детей заболевание прогрессировало на соседние анатомические области. Молодой возраст при постановке диагноза был в значительной степени связан с прогрессированием заболевания у детей с поражениями, ограниченными гортанью на момент постановки диагноза. Наконец, наши данные также отражают, что JORRP, ограниченный участками выше гортани, отличается от такового в гортани и ниже. Дети с поражением верхних дыхательных путей значительно старше и, по-видимому, хорошо справляются с болезнью, при этом в нашем исследовании не было признаков распространения.
Наблюдалась значительная тенденция к уменьшению возраста на момент постановки диагноза, связанная с увеличением числа пораженных участков. Что еще более важно, существовала значительная связь между более молодым возрастом при постановке диагноза и появлением папиллом ниже гортани. Почти у 6% детей заболевание прогрессировало на соседние анатомические области. Молодой возраст при постановке диагноза был в значительной степени связан с прогрессированием заболевания у детей с поражениями, ограниченными гортанью на момент постановки диагноза. Наконец, наши данные также отражают, что JORRP, ограниченный участками выше гортани, отличается от такового в гортани и ниже. Дети с поражением верхних дыхательных путей значительно старше и, по-видимому, хорошо справляются с болезнью, при этом в нашем исследовании не было признаков распространения.
Регистр также подтвердил, что у пациентов с JORRP, которым требуется трахеотомия, чаще проявляется прогрессирующее заболевание, распространяющееся на новые участки. 2 ,13 ,14 Данные не позволили решить, свидетельствует ли это просто о необходимости выполнения трахеотомии у детей с тяжелым прогрессирующим заболеванием или о независимой связи между необходимостью трахеотомии и последующим прогрессированием JORRP. Только рандомизированное проспективное исследование могло бы прояснить этот вопрос. 13 Интересно, что возраст на момент постановки диагноза не был связан с необходимостью трахеотомии. Как и в случае с количеством процедур, мы ограничили наш анализ детьми с RRP, ограниченным гортанью на момент постановки диагноза (чтобы уменьшить путаницу). Наши результаты контрастируют с предыдущими исследованиями 2 ,13 , показавшими, что у пациентов с JORRP, требующих трахеотомии, диагноз ставится в более молодом возрасте, чем у тех, кому процедура не требуется.
2 ,13 ,14 Данные не позволили решить, свидетельствует ли это просто о необходимости выполнения трахеотомии у детей с тяжелым прогрессирующим заболеванием или о независимой связи между необходимостью трахеотомии и последующим прогрессированием JORRP. Только рандомизированное проспективное исследование могло бы прояснить этот вопрос. 13 Интересно, что возраст на момент постановки диагноза не был связан с необходимостью трахеотомии. Как и в случае с количеством процедур, мы ограничили наш анализ детьми с RRP, ограниченным гортанью на момент постановки диагноза (чтобы уменьшить путаницу). Наши результаты контрастируют с предыдущими исследованиями 2 ,13 , показавшими, что у пациентов с JORRP, требующих трахеотомии, диагноз ставится в более молодом возрасте, чем у тех, кому процедура не требуется.
Реестр имеет 2 важных ограничения в отношении клинического течения и распространенности заболевания. Во-первых, медиана наблюдения составила всего 4,3 года. Во-вторых, природа регистра ограничивала данные, которые мы могли собрать, ограничивая наш анализ тяжести при постановке диагноза и вовлечении общих анатомических областей в клиническое течение. Мы разработали формы для сбора регистрационных данных, которые могут быть заполнены занятым персоналом клиники путем просмотра медицинской карты и минимально мешать работе клиники. Мы планировали, что это будет предварительная работа, которая будет развиваться.
Во-вторых, природа регистра ограничивала данные, которые мы могли собрать, ограничивая наш анализ тяжести при постановке диагноза и вовлечении общих анатомических областей в клиническое течение. Мы разработали формы для сбора регистрационных данных, которые могут быть заполнены занятым персоналом клиники путем просмотра медицинской карты и минимально мешать работе клиники. Мы планировали, что это будет предварительная работа, которая будет развиваться.
Необходимо собрать и проанализировать данные о поражении гортани. Было предложено несколько систем стадирования и оценки, но ни одна из них не получила широкого признания среди клиницистов и исследователей. 15 ,16 В ответ на потребность в деталях и единообразии разработчиками наиболее широко используемых шкал серьезности была предложена новая система стадирования. 16 Он включает субъективную функциональную оценку клинических факторов и анатомическую оценку распространения заболевания. Функциональные и анатомические показатели можно использовать в комбинации для оценки клинического течения заболевания и ответа на терапию у отдельного пациента. Эта система стадирования была проанализирована в ходе валидационного испытания и продемонстрировала превосходную воспроизводимость от хирурга к хирургу с минимальной вариабельностью в оценке одних и тех же поражений. 17 Эта система может быть полезна для стандартизации будущей документации и расширения полезности реестра.
Эта система стадирования была проанализирована в ходе валидационного испытания и продемонстрировала превосходную воспроизводимость от хирурга к хирургу с минимальной вариабельностью в оценке одних и тех же поражений. 17 Эта система может быть полезна для стандартизации будущей документации и расширения полезности реестра.
Наш анализ клинического течения и тяжести JORRP также был ограничен характером данных, полученных при просмотре медицинской карты. Вирус папилломы человека вызывает JORRP, и для более подробного объяснения клинических аспектов JORRP необходимо изучить анализ вирусных факторов и реакции хозяина на инфекцию. 1 ,6 Вирус папилломы человека типов 6 и 11 вызывает большинство случаев JORRP, и считается, что ВПЧ 11 предвещает плохой прогноз для ремиссии. 8 Однако нет единого мнения относительно связи между типом ВПЧ и клинической тяжестью. 18 ,19 Возможно, с более эффективными методами современной полимеразной цепной реакции и количеством потенциальных образцов, доступных в реестре, вопрос о геномных различиях в заражении вирусной ДНК может быть решен.
Наверх
Информация о статье
Соответствующий автор и перепечатки: Уильям С. Ривз, доктор медицинских наук, отделение вирусных экзантем и вирусов герпеса, отделение вирусных и риккетсиозных заболеваний, Национальный центр инфекционных заболеваний, Центры по контролю и профилактике заболеваний, 1600 Clifton Rd NE, Mail Stop A-15 , Атланта, Джорджия 30333 (электронная почта: [email protected]).
Поступила в печать 21 октября 2002 г.; принято 6 января 2003 г.
Мы благодарим координаторов сайта Национального регистра юношеского рецидивирующего респираторного папилломатоза за тщательный сбор данных: A. Ahmed, RN; Т. Бладворт, RN; Дж. Бокмейер, Р.Н.; С. Баклер, Р.Н.; Д. Берк, Р.Н.; Л. Голембиевски, Р.Н.; Т. Холмс, Р.Н.; Б. Иман, Р.Н.; Дж. Ленхерр, Р.Н.; Л. Льюис, Р.Н.; Дж. Магнотта, Р.Н.; В. Маллули, Р.Н.; Д. Филлипс, Р.Н.; Д. Пратер, Р.Н.; К. Рамирес, Р.Н.; К. Реймер, Р.Н.; М. Райхерт, Р.Н.; К. Селф, Р.Н.; М. Симмонс, Р.Н.; К. Салливан, Р.Н.; Ю. Стерн, доктор медицины; Дж. Вольфенбаргер, Р.Н.; и М. Юрский, РН.
Селф, Р.Н.; М. Симмонс, Р.Н.; К. Салливан, Р.Н.; Ю. Стерн, доктор медицины; Дж. Вольфенбаргер, Р.Н.; и М. Юрский, РН.
Полный список основных исследователей Целевой группы RRP был опубликован ранее ( Arch Otolaryngol Head Neck Surg . 1999;125:743-748).
Рекомендации
1.
Гэббот MCossart Екан Конопка Мчан RRозе BR Папилломавирус человека и переменные хозяина как предикторы клинического течения у пациентов с ювенильным рецидивирующим респираторным папилломатозом. J Clin Microbiol. 1997;35:3098-3103.PubMedGoogle Scholar
2.
Rimell
FLСапожник
DLPou
AMJordan
JAPost
JCEhrlich
GC Детский респираторный папилломатоз: прогностическая роль вирусного типирования и кофакторов. Ларингоскоп. 1997;107:915-918.PubMedGoogle Scholar
1997;107:915-918.PubMedGoogle Scholar
3.
Армстронг LR Престон EJDReichert М и др. Заболеваемость и распространенность рецидивирующего респираторного папилломатоза среди детей в Атланте и Сиэтле. Клин Инфекция Дис. 2000;31:107-109.PubMedGoogle Scholar
4.
Деркей CS Целевая группа по рецидивирующим респираторным папилломам. Arch Otolaryngol Head Neck Surg. 1995;121:1386-1391.PubMedGoogle Scholar
5.
Джонс Смайерс G Доброкачественные новообразования гортани. Отоларингол Clin North Am. 1984;17:151-178.PubMedGoogle Scholar
6.
Аалтонен
Л.М.Рихканен
ХВахери
Вирус папилломы человека в гортани. Ларингоскоп. 2002;112:700-707.PubMedGoogle Scholar
Ларингоскоп. 2002;112:700-707.PubMedGoogle Scholar
7.
Деркей CS Рецидивирующий респираторный папилломатоз: клинический обзор. Ларингоскоп. 2001;111:52-68.PubMedGoogle Scholar
8.
Бауман НМСмит RJH Рецидивирующий респираторный папилломатоз. Педиатрическая клиника North Am. 1996;43:1385-1401.PubMedGoogle Scholar
9.
Кашима HMounts Плевенталь БХрубан RH Места предрасположенности к рецидивирующему респираторному папилломатозу. Энн Отол Ринол Ларингол. 1993;102:580-583.PubMedGoogle Scholar
10.
Армстронг
LRDerkay
CSReeves
WC for the RRP Task Force Первоначальные результаты из Национального реестра ювенильных рецидивирующих респираторных папилломатозов. Arch Otolaryngol Head Neck Surg. 1999;125:743-748.PubMedGoogle Scholar
Arch Otolaryngol Head Neck Surg. 1999;125:743-748.PubMedGoogle Scholar
11.
Бреслоу NEDay NE Дизайн и анализ когортных исследований. В: Статистические методы в исследованиях рака . Том 2. Лион, Франция: Международное агентство по изучению рака; 1987: 48-51. Научная публикация IARC 82. Google Scholar
12.
Куини РЭУэллс М.Льюис FATerry РММайклс ЛКрофт CB Папилломатоз гортани: корреляция между тяжестью заболевания и наличием ВПЧ 6 и 11, обнаруженным с помощью гибридизации ДНК in situ. Джей Клин Патол. 1989;42:694-698.PubMedGoogle Scholar
13.
Шапиро
А.М.Римелл
FLСапожник
DPou
AStool
SE Трахеотомия у детей с ювенильным рецидивирующим респираторным папилломатозом: опыт Детской больницы Питтсбурга. Энн Отол Ринол Ларингол. 1996;105:1-5.PubMedGoogle Scholar
Энн Отол Ринол Ларингол. 1996;105:1-5.PubMedGoogle Scholar
14.
Коул RRMyer CMХлопок ЛТ Трахеотомия у детей с рецидивирующим респираторным папилломатозом. Голова Шея. 1989;11:226-230.PubMedGoogle Scholar
15.
Кашима HMounts Плевенталь BMounts Группа по изучению папилломы Система баллов для оценки тяжести и течения рецидивирующего респираторного папилломатоза при папилломавирусах: молекулярные и клинические аспекты . Нью-Йорк, штат Нью-Йорк: Alan R Liss Inc; 1985.
16.
Деркей
CMalis
Дзалзал
GWiatrak
БКашима
HCotrera
M Система стадирования для оценки тяжести заболевания и ответа на терапию при рецидивирующем респираторном папилломатозе.
